2. 重庆惠能标普科技有限公司, 重庆 401121;
3. 重庆医药高等专科学校 药学院, 重庆 401331
2. Chongqing Huinengbiaopu Technology Co. Ltd., Chongqing 401121, P. R. China;
3. College of Pharmacy, Chongqing Medical and Pharmaceutical College, Chongqing 401331, P. R. China
肼又称联氨,具有强还原性[1-2],是生产各种聚合物、药物等化工产品的原料,广泛应用于化工、医药、航天和军事等领域[3-7]。但肼有高毒性,对皮肤及粘膜有强烈的腐蚀作用,能引起肝和血液的损伤,是公认的致癌物[8-10]。因此,许多国家对肼在空气中的含量都有严格的限制,美国政府工业卫生工作者会议规定空气中肼的最高允许浓度为0.01 mg/m3,中国卫生部规定工作场所空气中肼的职业接触限值为0.06 mg/m3[11],因此,检测职业环境中的肼必须有高灵敏度的检测方法。
肼的测定方法主要有化学分析法、电化学分析法、荧光光谱法、分光光度法和气相色谱法等[11-16]。其中气相色谱分析法具有快速、准确、灵敏度高等特点[17],因此被用于肼的职业卫生检测。肼的分子结构简单,气相色谱的氢火焰检测法直接分析的响应低,无法准确定量,所以需经过衍生再进行检测分析,以实现灵敏的响应[16, 18-19]。肼糠醛衍生分析法的本质是样品肼的糠醛衍生产物经过填充柱分离,再经检测器获得该衍生产物的定性定量信息,结果是通过对肼衍生物的定量来实现对肼的等量代换。然而,不同实验室使用的分离柱千差万别,越来越多的实验室使用通用分离柱(毛细管柱),方法提供的标准物质又是肼而非肼的糠醛衍生物,在此情况下,如何根据所在实验室的仪器及分离柱等条件,证明肼完全衍生转化成单一的目标产物,探索理想的分析条件,确保能用该目标产物的定性定量信息对肼进行准确定量,目前尚无相关的研究报道。
笔者拟用过量糠醛与肼反应合成肼糠醛衍生物,经质谱定性结构,再用已定性结构的纯净糠醛衍生产物晶体与溶剂、衍生试剂糠醛等对比分析,获得可靠的定性定量分析信息,探索分析检测最佳条件,建立适于不同实验室仪器与色谱柱条件下气相色谱快速、准确分析肼的方法及条件探索程序。
1 实验部分 1.1 主要仪器与试剂所用的主要仪器包括质谱仪(PerkinElmer Clarus SQ8T)、气相色谱仪配FID检测器(PerkinElmer Clarus 680)、毛细管柱(PerkinElmer,Elite-WAX-ETR,30 m×0.25 mm×0.25 μm)、超纯水机(Millipore, Elix3)。
肼标准溶液:在100.0 mL容量瓶中加入一定量0.2 mol/L的硫酸(分析纯,成都艾科达化学试剂有限公司)溶液,准确称量后,加入烘干的硫酸肼(分析纯,成都艾科达化学试剂有限公司),再准确称量,得硫酸肼的质量为0.203 1 g,加0.2 mol/L硫酸溶液至刻度,得到浓度为500.0 mg/L的标准贮备液,临用前,取1.0 mL于100.0 mL的容量瓶中,用0.2 mol/L硫酸溶液稀释定容,得到5.00 mg/L的肼标准应用液。衍生剂:临用前,用0.5 mol/L乙酸钠(优级纯,成都科龙试剂有限公司)溶液稀释4.0 mL经重新蒸馏的糠醛(优级纯,成都西亚试剂有限公司)至100.0 mL。乙酸乙酯(色谱纯,成都科龙试剂有限公司),实验用水均为超纯水。
1.2 实验方法 1.2.1 糠醛衍生物的合成称取0.80 g烘干的硫酸肼溶于50.0 mL的0.2 mol/L硫酸溶液中,另取1.2 mL经过重新蒸馏过的糠醛,用0.5 mol/L乙酸钠溶液稀释至50.0 mL,将上述两种溶液混合均匀,室温反应静置得淡黄色结晶,过滤后先后用少量超纯水和乙酸乙酯洗涤晶体,风干备用。
1.2.2 质谱定性用0.5 mol/L乙酸钠溶液稀释0.2 mL新蒸的糠醛成20.0 mL糠醛溶液。称取糠醛衍生物晶体0.100 0 g,用乙酸乙酯溶解成100.0 mL溶液。在汽化室温度300 ℃、柱温210 ℃、离子源温度230 ℃、EM电压1 888 V、溶剂延迟时间6 min条件下,在m/35~300范围内分别对上述两种样品进行全扫描,对比定性分析糠醛和糠醛衍生物。
1.2.3 色谱分析肼标准溶液或样品溶液用0.2 mol/L的硫酸溶液稀释定容到2.0 mL,加入2.0 mL衍生剂,振摇后静置反应1 h,用0.5 mL乙酸乙酯萃取1 min。在汽化室温度300 ℃、柱温210 ℃、氢火焰检测器温度350 ℃、载气流速2.0 mL/min、分流比10:1等色谱条件下,取2.0 μL萃取液进行气相色谱分析。
1.2.4 方法评价实验线性范围实验:准确配制浓度为0.25,0.50,0.75,1.00,1.25 mg/L肼系列标准溶液2.0 mL,加入2.0 mL衍生剂,后续处理同步骤1.2.3,以峰面积为纵坐标、质量浓度为横坐标绘制标准曲线。
检出限测定:配制0.10 mg/L的肼标准溶液,加入2.0 mL衍生剂,后续处理同步骤1.2.3,平行测定11次。
精密度实验:分别配制浓度为0.25,0.50,1.00 mg/L的肼标准溶液,衍生化等后续操作同步骤1.2.3,各平行测定6次。
准确性(回收率)实验:用5.00 mg/L的肼标准应用液分别配制2.0 mL浓度分别为0.50 mg/L和1.25 mg/L的肼质控样,衍生化、萃取及后续操作同步骤1.2.3,进行空白加标回收实验。
2 结果及讨论 2.1 肼的衍生转化肼的糠醛衍生可能按式(1)与肼进行单分子糠醛衍生,也可能按式(2)与两分子糠醛形成衍生产物。
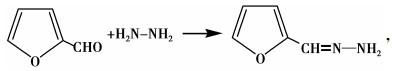
|
(1) |
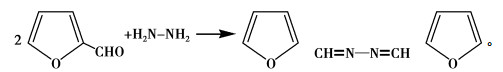
|
(2) |
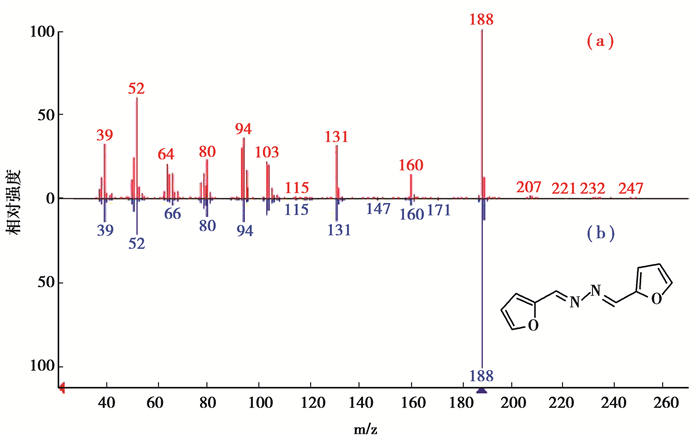
实验采用过量的衍生剂,充分反应后得到衍生产物的结晶,对结晶产物进行质谱分析,结果见图 1(a),与2-糠醛嗪的质谱图(图 1(b))对比可知,肼的糠醛衍生物和2-糠醛嗪具有相同分子离子峰和碎片峰。可见,过量糠醛使肼衍生转化为2-糠醛嗪,由此推测糠醛衍生反应按照式(2)进行。
|
图 1 质谱图对比分析:(a)肼的糠醛衍生物,(b)2-糠醛嗪 Fig. 1 Mass spectrometric analysis for (a) furfural derivatives of hydrazine, and (b) 2-furaldehyde azine |
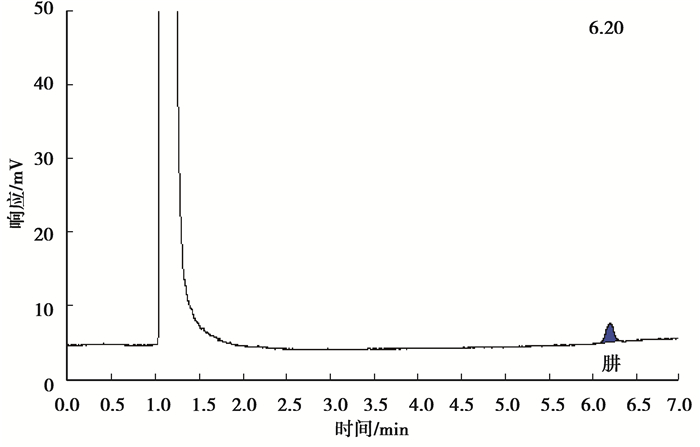
肼糠醛衍生物乙酸乙酯溶液的气相色谱分析结果如图 2所示,相同条件下纯溶剂乙酸乙酯的色谱分析结果见图 3。
|
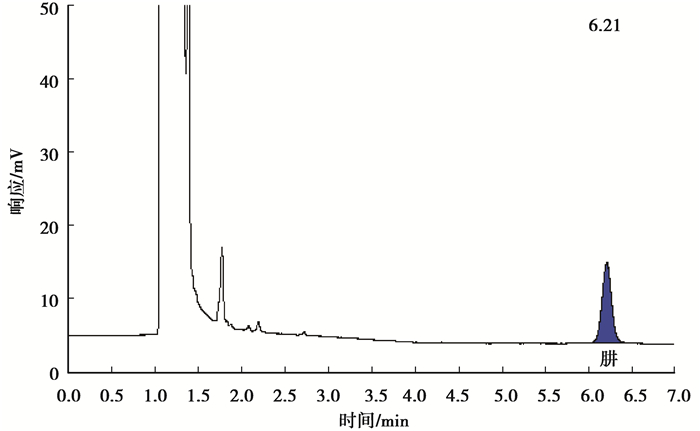
图 2 肼糠醛衍生物乙酸乙酯溶液的气相色谱分析 Fig. 2 Result of gas chromatographic analysis for furfural derivatives of hydrazine |
|
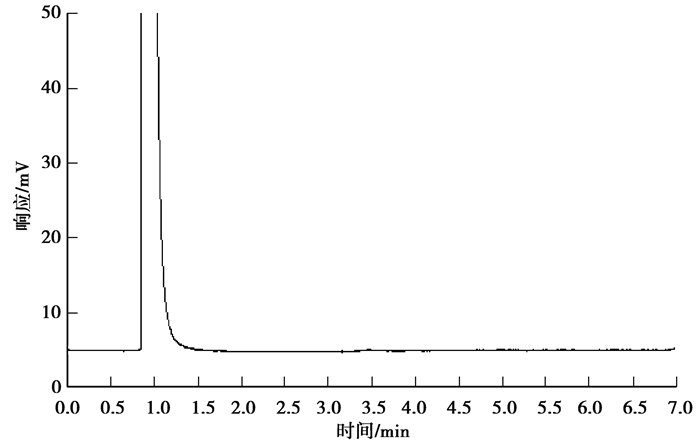
图 3 乙酸乙酯的气相色谱分析 Fig. 3 Gas chromatographic analysis for ethyl acetate |
图 3显示纯溶剂乙酸乙酯的保留时间为1.05 min,无其他杂质峰。图 2中出现了2个峰,一个在保留时间1.05 min处,属乙酸乙酯,另一个峰在保留时间6.20 min,从溶液的组成可以判断是肼的糠醛衍生物(即2-糠醛嗪)。由于肼与衍生产物2-糠醛嗪的化学计量比例为1:1,分析以保留时间定性,峰面积定量,所以可用肼衍生物对肼定量。
上述分析表明,肼的糠醛衍生按式(2)进行,得到淡黄色结晶,该结晶是单一的纯净衍生物2-糠醛嗪。但肼的糠醛衍生也可能按式(1)进行,停留在单分子糠醛衍生阶段,按式(1)生成的衍生产物在硫酸溶液中能形成可溶性的盐而不结晶。鉴于此,将糠醛过量的肼衍生溶液不经过晶体过滤和洗涤,直接用乙酸乙酯充分振摇萃取,将该萃取液与糠醛的乙酸乙酯溶液在相同条件下进行气相色谱对比分析,结果分别见图 4和图 5。
|
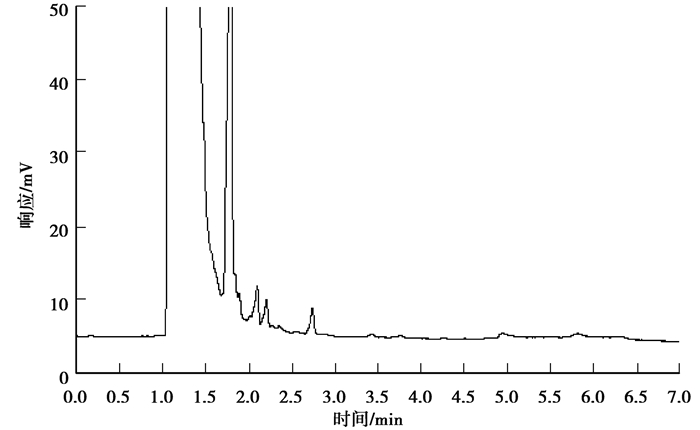
图 4 肼的糠醛衍生物乙酸乙酯萃取液的气相色谱分析 Fig. 4 Gas chromatographic analysis for ethyl acetate extraction solution of furfural derivatives of hydrazine |
|
图 5 糠醛乙酸乙酯溶液的气相色谱分析 Fig. 5 Gas chromatographic analysis for ethyl acetate solution of furfural |
图 4显示肼的糠醛衍生溶液除了溶剂和衍生物2-糠醛嗪的色谱峰以外,在保留时间1.6 min至3.0 min之间出现了系列色谱峰,与图 5糠醛的乙酸乙酯溶液的色谱分析结果比较,保留时间在1.6 min至3.0 min之间也出现了类似的系列色谱峰,可见该系列色谱峰是糠醛的色谱信息,没有肼与糠醛单分子加成产物存在。因为肼与糠醛的亲核加成反应活性高,易于进行,肼与单分子糠醛加成形成的产物仍存在可与醛基进行亲核反应的游离氨基,当糠醛过量时,这种单分子加成产物易于进一步与另一分子糠醛进行亲核加成反应,形成具有更长共轭体系结构、内能更低、稳定性更好的产物2-糠醛嗪。2-糠醛嗪分子的极性小,易溶于乙酸乙酯。所以,当过量糠醛存在时,没有肼的单分子糠醛衍生产物存在,肼全部衍生转化成了双分子糠醛衍生产物2-糠醛嗪。
上述实验结果表明,肼在过量糠醛存在时完全衍生转化为2-糠醛嗪,同时用乙酸乙酯可以有效地萃取糠醛衍生产物,在汽化室温度300 ℃、柱温210 ℃、氢火焰检测器温度350 ℃、载气流速2 mL/min、分流比10:1的色谱条件下可以得到定性定量分析肼(肼对应的糠醛衍生物)的对称色谱峰。
2.3 方法评价肼的糠醛衍生可以用气相色谱方法进行定性和定量,依据职业卫生标准制定指南,该方法用于肼的分析检测还需进一步从标准曲线的线性范围、检出限、标准偏差、精密度和准确性(回收率)等方面进行方法评价。
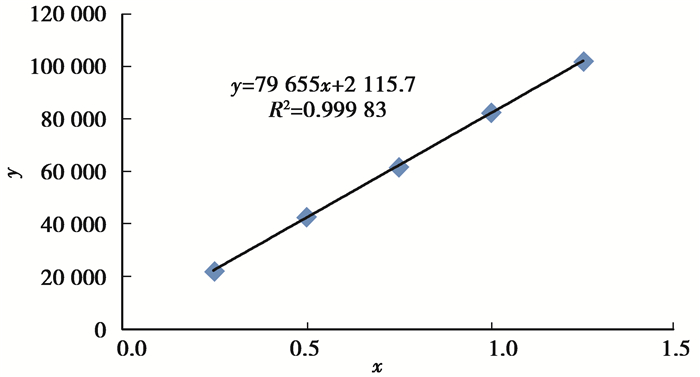
浓度为0.25,0.50,0.75,1.00,1.25 mg/L肼系列标准溶液经过衍生化、萃取后,在选定的最优分析条件下进行气相色谱分析,以峰面积为纵坐标y、质量浓度为横坐标x绘制的标准曲线如图 6所示。所得的线性回归方程为:y=796 55x+211 5.7,相关系数R2为0.999 8。结果表明,标准溶液在0.25~1.25 mg/L范围内,浓度与峰面积具有良好的线性关系,方法的适用范围较宽。
|
图 6 标准曲线 Fig. 6 Standard curve |
对0.10 mg/L低浓度的肼标准溶液,按照前述色谱分析的方法和条件平行测定11次,其标准偏差SD为0.002 5 mg/L,计算得到方法的检出限DL为0.007 8 mg/L,说明方法的灵敏度较高。
对方法线性范围内的浓度为0.25,0.50,1.00 mg/L的肼标准溶液进行衍生化、萃取及气相色谱分析,平行测定6次的平均值及相对标准偏差如表 1所示。低、中、高3个浓度的肼标准溶液检测结果相对标准偏差分别为1.90%、0.70%、0.29%,均小于5.0%,说明各浓度6次测定值之间的一致性较好,测定过程中的随机性误差小,方法的精密度好。
| 表 1 精密度实验结果 Table 1 Test results of precision |
用新配制的0.50 mg/L和1.25 mg/L肼质控样溶液各2.0 mL,进行空白加标回收实验,结果见表 2。两种浓度的加标回收率分别为98%和100%,表明该方法及分析条件对肼的分析检测的重现性好,具有较高的准确度。
| 表 2 加标回收实验结果 Table 2 Test results of recoveries |
上述结果表明,肼经过糠醛衍生在选定的色谱分析最优条件下,具有较宽的测定范围,方法的灵敏度、精密度和准确性较好,具有较高的精确度,是测定肼的较理想方法。
3 结论肼需要衍生转化后测定,但分析测定时定性定量依据来源于衍生转化产物2-糠醛嗪,而不是给定标准物质肼的直接色谱信息。先利用衍生转化原理,分析可能的转化途径,合成衍生转化的目标产物,用质谱定性结构,获得可靠的定性定量信息来源;再利用已定性结构的衍生产物与溶剂、衍生试剂等进行对比分析,确定理想的气相色谱分析条件;最后通过标准曲线法、平行测定法、加标回收法证明方法准确、灵敏度高、选择性好且色谱峰形对称。本研究不仅为不同实验室仪器及色谱柱条件下分析检测肼提供了一种快速、准确的条件探索程序,也为分析检测其它需衍生转化后测定的物质提供了可借鉴的方法。
| [1] |
Park S, An J, Potts J R, et al. Hydrazine-reduction of graphite- and graphene oxide[J]. Carbon, 2011, 49(9): 3019-3023. DOI:10.1016/j.carbon.2011.02.071 |
| [2] |
Zhang J, Cao X Y, Guo M, et al. Unique ni crystalline core/Ni phosphide amorphous shell heterostructured electrocatalyst for hydrazine oxidation reaction of fuel cells[J]. ACS Applied Materials & Interfaces, 2019, 11(21): 19048-19055. |
| [3] |
张琪, 高潮, 梁焕如, 等. 一种检测水合肼荧光探针的合成与应用[J]. 分析测试学报, 2017, 36(7): 937-940. ZHANG Qi, GAO Chao, LIANG Huanru, et al. Synthesis and application of a fluorescent probe for hydrazine determination[J]. Journal of Instrumental Analysis, 2017, 36(7): 937-940. (in Chinese) DOI:10.3969/j.issn.1004-4957.2017.07.019 |
| [4] |
郝帅, 蒋冬梅, 张晓腾, 等. 水合肼还原金属的研究进展[J]. 应用化学, 2018, 35(7): 756-766. HAO Shuai, JIANG Dongmei, ZHANG Xiaoteng, et al. Research progress on hydrazine hydrate reduction of metal[J]. Chinese Journal of Applied Chemistry, 2018, 35(7): 756-766. (in Chinese) |
| [5] |
Ganesan S, Vadivelu V M. Effect of external hydrazine addition on anammox reactor start-up time[J]. Chemosphere, 2019, 223: 668-674. DOI:10.1016/j.chemosphere.2019.02.104 |
| [6] |
Feng Z B, Li D G, Wang L, et al. In situ grown nanosheet Ni Zn alloy on Ni foam for high performance hydrazine electrooxidation[J]. Electrochimica Acta, 2019, 304: 275-281. DOI:10.1016/j.electacta.2019.03.017 |
| [7] |
Song Y Q, Chen G, Han X Y, et al. A highly sensitive near-infrared ratiometric fluorescent probe for imaging of mitochondrial hydrazine in cells and in mice models[J]. Sensors and Actuators B:Chemical, 2019, 286: 69-76. DOI:10.1016/j.snb.2019.01.116 |
| [8] |
姚旭, 张光友, 王煊军, 等. 环境中肼类燃料的分析方法研究进展[J]. 理化检验-化学分册, 2018, 54(1): 118-124. YAO Xu, ZHANG Guangyou, WANG Xuanjun, et al. Recent progress of analytical methods for hydrazine fuel in the environment[J]. Physical Testing and Chemical Analysis Part B(Chemical Analysis), 2018, 54(1): 118-124. (in Chinese) |
| [9] |
张勇, 刘劲风, 易润豪, 等. 一种黄酮类荧光探针的合成及用于肼的检测[J]. 分析化学, 2018, 46(4): 511-516, 630-632. ZHANG Yong, LIU Jinfeng, YI Runhao, et al. Synthesis and application of a flavone-based fluorescent probe for detection of hydrazine[J]. Chinese Journal of Analytical Chemistry, 2018, 46(4): 511-516, 630-632. (in Chinese) |
| [10] |
王真, 姜振邦, 李仁勇, 等. 离子色谱法测定空气中的氨、肼和乙醇胺[J]. 色谱, 2016, 34(10): 972-975. WANG Zhen, JIANG Zhenbang, LI Renyong, et al. Determination of ammonia, hydrazine and ethanol amine in air by ion chromatography[J]. Chinese Journal of Chromatography, 2016, 34(10): 972-975. (in Chinese) |
| [11] |
唐尧基, 樊静, 冯素玲. 环境水样中痕量肼的荧光分析[J]. 分析试验室, 2002, 22(1): 48-50. TANG Yaoji, FAN Jing, FENG Suling. Fluorescence analysis of trace hydrazine in environmental water samples[J]. Chinese Journal of Analysis Laboratory, 2002, 22(1): 48-50. (in Chinese) |
| [12] |
Nemakal M, Aralekallu S, Mohammed I, et al. Electropolymerized octabenzimidazole phthalocyanine as an amperometric sensor for hydrazine[J]. Journal of Electroanalytical Chemistry, 2019, 839: 238-246. DOI:10.1016/j.jelechem.2019.03.050 |
| [13] |
Shi X R, Yin C X, Zhang Y B, et al. A novel ratiometric and colorimetric fluorescent probe for hydrazine based on ring-opening reaction and its applications[J]. Sensors and Actuators B:Chemical, 2019, 285: 368-374. DOI:10.1016/j.snb.2019.01.075 |
| [14] |
Liu C, Liu K Y, Tian M G, et al. A ratiometric fluorescent probe for hydrazine detection with large fluorescence change ratio and its application for fluorescence imaging in living cells[J]. Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy, 2019, 212: 42-47. DOI:10.1016/j.saa.2018.12.026 |
| [15] |
Han X, Tian C, Yuan M S, et al. Colorimetric hydrazine detection and fluorescent hydrogen peroxide imaging by using a multifunctional chemical probe[J]. Analytica Chimica Acta, 2019, 1052: 137-144. DOI:10.1016/j.aca.2018.11.039 |
| [16] |
赵平, 梁蕊蕊, 高军龙, 等. 类伽腺苷中肼的测定[J]. 广州化工, 2017, 45(9): 146-148. ZHAO Ping, LIANG Ruirui, GAO Junlong, et al. Determination of hydrazine in regadenoson[J]. Guangzhou Chemical Industry, 2017, 45(9): 146-148. (in Chinese) DOI:10.3969/j.issn.1001-9677.2017.09.052 |
| [17] |
彭清涛, 张光友. 环境空气中肼的毛细管气相色谱法测定[J]. 现代科学仪器, 2012(5): 109-111. PENG Qingtao, ZHANG Guangyou. Determination of hydrazine in ambient air by capillary gas chromatography[J]. Modern Scientific Instruments, 2012(5): 109-111. (in Chinese) |
| [18] |
羡小超, 李立新, 赵朔, 等. 金属表面处理用混合硅烷体系中硅烷水解度的测定[J]. 重庆大学学报, 2017, 40(4): 70-77. XIAN Xiaochao, LI Lixin, ZHAO Shuo, et al. Measurement of hydrolysis degree of mixed silane system for surface treatment of mental[J]. Journal of Chongqing University, 2017, 40(4): 70-77. (in Chinese) |
| [19] |
赵艳梅, 张小林, 周尚, 等. 基于美拉德反应产物作为荧光和共振瑞利散射的传感平台快速检测阿斯巴甜[J]. 三峡生态环境监测, 2019, 4(2): 64-80. ZHAO Yanmei, ZHANG Xiaolin, ZHOU Shang, et al. Rapid detection of aspartame based on Maillard reaction product as a sensing platform for fluorescence and resonance Rayleigh scattering[J]. Ecology and Environmental Monitoring of Three Gorges, 2019, 4(2): 64-80. (in Chinese) |
 2019, Vol. 42
2019, Vol. 42


