随着工业的发展,电镀、皮革鞣制加工和纺织等行业的含铬废水排放入水体中,对水环境造成了巨大污染[1]。Cr(Ⅵ)的毒性高,可溶解并且迁移能力强,容易通过食物链积累于各种生物体内,危害人和动物的健康。目前,从水相中去除Cr(Ⅵ)的技术很多,例如化学沉淀法、离子交换法、生物吸附、膜分离法等等[2],这些方法处理过程较复杂并且成本较高。与之相比,吸附法由于效果好,操作简单,成本低,无二次污染而被广泛采用[3]。
生物炭作为一种新型吸附材料,是生物质在缺氧条件下热解转化而成的副产物[4],其性质稳定,具有发达的孔隙结构和丰富的表面官能团,在重金属污染修复方面受到了广泛关注[5, 6]。然而,生物质直接热解得到的炭质材料吸附效果有限,常常需要通过改性处理来提高对重金属的吸附效果[7]。目前,生物炭的改性方法包括酸改、碱改、金属盐浸渍改性等等[1]。在各种改性剂中,氯化锌对生物质原材料具有润胀、催化脱水和造孔的作用,对生物炭微孔的形成发挥着重要的作用,成为了环境领域的研究热点[4, 6]。此外,随着现代废物技术的发展,利用农业废弃物作为可持续替代资源制备炭质材料对实现废物资源化利用具有重要的意义[5]。基于此,笔者选用废弃物玉米秸秆作为原材料制备了生物炭,并用氯化锌进行改性,提高其对Cr(Ⅵ)的吸附性能,为含铬废水的处理以及获得高效廉价的生物炭吸附材料的应用提供支持。考察了改性剂比例、溶液pH、吸附温度、离子强度对吸附效果的影响,通过扫描电子显微镜(SEM)、傅里叶红外光谱分析仪(FTIR)、X射线衍射仪(XRD)对改性前后生物炭的理化性质进行了表征并进一步探究其吸附机理。
1 材料和方法 1.1 实验材料和样品材料:本实验选用的玉米秸秆购于重庆某农贸市场,对原材料进行预处理即筛选、破碎、阴干,粉碎粒径约为0.5~1.0 cm并在60 ℃条件下烘至24 h,密封保存备用。
药品:盐酸、氯化锌、重铬酸钾、硫酸、磷酸、二苯碳酰二肼,均为分析纯。
仪器:UV-1200紫外分光光度计(北京普析通用公司)、GF110-B热解炉(南京薄蕴通仪器科技有限公司)、SHZ-82恒温振荡器(国华企业有限公司)、PHB-5pH计(杭州奥利龙仪器有限公司)、AL104分析天平(梅特勒托利多仪器有限公司)、FEI Nova Nano扫描电镜(上海禹重实业有限公司)、傅里叶变换红外光谱仪(Thermo仪器公司)、D/Max 1200X射线衍射分析仪(Rigaku仪器公司)等。
1.2 生物炭的制备原炭的制备(biochar,BC):在无氧或缺氧状态下(充N2),热解一定质量的玉米秸秆。升温速率5 ℃/min,在500 ℃下保持2 h。热解完成后称重,研磨过40目筛后烘干密封储存备用,此时得到的产物为玉米秸秆原炭。
改性炭的制备(modified biochar,MBC):一定质量原炭与5%盐酸按照固液比为1:5混合搅拌4 h,用去离子水充分清洗后(洗后液pH为中性)置烘箱中干燥24 h。然后将生物炭按照固液比1 :5加入到ZnCl2溶液中(ZnCl2和BC质量比设定为0,0.15,0.30,0.45,0.60和0.75),搅拌4 h后烘干,然后进行二次热解,温度设定400 ℃,热解完成后碾磨过100目分样筛,此时得到的产物为改性生物炭,装入密封袋后存储备用。
1.3 材料表征用扫描电子显微镜(SEM)对BC和MBC的形貌结构进行了表征(FEI Nova 400 FEG-SEM)。用傅里叶变换红外光谱(FT-IR)分析了生物炭上的官能团(Nicolet Is 5)。用X射线衍射仪(D/max-2500,日本Rigaku)分析了生物炭的晶体结构。
1.4 Cr(Ⅵ)吸附单因素实验 1.4.1 改性剂比例的影响为了评价不同质量ZnCl2改性后的生物炭对Cr(Ⅵ)的吸附效果,分别称取不同质量改性剂改性后的生物炭0.1 g(ZnCl2和BC质量比设定为0,0.15,0.30,0.45,0.60和0.75),加入50 mL质量浓度为100 mg/L的Cr(Ⅵ)溶液,初始pH控制在2,恒温振荡,转速为120 r/min,温度设定为30 ℃。分别在震荡时间为0,0.25,0.5,1,2,3,4,6 h时,取样后用0.45 μm滤膜过滤,用紫外分光光度法测定Cr(Ⅵ)的质量浓度。
1.4.2 pH的影响Cr(Ⅵ)初始质量浓度为100 mg/L,溶液体积50 mL,用1 mol/L的NaOH和1 mol/L的HCl调节溶液的pH值分别为2,3,4,5,6,7,改性炭(ZnCl2和BC质量比为0.45 :1)投加量为0.05 g,温度设定30 ℃。转速为120 r/min恒温振荡24 h后,取样后用0.45 μm滤膜过滤,测定Cr(Ⅵ)的质量浓度。
1.4.3 吸附温度的影响Cr(Ⅵ)初始质量浓度为50,75,100 mg/L,溶液体积50 mL,pH调节为2,改性炭(ZnCl2和BC质量比为0.45 :1)投加量为0.05 g,恒温振荡,转速为120 r/min,温度设定为25,30,35,40 ℃。振荡24 h后,取样后用0.45 μm滤膜过滤,测定Cr(Ⅵ)的质量浓度。
1.4.4 离子强度的影响分别用0,0.001,0.005,0.01,0.05,0.1,0.5 mol/L的氯化钠溶液配置50 mL质量浓度为100 mg/L的Cr(Ⅵ)溶液,加入0.05 g的改性炭(ZnCl2和BC质量比为0.45 :1),恒温振荡,转速为120 r/min,温度设定为30 ℃。振荡24 h后,取样后用0.45 μm滤膜过滤,测定Cr(Ⅵ)的质量浓度。
1.5 动力学实验Cr(Ⅵ)初始质量浓度为100 mg/L,溶液体积50 mL,pH调节为2,改性炭(ZnCl2和BC质量比为0.45 :1)投加量为0.05 g,温度设定30 ℃,转速为120 r/min恒温振荡。分别在时间为0,0.25,0.5,1,2,3,4,8,12,24 h时,取样后用0.45 μm滤膜过滤,测定Cr(Ⅵ)的质量浓度。
1.6 吸附等温线的测定Cr(Ⅵ)初始质量浓度梯度25,50,75,100,200,300,400,500 mg/L,溶液体积50 mL,pH调节为2,改性炭(ZnCl2和BC质量比为0.45 :1)投加量为0.05 g,温度设定30 ℃。振荡24 h后,取样后用0.45 μm滤膜过滤,测定Cr(Ⅵ)的质量浓度。
2 结果与讨论 2.1 理化性质的表征 2.1.1 扫描电镜通过扫描电镜(图 1)比较了改性前后生物炭表面形态变化。可以看出未经过改性的生物炭表面相对平坦,孔隙疏松,几乎没有微孔。改性后的生物炭有更加清晰明显的孔道轮廓,孔径较小且排列致密,微孔结构明显,这可能是因为改性过程中反应强烈,改性剂对生物炭有造孔的作用[6]。良好的孔隙结构增大了生物炭的表面积和孔隙率,并且改性后生物炭表面更加粗糙从而为重金属提供了吸附位点,有利于Cr(Ⅵ)的吸附。此外,通过进一步放大改性生物炭的扫描电镜图可以看到,生物炭表面粗糙且均匀分布有许多白斑,可能是改性过程中在生物炭表面形成的锌颗粒物质,这与Li等[4]的研究结果一致。

|
图 1 生物炭扫描电镜图 Fig. 1 SEM photographs of biochar |
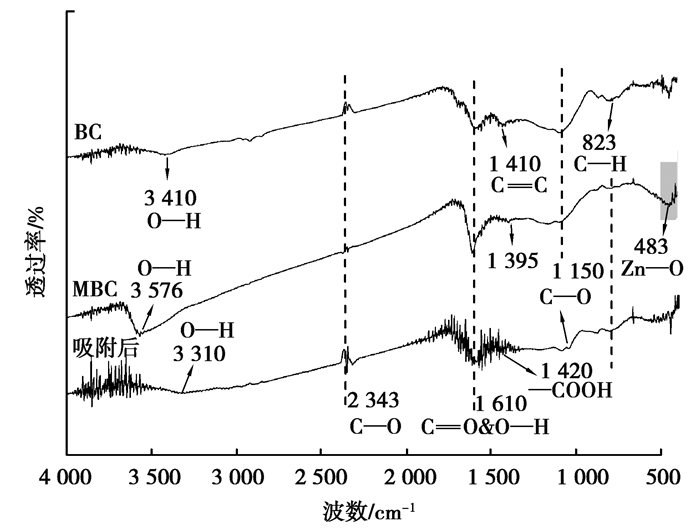
红外光谱(图 2)显示了改性前后及吸附后生物炭的表面官能团变化。在3 410 cm-1处的吸收峰代表羟基—OH官能团的伸缩振动[7],且在改性后峰移动到了3 576 cm-1。在1 610 cm-1处的吸收峰与—OH和羰基中C=O的伸缩振动有关[4, 8]。在1 150 cm-1处的吸收峰代表C—O的对称拉伸振动[9]。在823 cm-1处的吸收峰为脂族上C—H的面外弯曲振动[10]。在1 400 cm-1处的吸收峰与C=C的伸缩振动有关[11]。2 357 cm-1处的吸收峰代表CO2导致的C—O官能团的不对称伸缩振动,在原炭中显示为倒峰[2, 12]。
|
图 2 生物炭傅里叶红外光谱图 Fig. 2 Fourier transform infrared spectrum analysis of biochars |
氯化锌改性后羰基C=O的吸收峰增强,C—H吸收峰增强减弱,表明改性过程使生物炭的芳香化程度提高,增强了阳离子-π作用从而为生物炭表面提供了活性位点[13, 14]。在483 cm-1处的吸收峰与Zn—O的拉伸振动有关[15-17],并且由于—OH官能团的吸收峰增强,所以可以推测ZnCl2在改性过程中生成了Zn的氢氧化物,这与Xia等[6]的研究一致,且通过XRD图谱分析得到证实。
当生物炭与Cr(Ⅵ)发生吸附反应后,通过红外光谱可以看出部分官能团的特征峰发生了偏移。3 576,1 150,1 608,1 400 cm-1处吸收峰的波数发生移动,表明—OH、C—O、C=O、C=C和—COOH等官能团均与Cr(Ⅵ)的吸附过程有关。代表—OH、C—O和C=O基团的吸收峰在吸附后向低波数偏移,主要是因为在吸附过程中与Cr(Ⅵ)基团相结合,与Cr(Ⅵ)的氧化还原有关[18]。1 400 cm-1吸收峰发生偏移,归因于环状结构上的C=C或1 427 cm-1处的羧基基团与Cr(Ⅵ)的反应[19, 20]。Hsu等[21]采用X射线吸收光谱(XAS)结合红外研究黑炭对Cr(Ⅵ)的吸附指出:生物炭表面—OH和C—O基团参与Cr(Ⅵ)的吸附过程,能够为Cr(Ⅵ)的还原提供质子,并且吸附剂表面的羧基基团与还原产物Cr(Ⅲ)发生络合以及沉淀作用。Gan等[22]和Suksabye等[23]同样指出—OH和C=O对Cr(Ⅵ)氧化还原起重要作用。此外,文献[18]和[24]采用X射线光电子能谱(XPS)和红外结合说明了C=C在吸附过程中与Cr(Ⅵ)发生了氧化还原作用,而羧基基团—COOH主要是通过与Cr(Ⅵ)的还原产物Cr(Ⅲ)发生了结合。综上所述,氯化锌改性的生物炭吸附Cr(Ⅵ)包括直接吸附和还原2种途径,其中—OH、C—O、C=O、C=C和—COOH等官能团对Cr(Ⅵ)的吸附和还原起重要的作用。
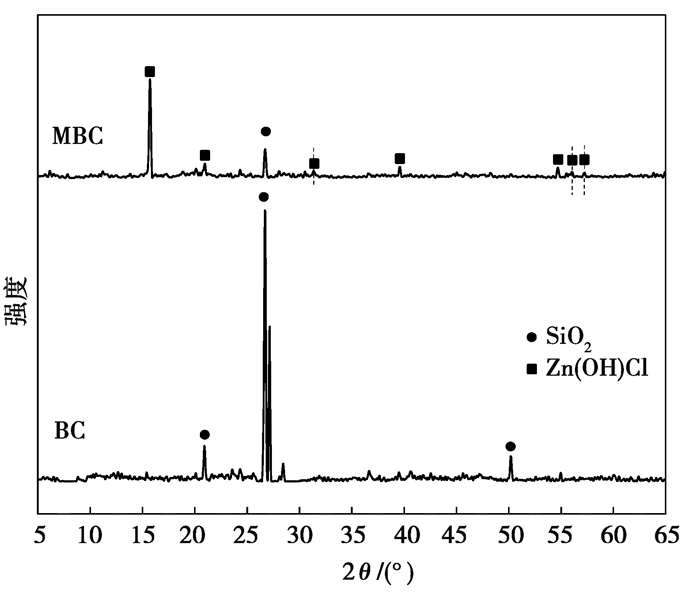
2.1.3 X衍射图(XRD)分析改性前后生物炭的XRD图谱如图 3所示。在原炭和改性炭都观察到对应的SiO2石英峰26.6°[25](PDF No.85-0930和PDF No.46-1045)。改性后生物炭出现了新的衍射峰2θ为15.7°,31.3°,39.5°,54.7°,56.0°和57.1°,与Zn(OH)Cl(PDF No.72-0525)相符,分别对应晶面(002)、(113)、(123)、(023)、(040)、(223),表明生物炭表面Zn主要以Zn—OH的形式存在[6]。
|
图 3 改性生物炭XRD谱图 Fig. 3 XRD spectrogram of modified biochar |
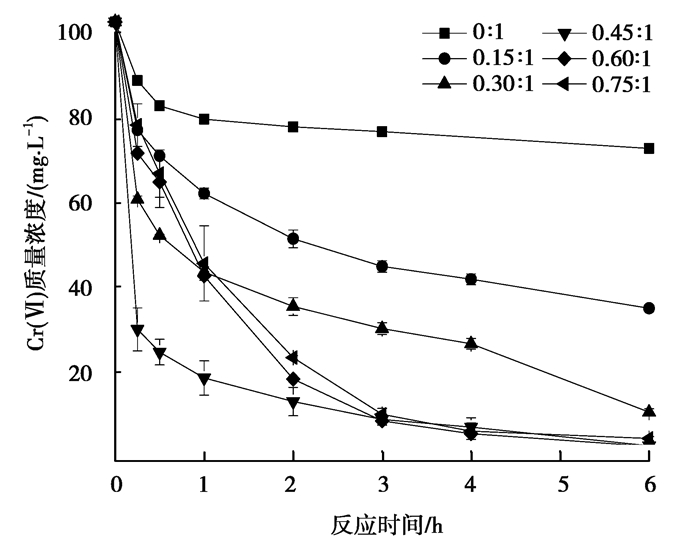
不同质量比(氯化锌/原炭)改性的玉米秸秆生物炭对Cr(Ⅵ)的吸附见图 4,可以明显看出,所有改性后的生物炭均比未改性的生物炭(即改性剂与原炭质量比为0 :1)对Cr(Ⅵ)的去除效率高,说明了经过氯化锌的改性提高了生物炭对Cr(Ⅵ)的吸附。改性剂与原炭质量比为0.45 :1时改性的生物炭的吸附效果最好,最快达到吸附平衡且6 h后去除率达到99.3%,比质量比为0 :1(25.6%),0.15 :1(65.9%),0.30 :1(89.8%),0.45 :1(99.3%),0.60 :1(97.7%),0.75 :1(95.91%)改性生物炭的去除率高出73.7%,33.4%,9.5%,1.6%,3.4%。虽然改性剂与原炭质量比为0.60 :1和0.75 :1时改性的生物炭在6 h去除率同样能达到95%以上,但其吸附速率远小于0.45 :1的改性生物炭。在吸附过程进行1 h时,质量比为0.45 :1(氯化锌/原炭)改性生物炭的去除率(81.5%)比质量比为0.60 :1(58.4%)和0.75 :1(55.6%)的高23.1%,25.9%。
|
图 4 改性剂比例对吸附Cr6+的影响 Fig. 4 Effect of modifier ratio on Cr6+ adsorption |
当改性剂与原炭的质量比从0:1增加到0.45 :1时,改性炭的Cr(Ⅵ)的去除率逐渐提高,可能的原因是改性过程中氯化锌的造孔作用促进生物炭微孔结构的形成[26],吸附位点增加。然而,当改性剂过量时,吸附变慢,较长时间达到平衡,可能是因为过量金属离子堵塞了形成的微孔[27],说明改性剂在一定的剂量范围内对改性效果是最好的。这与Yu等[16]的研究结果一致。
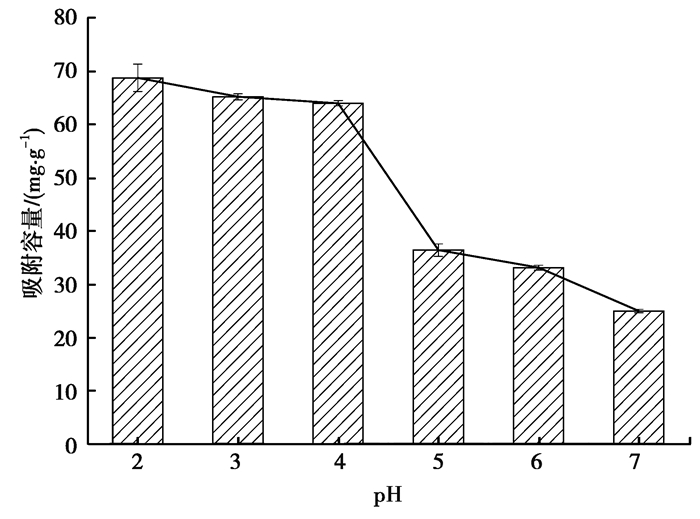
2.2.2 pH的影响溶液pH值是吸附过程中的重要参数之一,它会对吸附剂的表面电荷以及吸附质的形态产生影响[22]。图 5为pH值影响曲线。pH从2变化到7时,吸附容量从68.7 mg/g下降到24.9 mg/g,说明随pH值的上升,改性生物炭对Cr(Ⅵ)的吸附下降。主要原因如下:1)在Cr(Ⅵ)溶液中,不同的pH条件下Cr的存在形式不同,它主要以H2CrO4(pH<1.0)、HCrO4-(1.0<pH<6.0)和CrO42-(pH>6)的形式存在。OH-浓度越高,会与铬负离子竞争吸附位点从而导致吸附能力下降[8]。2)低pH下,生物炭表面正电荷变多,有利于生物炭和铬负离子之间发生静电吸附作用。而pH上升会导致生物炭表面官能团带负电性,从而与HCrO4-和CrO42-发生排斥作用[18, 28]。
|
图 5 pH对吸附Cr6+的影响 Fig. 5 Effect of pH on Cr6+ adsorption |
表 1显示了不同温度下改性生物炭的饱和吸附容量以及相关热力学参数值。从表 1中可以看到,吸附容量随Cr(Ⅵ)初始质量浓度的增加而提高。这是因为溶液浓度越高,单位质量生物炭所能接触到的吸附质的量增加,吸附位点被充分利用直至生物炭吸附达到饱和。此外,温度越高,吸附容量越大,是因为温度上升,Cr6+的扩散速度加快,离子间碰撞几率增加,能量越高[29]。
| 表 1 改性生物炭吸附Cr6+的热力学参数 Table 1 Adsorption thermodynamic parameters of Cr6+ adsorption by modified biochar |
热力学分别在288.15,293.15,298.15,303.15 K条件下进行研究。吸附过程用3个热力学参数,自由能变化(ΔG,kJ/mol)、焓变化(ΔH、kJ/mol)、熵变化(ΔS、kJ/kmol)来描述,结果见表 1。ΔG<0,ΔH>0表明吸附过程是自发的吸热反应[30]。随着吸附反应温度的升高,ΔG逐渐变小。表明吸附过程中温度的升高有利于反应的进行。此外,ΔS的正值表明了吸附过程在固溶体界面上的随机性增大[10]。从表 1中还可以看出,质量浓度越低ΔG越小,表明Cr(Ⅵ)的浓度越低,反应越剧烈,能够快速达到平衡。
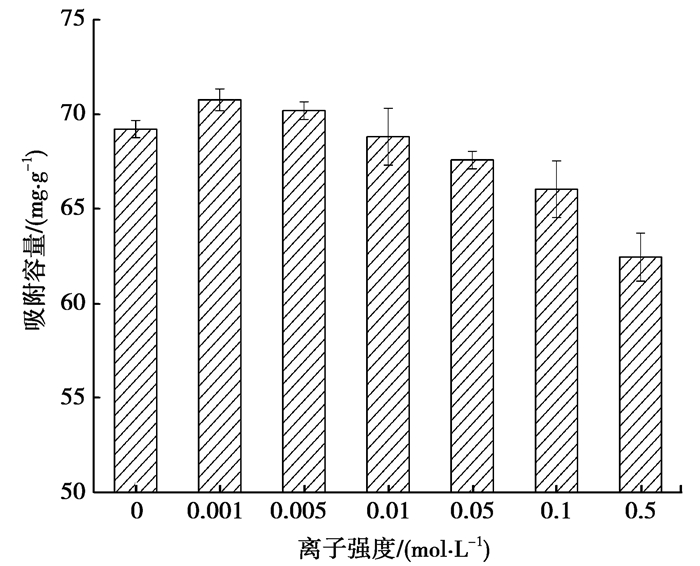
2.2.4 离子强度的影响废水中一般含有大量的无机盐[15],所以离子强度也是影响生物炭吸附Cr(Ⅵ)的重要因素。图 6显示了离子强度对吸附的影响。在低浓度(0.001~0.005 mol/L)NaCl溶液中,共存离子几乎不影响Cr(Ⅵ)的吸附。然而在较高浓度(0.01~0.05 mol/L)情况下,吸附容量从70.7 mg/g降低至62.4 mg/g。原因是杂质离子会竞争生物炭上的吸附位点,对生物炭表面电荷产生影响[29]。此外,Cr6+离子的活度系数会随之降低,从而减少与吸附剂之间的碰撞,导致吸附容量的降低[22]。
|
图 6 离子强度对吸附Cr6+的影响 Fig. 6 Effect of Ionic strength on Cr6+ adsorption |
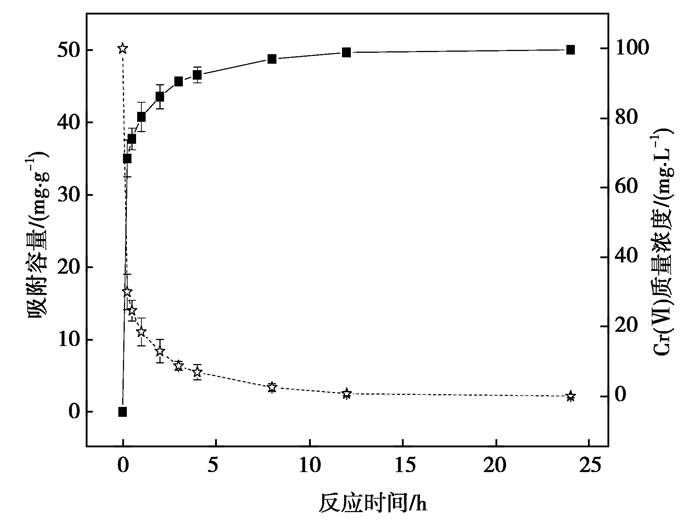
不同接触时间的吸附过程如图 7所示。可以看出,吸附速率在前0.5 h较高,吸附容量为37.7 mg/g,是饱和时吸附容量(50.1 mg/g)的75.4%。6 h后吸附达到平衡,去除率为99.3%,吸附达到饱和。在吸附开始的初期,由于生物炭表面丰富的吸附位点以及溶液与生物炭之间的浓度差促使金属离子快速迁移至生物炭表面[1],吸附速率最大。随后吸附速率减缓,可能与吸附位点的减少、浓度梯度减小以及通过微孔通道的运动学抑制有关[16]。因此,改性生物炭对Cr(Ⅵ)的吸附是复杂的,与表面吸附和颗粒内扩散有关[31-33]。
|
图 7 Cr(Ⅵ)吸附量与吸附时间的关系 Fig. 7 The relationship between Cr(Ⅵ) adsorption capacity and adsorption time |
吸附过程用准一级和准二级动力学拟合。
1) 准一级:
| $ \log \left( {{q_{\rm{e}}} - {q_t}} \right) = \log {q_{\rm{e}}} - \frac{{{k_1}t}}{{2.030}}。$ |
2) 准二级:
| $ \frac{t}{{{q_t}}} = \frac{t}{{{q_{\rm{e}}}}} + \frac{1}{{{k_2}q_{\rm{e}}^2}}, $ |
式中:qt和qe分别为t(min)时刻的吸附容量和平衡时的吸附容量,mg/g;k1是准一级动力学模型吸附速率,min-1;k2是准二级动力学模型吸附速率,g/(mg·min)。
从表 2中可以看出,准二级模型相关系数R2(0.998)要高于准一级,说明吸附过程更加符合准二级动力学,是物理化学[34]的复合吸附,化学吸附是控制速率的主要步骤。准二级动力学能够准确描述吸附反应的全过程,这与Shang等[35]的研究类似,Shang等[35]的研究表明改性生物炭去除铬符合了准二级模型,其反应过程包含了还原、络合、离子交换等多种机制。
| 表 2 改性生物炭吸附Cr(Ⅵ)的动力学参数 Table 2 Kinetic parameters of adsorption of Cr(Ⅵ) onto modified biochar |
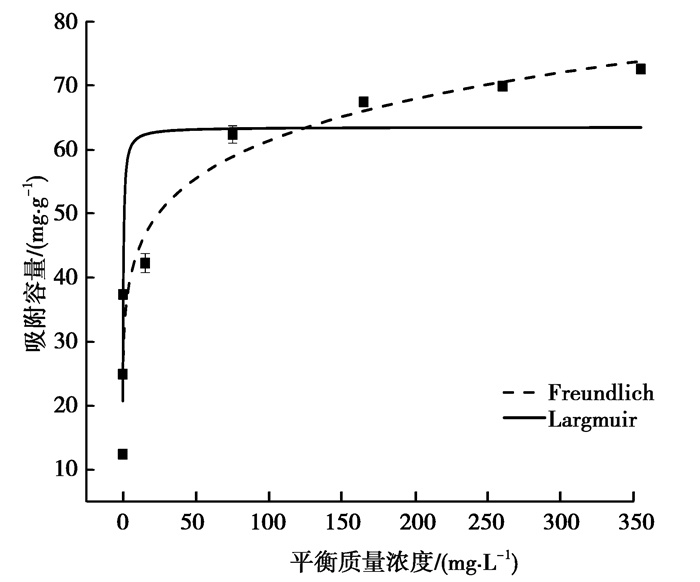
生物炭的吸附等温线如图 8所示。在溶液中吸附重金属的过程通常用Langmuir和Freundlich模型来拟合。Langmuir模型假设吸附剂上发生的是单分子层吸附,吸附剂表面性质均一。而Freundlich模型是一个不均匀表面的经验吸附等温式[36]。
|
图 8 生物炭的吸附等温线 Fig. 8 Adsorption isotherms of the biochars |
Langmuir模型:
| $ \frac{1}{{{Q_{\rm{e}}}}} = \frac{1}{{{Q_{\rm{m}}}{K_{\rm{L}}}{C_{\rm{e}}}}} + \frac{1}{{{Q_{\rm{m}}}}}。$ |
Freundlich模型:
| $ \ln {Q_{\rm{e}}} = \ln {K_{\rm{F}}} + \frac{1}{n}\ln {C_{\rm{e}}}, $ |
式中:Qm为饱和吸附容量,mg/g;Qe是平衡时吸附容量;Ce是平衡时溶液中Cr(Ⅵ)质量浓度,mg/L;KL是与吸附能力相关的吸附Langmuir常数,L/mg;KF和1/n分别代表亲和系数和吸附强度的Freundlich常数。
计算出的2种等温线模型相关参数结果见表 3,与Freundlich模型相比,Langmuir模型具有较高的相关系数R2(0.998),较好地拟合了实验数据。因此,基于langmuir模型,改性炭对Cr(Ⅵ)的最大吸附容量为72.46 mg/g,吸附效果较好,可有效地应用于废水中去除Cr(Ⅵ)。
| 表 3 改性生物炭等温吸附模型参数 Table 3 Parameters of modified biochar isothermal adsorption model |
利用氯化锌对玉米秸秆生物炭进行改性实现了对Cr(Ⅵ)的高效去除,通过一系列吸附试验和相关表征技术(SEM、FTIR、XRD)得到以下结论:
1) 通过扫描电镜可以看出氯化锌改性的玉米秸秆生物炭微孔结构明显,生物炭表面粗糙且均匀分布有白色颗粒,XRD和FTIR分析表明改性炭的芳香化程度提高,吸附位点增加,表面负载的白色颗粒是含锌的氢氧化物颗粒。此外,FTIR图谱显示了生物炭表面的—OH、C=C、C=O及C—OH等官能团对Cr(Ⅵ)的吸附和还原起重要的作用。
2) 当氯化锌与原炭的质量比在0.45 :1时进行改性时,改性炭的去除率能够达到99.3%,比质量比为0 :1,0.15 :1,0.30 :1,0.45 :1,0.60 :1,0.75 :1改性的生物炭的去除率高出73.7%,33.4%,9.5%,1.6%,3.4%。当pH从2.0上升到7.0,改性生物炭对Cr(Ⅵ)的吸附容量降低。当溶液离子强度增加时,吸附过程受到了轻微抑制。热力学研究说明该吸附是自发的吸热过程。
3) 改性生物炭对Cr(Ⅵ)的吸附拟合了准二级动力学和Langmuir模型,表明了吸附过程是物理化学的复合吸附,基于Langmuir模型最大饱和吸附容量能够达到72.46 mg/g。
通过氯化锌改性制备的这种低成本生物炭吸附剂,能够高效去除废水中的Cr(Ⅵ),对实现废物资源化利用具有重要的意义,并且具有较大的环境修复应用潜力。
| [1] |
Wang S S, Gao B, Zimmerman A R, et al. Removal of arsenic by magnetic biochar prepared from pinewood and natural hematite[J]. Bioresource Technology, 2015, 175: 391-395. DOI:10.1016/j.biortech.2014.10.104 |
| [2] |
Kazarian S G, Vincent M F, Bright F V, et al. Specific intermolecular interaction of carbon dioxide with polymers[J]. Journal of the American Chemical Society, 1996, 118(7): 1729-1736. DOI:10.1021/ja950416q |
| [3] |
Vo A T, Nguyen V P, Ouakouak A, et al. Efficient removal of Cr(Ⅵ) from water by biochar and activated carbon prepared through hydrothermal carbonization and pyrolysis: adsorption-coupled reduction mechanism[J]. Water, 2019, 11(6): 1164. DOI:10.3390/w11061164 |
| [4] |
Li C J, Zhang L, Gao Y, et al. Facile synthesis of nano ZnO/ZnS modified biochar by directly pyrolyzing of zinc contaminated corn stover for Pb(Ⅱ), Cu(Ⅱ) and Cr(Ⅵ) removals[J]. Waste Management, 2018, 79: 625-637. DOI:10.1016/j.wasman.2018.08.035 |
| [5] |
Dubey S, Gopal K. Adsorption of chromium(Ⅵ) on low cost adsorbents derived from agricultural waste material: a comparative study[J]. Journal of Hazardous Materials, 2007, 145(3): 465-470. DOI:10.1016/j.jhazmat.2006.11.041 |
| [6] |
Xia D, Tan F, Zhang C P, et al. ZnCl2-activated biochar from biogas residue facilitates aqueous As(Ⅲ) removal[J]. Applied Surface Science, 2016, 377: 361-369. DOI:10.1016/j.apsusc.2016.03.109 |
| [7] |
Zhai S M, Li M, Wang D, et al. In situ loading metal oxide particles on bio-chars: reusable materials for efficient removal of methylene blue from wastewater[J]. Journal of Cleaner Production, 2019, 220: 460-474. DOI:10.1016/j.jclepro.2019.02.152 |
| [8] |
Xiao F F, Cheng J H, Cao W, et al. Removal of heavy metals from aqueous solution using chitosan-combined magnetic biochars[J]. Journal of Colloid and Interface Science, 2019, 540: 579-584. DOI:10.1016/j.jcis.2019.01.068 |
| [9] |
Wu J, Zheng H, Zhang F, et al. Iron-carbon composite from carbonization of iron-crosslinked sodium alginate for Cr(Ⅵ) removal[J]. Chemical Engineering Journal, 2019, 362: 21-29. DOI:10.1016/j.cej.2019.01.009 |
| [10] |
Wang P, Tang L, Wei X, et al. Synthesis and application of iron and zinc doped biochar for removal of p-nitrophenol in wastewater and assessment of the influence of co-existed Pb(Ⅱ)[J]. Applied Surface Science, 2017, 392: 391-401. DOI:10.1016/j.apsusc.2016.09.052 |
| [11] |
Son E B, Poo K M, Chang J S, et al. Heavy metal removal from aqueous solutions using engineered magnetic biochars derived from waste marine macro-algal biomass[J]. Science of the Total Environment, 2018, 615: 161-168. DOI:10.1016/j.scitotenv.2017.09.171 |
| [12] |
Kumar S, Rajawat S, Purohit R, et al. Optical properties of BCNO nano phosphor synthesized using novel green technology[J]. Materials Research Express, 2019, 6(10): 105027. DOI:10.1088/2053-1591/ab3741 |
| [13] |
朱银涛, 李业东, 王明玉, 等. 玉米秸秆碱化处理制备的生物炭吸附锌的特性研究[J]. 农业环境科学学报, 2018, 37(1): 179-185. ZHU Yintao, LI Yedong, WANG Mingyu, et al. Adsorption characteristics of biochar prepared by corn stalk alkalization on zinc[J]. Journal of Agro-Environment Science, 2018, 37(1): 179-185. (in Chinese) |
| [14] |
刘雪梅, 赵蓓. 氯化锌造孔甘蔗渣制备的生物炭对废水中Cr(Ⅵ)的吸附研究[J]. 应用化工, 2019, 48(6): 1354-1358, 1362. LIU Xuemei, ZHAO Bei. Adsorption of Cr(Ⅵ) in wastewater by biochar prepared from zinc chloride modified bagasse[J]. Applied Chemical Industry, 2019, 48(6): 1354-1358, 1362. (in Chinese) |
| [15] |
Hu Y, Zhu Y, Zhang Y, et al. An efficient adsorbent: simultaneous activated and magnetic ZnO doped biochar derived from camphor leaves for ciprofloxacin adsorption[J]. Bioresource Technology, 2019, 288: 121511. DOI:10.1016/j.biortech.2019.121511 |
| [16] |
Yu J D, Jiang C Y, Guan Q Q, et al. Enhanced removal of Cr(Ⅵ) from aqueous solution by supported ZnO nanoparticles on biochar derived from waste water hyacinth[J]. Chemosphere, 2018, 195: 632-640. DOI:10.1016/j.chemosphere.2017.12.128 |
| [17] |
武志富, 李素娟. 氢氧化锌和氧化锌的红外光谱特征[J]. 光谱实验室, 2012, 29(4): 2172-2175. WU Zhifu, LI Sujuan. Infrared spectra characteristics of zinc hydroxide and zinc oxide[J]. Chinese Journal of Spectroscopy Laboratory, 2012, 29(4): 2172-2175. (in Chinese) |
| [18] |
丁文川, 田秀美, 王定勇, 等. 腐殖酸对生物炭去除水中Cr(Ⅵ)的影响机制研究[J]. 环境科学, 2012, 33(11): 3847-3853. DING Wenchuan, TIAN Xiumei, WANG Dingyong, et al. Mechanism of Cr(Ⅵ) removal from aqueous solution using biochar promoted by humic acid[J]. Environmental Science, 2012, 33(11): 3847-3853. (in Chinese) |
| [19] |
Zhang S, Lyu H H, Tang J C, et al. A novel biochar supported CMC stabilized nano zero-valent iron composite for hexavalent chromium removal from water[J]. Chemosphere, 2019, 217: 686-694. DOI:10.1016/j.chemosphere.2018.11.040 |
| [20] |
Wan Z H, Cho D W, Tsang D C W, et al. Concurrent adsorption and micro-electrolysis of Cr(Ⅵ) by nanoscale zerovalent iron/biochar/Ca-alginate composite[J]. Environmental Pollution, 2019, 247: 410-420. DOI:10.1016/j.envpol.2019.01.047 |
| [21] |
Hsu N H, Wang S L, Lin Y C, et al. Reduction of Cr(Ⅵ) by crop-residue-derived black carbon[J]. Environmental Science & Technology, 2009, 43(23): 8801-8806. |
| [22] |
Gan C, Liu Y G, Tan X F, et al. Effect of porous zinc-biochar nanocomposites on Cr(Ⅵ) adsorption from aqueous solution[J]. RSC Advances, 2015, 5(44): 35107-35115. DOI:10.1039/C5RA04416B |
| [23] |
Suksabye P, Nakajima A, Thiravetyan P, et al. Mechanism of Cr(Ⅵ) adsorption by coir pith studied by ESR and adsorption kinetic[J]. Journal of Hazardous Materials, 2009, 161(2/3): 1103-1108. |
| [24] |
Zhu Y E, Li H, Zhang G X, et al. Removal of hexavalent chromium from aqueous solution by different surface-modified biochars: Acid washing, nanoscale zero-valent iron and ferric iron loading[J]. Bioresource Technology, 2018, 261: 142-150. DOI:10.1016/j.biortech.2018.04.004 |
| [25] |
Wang Z W, Yang X, Qin T T, et al. Efficient removal of oxytetracycline from aqueous solution by a novel magnetic clay-biochar composite using natural attapulgite and cauliflower leaves[J]. Environmental Science and Pollution Research, 2019, 26(8): 7463-7475. DOI:10.1007/s11356-019-04172-8 |
| [26] |
张志柏, 朱义年, 刘辉利, 等. 氯化锌活化法制备甘蔗渣活性炭吸附剂[J]. 化工环保, 2009, 29(1): 62-66. ZHANG Zhibai, ZHU Yinian, LIU Huili, et al. Preparation of activated carbon from bagasse by activation with zinc chloride[J]. Environmental Protection of Chemical Industry, 2009, 29(1): 62-66. (in Chinese) |
| [27] |
高银东, 王淑花, 于晓颖, 等. 氯化锌活化棉纤维制备成型活性炭工艺研究[J]. 应用化工, 2019, 48(4): 853-856. GAO Yindong, WANG Shuhua, YU Xiaoying, et al. Preparation of activated carbon from cotton fiber by zinc chloride[J]. Applied Chemical Industry, 2019, 48(4): 853-856. (in Chinese) |
| [28] |
Zhu S S, Huang X C, Wang D W, et al. Enhanced hexavalent chromium removal performance and stabilization by magnetic iron nanoparticles assisted biochar in aqueous solution: Mechanisms and application potential[J]. Chemosphere, 2018, 207: 50-59. DOI:10.1016/j.chemosphere.2018.05.046 |
| [29] |
唐登勇, 胡洁丽, 胥瑞晨, 等. 芦苇生物炭对水中铅的吸附特性[J]. 环境化学, 2017, 36(9): 1987-1996. TANG Dengyong, HU Jieli, XU Ruichen, et al. Adsorption of lead onto reed biochar in aqueous solution[J]. Environmental Chemistry, 2017, 36(9): 1987-1996. (in Chinese) |
| [30] |
Yousaf B, Liu G J, Abbas Q, et al. Enhanced removal of hexavalent chromium from aqueous media using a highly stable and magnetically separable rosin-biochar-coated TiO2@C nanocomposite[J]. RSC Advances, 2018, 8(46): 25983-25996. DOI:10.1039/C8RA02860E |
| [31] |
Zhang W Y, Qian L B, Ouyang D, et al. Effective removal of Cr(Ⅵ) by attapulgite-supported nanoscale zero-valent iron from aqueous solution: Enhanced adsorption and crystallization[J]. Chemosphere, 2019, 221: 683-692. DOI:10.1016/j.chemosphere.2019.01.070 |
| [32] |
Zhang X, Lv L, Qin Y Z, et al. Removal of aqueous Cr(Ⅵ) by a magnetic biochar derived from Melia azedarach wood[J]. Bioresource Technology, 2018, 256: 1-10. DOI:10.1016/j.biortech.2018.01.145 |
| [33] |
Zhong D L, Zhang Y R, Wang L L, et al. Mechanistic insights into adsorption and reduction of hexavalent chromium from water using magnetic biochar composite: Key roles of Fe3O4 and persistent free radicals[J]. Environmental Pollution, 2018, 243: 1302-1309. DOI:10.1016/j.envpol.2018.08.093 |
| [34] |
李佳霜, 冒国龙, 赵松炎, 等. 改性生物炭对Sb(Ⅲ)的吸附行为及机理[J]. 化工环保, 2018, 38(5): 546-551. LI Jiashuang, MAO Guolong, ZHAO Songyan, et al. Adsorption behavior and mechanism of modified biochar to Sb(Ⅲ)[J]. Environmental Protection of Chemical Industry, 2018, 38(5): 546-551. (in Chinese) |
| [35] |
Shang J G, Zong M Z, Yu Y, et al. Removal of chromium (Ⅵ) from water using nanoscale zerovalent iron particles supported on herb-residue biochar[J]. Journal of Environmental Management, 2017, 197: 331-337. DOI:10.1016/j.jenvman.2017.03.085 |
| [36] |
Lonappan L, Rouissi T, Kaur Brar S, et al. An insight into the adsorption of diclofenac on different biochars: mechanisms, surface chemistry, and thermodynamics[J]. Bioresource Technology, 2018, 249: 386-394. DOI:10.1016/j.biortech.2017.10.039 |
 2020, Vol. 43
2020, Vol. 43

