光催化技术通过利用太阳光将有毒有害的污染物直接分解成无毒或低毒的小分子,展现出无毒(或低毒)和广泛使用性,得到了高度重视[1-2]。光催化技术中,开发高效稳定的光催化剂是核心问题,已研制出的光催化剂主要有TiO2、ZnO、ZnS、CdS等多元化合物[3-4]。半导体光催化降解有机污染物的研究取得了长足的进步,但由于多元化合物自身的制备过程烦琐,成本较高,其实际应用受到极大的限制。近年来,以红磷(RP)为首的单质光催化剂引起了广泛关注,这类半导体的光催化活性并不亚于多元化合物,同时避免了上述缺点。RP具有带隙窄(1.8 eV)、可见光(400~700 nm)吸收率较强、在常温常压条件下稳定性较好、无毒无气味等特点,在利用可见光光解水、提高太阳能的转化利用效率方面具有十分巨大的应用前景[5-7]。然而,商业红磷(C-RP)本身也存在着很大的局限性[8-10]:1)块状结构占主导地位,从而导致表面活性物质的种类少;晶体结构不同使光生载流子的分离和迁移能力有差异。2)量子效率偏低。因带隙仅为1.8 eV,光生载流子易复合,从而减弱了RP的光催化活性。3)比表面积小。光催化活性位点少,很难吸附污染物和捕获太阳光子。
通过控制不同的反应条件来提高C-RP的光催化活性是最简单的一种方法。如Qi等[5]以C-RP为前驱体,通过水热处理和管式炉煅烧后获得的红磷的尺寸远小于C-RP,且孔洞结构丰富,比表面积大,从而有效增大了RP的反应活性位点,通过对亚甲基蓝的吸附和光降解性能评价发现处理后的RP具有极强的吸附性能和光催化降解能力。Ren等[11]用水热法结合超声法,制备了纳米尺寸的红磷光催化剂,实验条件考察结果发现水热12 h,超声2 h得到的RP对罗丹明B(RhB)和甲苯酚具有最佳的光降解性),机理探究发现光催化性能增强的原因是纳米尺寸的红磷比表面积增大导致其活性位点增多,光生载流子传到光催化剂表面的时间短,从而增强了光催化活性。Ansari等[12]采用机械球磨方法处理C-RP,实验发现研磨36 h所得的RP具有最好的光催化性能,其反应速率常数远大于C-RP。表征结果发现球磨后RP粒径明显变小,且具有一定的结晶性。寻找简单、可控、经济的方法提高C-RP光催化活性是发展的趋势。基于上述分析,笔者以C-RP为原料,以NaOH溶液为调节剂,采用水热法处理C-RP获得HRP-pHx(x=5, 7, 9)光催化剂。采用XRD、粒度分析仪等系列方法表征其晶型、晶粒、结构等。以RhB为模型污染物,研究HRP-pHx光催化剂的光降解能力,并探究其机理。
1 实验方法 1.1 HRP-pHx的制备以C-RP为原料、NaOH溶液为调节剂,采用水热法制备HRP-pHx,具体制备过程如下:将0.6 g的C-RP于20 mL蒸馏水中分散,磁力搅拌下用NaOH溶液调pH(5, 7, 9)后装进水热反应釜里,在200 ℃恒温反应12 h。反应结束后离心,洗涤,于80 ℃干燥4 h,获得目标产物(标记为HRP-pH5、HRP-pH7、HRP-pH9)。未调pH的RP用相同的方法进行处理,产物标记为HRP。
1.2 HRP-pHx表征用XRD(D8 Advance,德国BRUKER)表征催化剂的晶体结构和物相组成;应用粒度分析仪(ZS90, 英国Malvern)测定催化剂的粒径;用场发射扫描电子显微镜(FESEM JSM-7610F,日本捷欧路)分析催化剂表面的微观形貌;利用比表面积与孔隙度分析仪(BET ASAP 2460,美国麦克)测试催化剂的比表面积和孔径分布;用电化学工作站(CHI 660D,上海辰华)选择三电极分析样品的电化学性质,制备的催化剂为工作电极,Pt电极为对电极,饱和甘汞电极为参比电极,pH 4.8、0.5 mol/L Na2SO4水溶液为电解液。
1.3 HRP-pHx催化剂光降解性能评价以10 mg·L-1 RhB溶液为降解对象,500 W氙灯为光源,将50 mg RP-pHx光催化剂分散于200 mL RhB溶液中。首先在暗环境下吸附脱附平衡,然后在可见光照射下反应一定时间,离心得上清液,取4 mL于比色皿中,用紫外可见分光度计在554 nm(RhB的最大吸收波长)测定吸光度。按以下公式计算降解率η,实验平行测定3次,结果取平均值。
| $ \eta = \frac{{{C_0} - {C_i}}}{{{C_0}}} \times 100\% 。$ | (1) |
式中:C0为RhB的初始浓度,Ct为光照时间t后RhB的浓度。
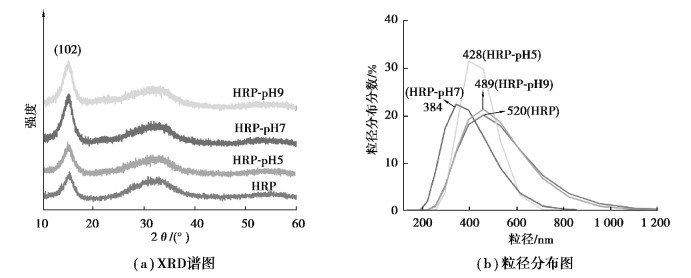
2 结果和讨论 2.1 表征HRP和HRP-pH7的XRD谱图见图 1(a)。15.1°处的衍射角对应的是RP的(102)衍射晶面,与文献报道一致[13],该表征证实在HRP和HRP-pH7样品中仅有RP,没有产生新的峰,表明在水热处理过程中红磷没有明显的变化,也没有引入其他杂质。但是可以看出随着pH增大峰强度和宽度先增大后减小,当pH为7时,所获得的催化剂(HRP-pH7)的峰最强最宽。这说明pH为7的环境下所得的RP结晶性更好,颗粒更小。粒径分析结果如图 1(b)所示,可以看出随着pH增大,催化剂的粒径先减小后增大,其中RP-pH7的粒径最小,说明中性环境所制备的RP具有更大的比较面积和更小的粒径,利于提高空穴与光生电子的扩散速率,能够大大提高光催化剂的催化活性[14]。
|
图 1 HRP、HRP-pH5、HRP-pH7和HRP-pH9样品的XRD图和粒径分布图 Fig. 1 XRD patterns and particle size distribution of HRP, HRP-pH5, HRP-pH7 and HRP-pH9 |
图 2为HRP和HRP-pH7催化剂的SEM图,不调pH水热处理后催化剂表面比较光滑,孔洞分布较为均一(图 2(a)和(b))。经调整pH后获得的催化剂表面粗糙,产生无序、不规则的小凹陷(图 2(c)),孔洞数目增多,大小不一,分布更为规整(图 2(d)),利于催化剂吸附富集定位光降解污染物。BET的结果发现HRP的孔径为37.0 nm,比表面为13.6 m2/g;HRP-pH7的孔径为44.2 nm,比表面积为14.9 m2/g,调整pH为7所获得的催化剂的孔径和比表面积均增大。该结果说明调整pH为7所获的催化剂更利于吸附污染物和传输电子。在纳米材料形成和生长过程中溶液的环境起了关键的作用,以上表征结果表明在其它条件相同的情况下,红磷在纯水中结晶度低,表面较为平整光滑,说明红磷在纯水中各个方向上的生长速率相似;而用NaOH调整溶液pH为7的条件下所获得的红磷的结晶度高,(102)面强度增加,表明红磷在pH为7的环境中存在优势生长方向,HRP-pH7表面粗糙,分布着大小不一的各种孔洞,便于污染物吸附以及光生电子和空穴传输。

|
图 2 HRP和HRP-pH7样品的电镜扫描图 Fig. 2 SEM images of HRP and HRP-pH7RP samples |
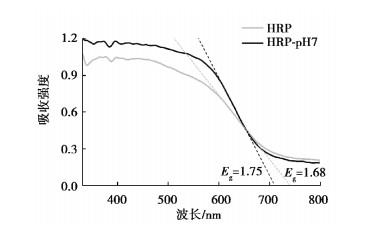
HRP和HRP-pH7催化剂的紫外可见漫反射光谱(UV-Vis DRS)表征结果见图 3。HRP和HRP-pH7催化剂对紫外和可见光均有较强的吸收,吸收波长至700 nm,吸收范围未见明显区别。与HRP相比,HRP-pH7对紫外光和可见光的吸收强度均增加了,表明调pH为7所获得的催化剂对光的利用率更高,使HRP-pH7表现出较高的光催化活性。HRP和HRP-pH7的禁带宽度通过Eg=1 240/λ0计算获得,其中Eg为禁带宽度,λ0为吸收延长线与横轴交点处的波长值。计算得出HRP和HRP-pH7样品的Eg值分别为1.68 eV和1.75 eV。与HRP相比,HRP-pH7的Eg值增大,结果说明调节pH为7水热使得催化剂的粒径变小,光吸收强度增强。
|
图 3 HRP和HRP-pH7样品的UV-vis DRS图 Fig. 3 UV-vis DRS patterns of HRP and HRP-pH7RP sample |
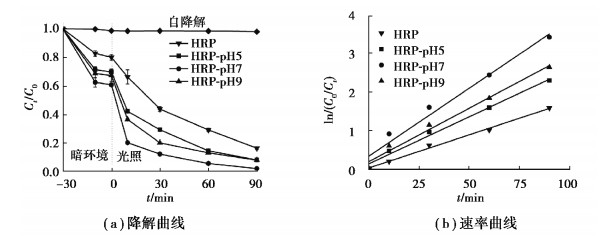
从图 4(a)可以看出,无光照条件下催化剂吸附RhB 30 min达到了吸附脱附平衡。可见光照射后,RhB在没添加催化剂的条件下并未发生明显的光解,说明RhB的稳定性较高。添加催化剂并光照条件下降解率随降解时间延长而增加,可见光照射90 min时,HRP、HRP-pH5、HRP-pH7和HRP-pH9催化剂的降解率分别为84%、91%、98.7%和92%。HRP-pH7催化剂的降解率最大。反应动力学结果表明HRP、HRP-pH5、HRP-pH7和HRP-pH9光催化降解RhB的反应均符合伪一级模型:
|
图 4 HRP、HRP-pH5、HRP-pH7和HRP-pH9光降解RhB的降解曲线和速率曲线 Fig. 4 Photocatalytic degradation and reaction kinetics of RhB by HRP, HRP-pH5, HRP-pH7 and HRP-pH9. |
| $ \ln \left( {{C_t}/C_0^\prime } \right) = - kt, $ | (2) |
式中:k为反应速率常数,min-1;C′0是吸附脱附平衡后RhB的浓度。
从图 4(b)可知,HRP-pH7对RhB的k值是3.55×10-2,是HRP的2.1倍。数据表明控制酸碱度为中性时所得的RP光催化剂比在酸性环境、碱性环境下所得RP的光降解性能好,即酸碱度为中性时所得的RP为最佳光催化剂。Wang等[15]用红磷与TiO2在700 ℃高温复合,用50 mg复合物光降解50 mL RhB(浓度10 mg/L),90 min后的降解率为96%;本研究中通过调节pH为7水热处理后得到HRP-pH7,用50 mg HRP-pH7降解200 mL RhB(浓度10 mg/L),90 min后达到更高的降解率98.7%。红磷的着火点约240 ℃,高温会使红磷燃烧转化为白磷。所以从工艺角度考虑,本研究所提出的处理红磷的方法更安全。Ansari等[12]通过球磨提高红磷的光催化活性,经过球磨36 h的红磷需要反应360 min才将10 mg/L的RhB降解完,活性也远低于本研究所得的HRP-pH7。
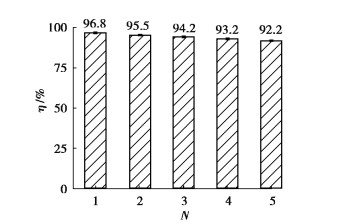
2.2.2 稳定性用光降解性能最佳的RP-pH7进行循环实验,实验结果如图 5,其中η为降解率,N为循环次数。RP-pH7在5次循环实验之后其降解率仍然高于92%,表明RP-pH7有较高的催化活性以及较好的稳定性。
|
图 5 HRP-pH7催化剂的循环实验 Fig. 5 The photocatalytic activity of HRP-pH7 in five circles of degradation experiments |
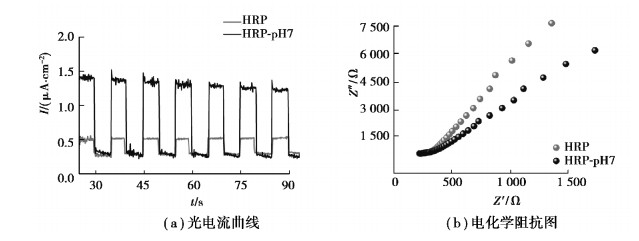
在反复开/关照明测试中HRP和HRP-pH7的光电流曲线见图 6(a),图中I为电流,t为时间。在光照条件下HRP和HRP-pH7电极均由于在催化剂表面生成的光生电荷而产生光电流响应信号,当光照结束,催化剂电极上的光电流快速消失,均表现出快速而重复的光电流响应,且HRP-pH7催化剂上的光电流值远大于HRP(2.8倍)。结果表明,与HRP相比,HRP-pH7催化剂在光照下会产生更多的载流子,众所周知,载流子越多越利于光催化反应。
|
图 6 HRP和HRP-pH7的光电流曲线和电化学阻抗图 Fig. 6 Photocurrent response and electrochemical impedance spectra of HRP and HRP-pH7 |
HRP和HRP-pH7的阻抗曲线如图 6(b)所示,图中Z′为电导组件的总阻抗的实部,[Z]″为虚部。与HRP工作电极相比,HRP-pH7工作电极上的阻抗圆弧半径减小,说明其阻抗值小,光催化降解污染物的反应所需要克服的能垒小,因此在电极上更容易发生光催化反应,表明HRP-pH7催化剂光降解RhB的活性高于HRP的原因是反应所需要克服的能垒低了。
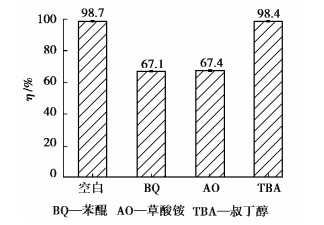
光生空穴(h+)、羟基自由基(·OH)和超氧自由基(·O2-)等作为活性物在光降解有机污染物反应中起重要的作用[16-17]。为了确定本实验中哪些活性物中在HRP-pH7降解RhB的反应中起主要作用,我们选择了草酸铵(AO)、叔丁醇(TBA)和苯醌(BQ)分别作为h+、·OH和·O2-的捕获剂。捕获剂实验结果表明加入TBA后,HRP-pH7对RhB的降解率几乎没变化,而加入AO和BQ后,HRP-pH7对RhB的降解率明显降低(图 7)。由此可知,h+和·O2-是HRP-pH7降解RhB过程中主要的活性物种。
|
图 7 不同捕获剂对HRP-pH7降解RhB的影响 Fig. 7 Effects of different radical scavengers on the degradation efficiency of RhB by HRP-pH7 |
基于以上结果分析,提出了调节pH为7提高水热处理红磷光催化活性的潜在机制。相比于HRP,在pH为7的环境下红磷出现优势生长方向,朝着(102)面生长,结晶度增加。同时,HRP-pH7的表面变得更为粗糙,出现了各种大小不一、分布不均的孔洞,总比表面积和孔径均增大,利于污染物的吸附富集、光生电子和空穴的传输。可见光的辐照下,体系吸收光子,因红磷具有较窄的带隙,很容易被激发产生电子和空穴。HRP-pH7催化剂的光吸收强、反应能垒小,使得催化剂更易降解污染物。
3 结论用NaOH溶液调制出酸、中、碱性环境下的RP溶液,采用水热合成法处理商业RP获得HRP、HRP-pH5、HRP-pH7和HRP-pH9光催化剂。表征结果显示HRP-pH7光催化剂的结晶度高、粒径更小。进一步光降解实验发现HRP-pH7的光催化性能最好,光降解速率是HRP的2.1倍。重复实验发现HRP-pH7循环降解5次后仍保持较高的光催化活性(对RhB的光降解率高于92%)。机理探究表明,光催化活性提高的原因是调节pH为中性后,其活性物种增多,光生电子和空穴分离效率高。研究表明HRP-pH7是一种很有应用前景的光催化剂。
| [1] |
Zhang Z Z, Liang Y Q, Huang H L, et al. Stable and highly efficient photocatalysis with lead-free double-perovskite of Cs2AgBiBr6[J]. Angewandte Chemie International Edition, 2019, 58(22): 7263-7267. DOI:10.1002/anie.201900658 |
| [2] |
Buzzetti L, Crisenza G E M, Melchiorre P. Mechanistic studies in photocatalysis[J]. Angewandte Chemie International Edition, 2019, 58(12): 3730-3747. DOI:10.1002/anie.201809984 |
| [3] |
Yang J, Du J, Li X Y, et al. Highly hydrophilic TiO2 nanotubes network by alkaline hydrothermal method for photocatalysis degradation of methyl orange[J]. Nanomaterials, 2019, 9(4): 526. DOI:10.3390/nano9040526 |
| [4] |
Liu Y P, Shen S J, Zhang J T, et al. Cu2-xSe/CdS composite photocatalyst with enhanced visible light photocatalysis activity[J]. Applied Surface Science, 2019, 478: 762-769. DOI:10.1016/j.apsusc.2019.02.010 |
| [5] |
Zhang G P, Chen D Y, Li N J, et al. Preparation of ZnIn2S4 nanosheet-coated CdS nanorod heterostructures for efficient photocatalytic reduction of Cr(VI)[J]. Applied Catalysis B:Environmental,, 2018, 232: 164-174. DOI:10.1016/j.apcatb.2018.03.017 |
| [6] |
Wang F, Ng W K H, Yu J C, et al. Red phosphorus:an elemental photocatalyst for hydrogen formation from water[J]. Applied Catalysis B:Environmental, 2012, 111/112: 409-414. DOI:10.1016/j.apcatb.2011.10.028 |
| [7] |
Ceppatelli M, Bini R, Caporali M, et al. High-pressure chemistry of red phosphorus and water under near-UV irradiation[J]. Angewandte Chemie International Edition, 2013, 52(8): 2313-2317. DOI:10.1002/anie.201208684 |
| [8] |
Li W B, Yue J G, Hua F X, et al. Enhanced visible light photocatalytic property of red phosphorus via surface roughening[J]. Materials Research Bulletin, 2015, 70: 13-19. DOI:10.1016/j.materresbull.2015.04.009 |
| [9] |
Shen Z R, Sun S T, Wang W J, et al. A black-red phosphorus heterostructure for efficient visible-light-driven photocatalysis[J]. Journal of Materials Chemistry A, 2015, 3(7): 3285-3288. DOI:10.1039/C4TA06871H |
| [10] |
Shi Z S, Dong X F, Dang H F. Facile fabrication of novel red phosphorus-CdS composite photocatalysts for H2 evolution under visible light irradiation[J]. International Journal of Hydrogen Energy, 2016, 41(14): 5908-5915. DOI:10.1016/j.ijhydene.2016.02.146 |
| [11] |
Ren Z P, Li D H, Xue Q, et al. Facile fabrication nano-sized red phosphorus with enhanced photocatalytic activity by hydrothermal and ultrasonic method[J]. Catalysis Today, 2020, 340: 115-120. DOI:10.1016/j.cattod.2018.09.029 |
| [12] |
Ansari S A, Ansari M S, Cho M H. Metal free earth abundant elemental red phosphorus:a new class of visible light photocatalyst and photoelectrode materials[J]. Physical Chemistry Chemical Physics, 2016, 18(5): 3921-3928. DOI:10.1039/C5CP06796K |
| [13] |
Wu Y, Liu Z, Zhong X W, et al. Amorphous red phosphorus embedded in sandwiched porous carbon enabling superior sodium storage performances[J]. Small, 2018, 14(12): 1703472. DOI:10.1002/smll.201703472 |
| [14] |
Ma Y H, Wang J J, Xu S M, et al. Ag2O/sodium alginate-reduced graphene oxide aerogel beads for efficient visible light driven photocatalysis[J]. Applied Surface Science, 2018, 430: 155-164. DOI:10.1016/j.apsusc.2017.03.299 |
| [15] |
Wang J, Zhang D K, Deng J K, et al. Fabrication of phosphorus nanostructures/TiO2 composite photocatalyst with enhancing photodegradation and hydrogen production from water under visible light[J]. Journal of Colloid and Interface Science, 2018, 516: 215-223. DOI:10.1016/j.jcis.2018.01.003 |
| [16] |
Che H N, Liu C B, Hu W, et al. NGQD active sites as effective collectors of charge carriers for improving the photocatalytic performance of Z-scheme g-C3N4/Bi2WO6 heterojunctions[J]. Catalysis Science & Technology, 2018, 8(2): 622-631. |
| [17] |
Jiang Z F, Jiang D L, Yan Z X, et al. A new visible light active multifunctional ternary composite based on TiO2-In2O3 nanocrystals heterojunction decorated porous graphitic carbon nitride for photocatalytic treatment of hazardous pollutant and H2 evolution[J]. Applied Catalysis B:Environmental, 2015, 170/171: 195-205. DOI:10.1016/j.apcatb.2015.01.041 |
 2020, Vol. 43
2020, Vol. 43


