2. 上海市钢铁冶金新技术开发 应用重点实验室, 上海 200072;
3. 上海大学 材料科学与工程学院, 上海 200072;
4. 上海特种铸造工程 技术研究中心, 上海 201605;
5. 中国科学院 上海微系统与信息技术研究所, 上海 200050
2. Shanghai Key Laboratory of Advanced Ferrometallurgy, Shanghai 200072, P. R. China;
3. School of Materials Science and Engineering, Shanghai University, Shanghai 200072, P. R. China;
4. Shanghai Special Casting Engineering Technology Research Center, Shanghai 201605, P. R. China;
5. Shanghai Institute of Microsystem and Information Technology Chinese Academy of Sciences, Shanghai 20050, P. R. China
作为AB型储氢合金的典型代表,TiFe基储氢合金是美国国立布鲁克海文实验室的Reilly等[1]在1974年首先提出来的。作为储氢材料,TiFe合金的储氢密度极高(可达5.7×1022氢原子/cm3)[2],超过了液氢的密度,与固态氢的密度相近。经过活化后,不需要气体钢瓶的高压和液氢的低温,在室温下就能可逆地吸放大量的氢,其理论值达1.86%,平衡氢压在室温下仅为0.3 MPa[3],而且资源丰富,价格低廉,很接近工业实用。TiFe合金还有难活化、易受杂质气体毒化和吸放氢平衡压差大的不足,为了改善TiFe的活化特性,常用第三组元部分置换Fe的方法来调整其相应的元素和成分,形成TiFe1-xMx形式的合金。第三组元(M)多是过渡金属,如Mn、Ni、Co、Cr、Cu、Mo、Al、Nb、Zr和V等元素。因此,无论从储氢量、室温平衡压、原料资源等方面考虑,TiFe系储氢合金都是最具有工业化应用前景的储氢材料之一[4]。
感应熔炼法作为工业上最常用的TiFe合金的制备工艺[5],其熔炼规模可从几公斤到几吨不等,具有可批量生产、成本低等优点。近些年,机械合金化法[6]、固相反应合成法[7]、FFC法[8](熔盐电脱氧法)和SOM法[9](固体透氧膜法)也逐步发展起来,但机械合金化法需要较长的球磨时间,效率低下,还易引入Fe、O等元素的污染;固相反应合成法制备TiFe储氢合金,由于在反应时产物始终为固态,TiFe的形成主要靠Fe、Ti原子之间的接触扩散来实现,合金化很难完成;FFC法也存在使用时阳极石墨易烧蚀和电解电位不易控制;SOM法虽成功用于多种金属单质的制备,但也局限于实验室或少量生产时使用。
熔炼法常采用水冷铜坩埚或石墨坩埚,在惰性气体保护下熔炼TiFe合金,但是水冷铜坩埚会带走大量的热,造成能源浪费,且热场不均匀,合金组织难以控制,影响其储氢性能[10]。而使用石墨坩埚则会使TiFe储氢合金增碳,生成大尺度脆性层,从而降低TiFe基储氢合金的储氢性能[11, 12, 13]。因此,需要寻找一种熔炼TiFe基储氢合金的新方法来改变现状。
钛在熔融状态下具有极高的化学活性,几乎与所有的耐火材料发生反应,如MgO、Al2O3、SiO2、ZrO2等都会与液钛发生剧烈的反应,故均不适合作为熔炼TiFe储氢合金的耐火材料[14, 15, 16]。但在国外,有一些研究中已经将BaZrO3作为耐火材料来生长高温超导材料YBCO单晶,其与合金熔体表现出良好的反应惰性[17, 18]。张钊等[19]采用自制BaZrO3坩埚进行TiNi合金真空感应熔炼实验,实验表明,BaZrO3耐火材料与TiNi合金熔体表现出较差的润湿性能,熔体金属与坩埚之间无反应中间层存在。而将BaZrO3耐火材料应用于TiFe系储氢合金的熔炼制备的研究还未见报道。因此,针对石墨坩埚熔炼TiFe基储氢合金导致铸锭增碳的缺点,在对BaZrO3耐火材料用于熔炼钛及钛合金的研究结果的基础上[20],试图将BaZrO3坩埚用于熔炼TiFe基储氢合金,并与石墨坩埚熔炼的合金作对比,对两种坩埚熔炼后的TiFe合金进行金相组织分析、XRD分析、化学成分分析、合金内C、O元素含量的测定及PCT储氢性能测试。
1 实验材料及方法熔炼实验分别在自合成25kg级BaZrO3坩埚及三高石墨坩埚中进行。自合成BaZrO3坩埚是将粒径在0~1 mm与1~3 mm的BaZrO3粉体,按照体积比约为1:2进行混合、称量,以液体石蜡为黏结剂(1 500 ml/20 kg),采用等静压成型技术配合固相烧结技术,分段焙烧制成坩埚成品[21]。熔炼所用合金组分以99.9%钛棒、99.9%纯铁、电解锰、高纯钴为原料,4种原料的碳、氧质量分数见表 1,按照TiFe0.94Mn0.02Co0.04的设计成分进行称量、配料,合金铸锭质量为15 kg左右,实验铸锭熔炼前用名义成分为TiFe合金配料分别对BaZrO3及石墨坩埚进行4~6次洗埚,每次装炉量均为15 kg。将自制BaZrO3坩埚熔炼的合金编号为1#样品,BaZrO3坩埚的规格尺寸为:内径×高=150 mm×300 mm;铸锭尺寸规格约为:直径×高=150 mm×200 mm,坩埚外形及所浇注后的合金铸见图 1。熔炼装置为ZG-0.05型真空感应熔炼炉,熔炼时以高纯Ar气作保护气体,通过调节真空感应炉的功率控制熔炼温度,升温速度为5 kW/5 min,直到熔化。精炼期功率控制在20 kW,精炼时间5~10 min,最后浇铸在周围有石英砂填充的黏土石墨铸型内,而三高石墨坩埚熔炼的合金则为2#样品。得到合金铸锭,后经过表面清理、切割、粗磨、细磨后备用。
| 表 1 所用原料及碳、氧的质量分数 Table 1 Oxygen content of the raw materials |

|
图 1 BaZrO3坩埚及浇注所得铸锭 Fig. 1 BaZrO3 crucible and the ingot |
用Leca光学显微镜和JSM6700F型带能谱仪的扫描电镜分析1#和2#合金的金相组织及微区元素分布,然后用D/Max-2200型X射线衍射仪对熔炼后的合金铸锭进行物相分析,1#、2#样品熔炼前后合金内C、O元素含量由CS-600碳硫测定仪和TC-436氮氧测定仪测定,两组合金的化学成分则由IRIS Advantage ICP-AES型电感耦合等离子体(ICP)原子发射光谱分析仪分析,最后采用美国应用材料公司(ANIC)的气体反应控制器测定合金的P-C-T储氢曲线。
2 实验结果及分析讨论 2.1 化学成分分析实验所用合金的理论配料和合金成分见表 2,配料过程各元素均未考虑烧损情况。
| 表 2 1#和2#合金的化学成分 Table 2 Chemical composition of the sample 1# and 2# |
Busch等[22]认为TiFe基储氢合金的化学成分偏离化学计量比时,其有效储氢量也会明显减少,而真空感应熔炼技术能够很好地控制合金的化学成分,从表 2可知,熔炼后1#合金的化学计量比为TiFe0.935Mn0.0221Co0.041,与目标成分配比TiFe0.94Mn0.02Co0.04相吻合,2#合金的化学计量比为TiFe0.932Mn0.021Co0.042,与目标成分配比相吻合,这表明使用BaZrO3坩埚和石墨坩埚真空感应熔炼后,两组合金的Ti和Fe两种元素的烧损率均低于0.60%,只有Mn和Co的烧损率偏高(在5.0%左右),合金成分与实际配料成分吻合。
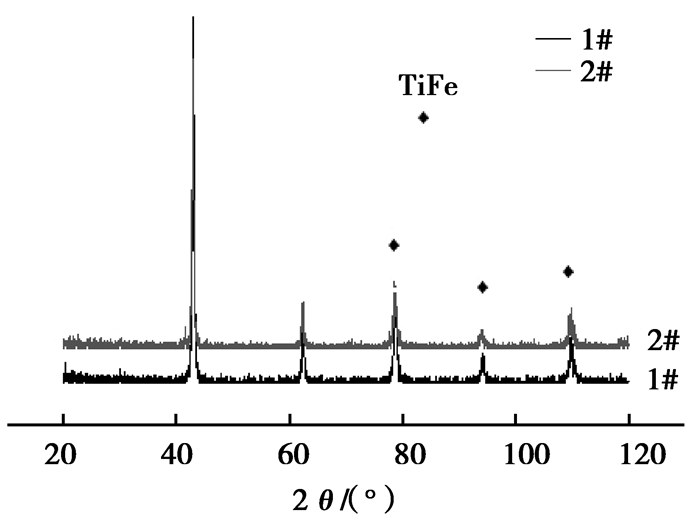
2.2 XRD分析图 2是用BaZrO3坩埚和石墨坩埚熔炼后1#和2#合金样品的XRD图谱,图 2表明:1#和2#合金完全是由CsCl型结构的立方FeTi相构成,之所以没有其他物象存在,是因为X射线衍射仪检测精度有限,无法检测到含量很少物相的存在。
|
图 2 1#和2#样品的XRD图谱 Fig.2 X-ray diffraction (XRD) patterns of the sample 1# and 2# |
沿1#和2#合金铸锭的纵切面切开,在中心部位进行取样,经粗磨、细磨、机械抛光,最后对样品进行化学腐蚀,腐蚀剂配比(体积比)为:V(HF):V(HNO3):V(C2H5OH )=1:1:3。利用Leca金相显微镜观察金相组织,图 3是分别用BaZrO3坩埚和石墨坩埚熔炼后得到的合金铸锭的金相组织,从图 3(a)和(b)看到,1#样品金相组织为等轴晶组织,2#样品则由等轴晶组织和在晶粒内或沿晶界分布的黑色颗粒物构成;从图 3(c)和(d)看到,1#样品仍为等轴晶组织,而2#样品则由等轴晶组织和沿晶界或在晶粒内弥散分布的黑色颗粒物组成。

|
图 3 1#和2#样品腐蚀后的金相组织 Fig. 3 Optical micrographs of the sample 1# and 2# alloys |
本实验利用HITEACHI SU-1500钨丝灯扫描电子显微镜分析TiFe合金的表面形貌及微区元素分布,图 4是1#和2#合金的显微组织,表 3是1#和2#合金在不同区域的EDS分析结果,结合图 3的金相组织可以分析,1#合金由均匀分布的等轴晶组织构成,2#合金则由等轴晶组织和沿其晶界或在晶粒内分布的白色球形颗粒物构成,值得注意的是,图 3和图 4所示1#和2#熔炼样品的晶体形貌明显不同,这是因为在2#合金熔体中存在大量细小的TiC颗粒,浇铸后合金凝固时,这些TiC颗粒将作为2#合金非均匀形核的核心,促进了结晶晶核的形成,这些晶核迅速长大至相互接触,形成细小的等轴晶组织。

|
图 4 1#和2#合金的SEM图 Fig. 4 SEM images of the sample 1# and 2# |
| 表 3 1#和2#合金的EDS分析 Table 3 EDS results of the sample 1# and 2# |
由表 3可知,1#合金区域A的组成为TiFe0.932Mn0.019Co0.035,B区域的组成为TiFe0.569Mn0.024Co0.041,即1#合金中区域A处Ti、Fe、Mn和Co元素在基体中均匀分布,B处Fe元素流失比较严重。同时由表 2知,1#熔炼样品中Fe的配料成分为46.11%,1#熔炼样品的化学成分分析表明,其Fe元素的成分为46.18%,而A、B处EDS分析表明,A处Fe质量分数为50.52%,B处Fe质量分数为38.11%,考虑到EDS的测试误差,可以将A处的大小枝晶组织考虑为富Fe相,而B处的枝晶间则为贫Fe区域。
同时,由表 3可知,2#合金C区域的组成为TiFe0.945Mn0.016Co0.044C0.042,D区域的组成为 TiFe0.047Mn0.024Co0.053C0.932,考虑到EDS的测试精度,可认为在2#合金D区域的白色球形颗粒物只含Ti和C元素,且Ti和C元素的物质的量之比接近1:1,由于石墨坩埚中C元素的引入,2#合金生成了一种TiC新相,因此,可以确定2#合金中的白色球形颗粒物是TiC。C元素的引入,不仅结合一部分Ti元素,而且TiC没有吸放氢的能力,因此,会降低合金的最大吸氢量。
2.5 C、O含量测定有文献报道,采用石墨坩埚熔炼制备TiFe基储氢合金时,碳与FeTi在高温下反应生成高熔点的TiC,而TiC相几乎不吸氢,从而降低FeTi合金的储氢能力[22];而氧对氢化性质的影响较大,因为FeTi相是TiFe基储氢合金中最主要的吸氢相,液态FeTi对氧有非常高的亲和力和溶解度,氧的存在使FeTi储氢能力大幅度降低,因此,在制备TiFe基储氢合金时,要严格控制碳、氧的混入,要求碳、氧含量均应低于0.1%,最好低于0.01%。
由表 4可以看出,1#合金和2#合金的氧含量分别为0.097%和0.038%,可见两组合金熔炼后的含氧量均低于0.1%,符合TiFe基储氢合金对O元素含量的技术要求;但是1#样品的碳含量仅为0.016%,这是由于合金原料中碳含量决定的,2#样品的碳含量却为 0.417%,已超过TiFe基储氢合金对碳含量低于0.1%的技术要求,这表明合金在经BaZrO3坩埚熔炼后,可以克服由石墨坩埚熔炼所带来的增碳,且符合将TiFe基储氢合金对杂质元素C、O含量控制在0.1%以下的技术要求。
| 表 4 1#和2#合金的C、O元素含量 Table 4 Oxygen and carbon content of the sample 1# and 2# |
利用美国应用材料公司(ANIC)的气体反应控制器测试了1#和2#合金在333 K下的吸放氢P-C-T曲线,如图 5所示。由图可知,333 K时,1#,2#合金的吸氢平台压力分别为(5.83~7.67)×105 Pa和(8.19~9.92)×105 Pa,放氢平台压力分别为(2.81~4.35)×105 Pa和(3.24~5.48)×105 Pa,并且1#,2#合金的最大吸氢量分别为1.854%和1.835%,可见,1#合金不仅比2#合金的最大吸氢量要稍大,而且1#合金的吸放氢平台压力略低于2#合金的吸放氢平台压力,由此认为用BaZrO3坩埚熔炼TiFe基储氢合金,可以克服石墨坩埚熔炼引起的增碳,同时,其熔炼的合金具有不弱于石墨坩埚熔炼合金的储氢性能。

|
图 5 1#和2#合金样品的吸放氢P-C-T曲线的比较 Fig. 5 Absorption and desorption P-C-T curves of the sample 1# and 2# |
1) 1#熔炼样品的氧含量与2#熔炼样品的氧含量均符合要求且未见增碳,但2#样品的碳含量却为0.417%,已超过TiFe基储氢合金对C含量要低于0.1%的技术要求,即BaZrO3坩埚真空感应熔炼TiFe合金,能有效控制合金的化学成分及氧含量,同时,还能克服因石墨坩埚熔炼后合金铸锭的增碳。
2) 两种坩埚熔炼后合金的微观组织相差很大,BaZrO3坩埚熔炼后合金完全由等轴晶构成,而石墨坩埚熔炼后合金则由等轴晶组织和在晶粒内或沿晶界分布的球形TiC颗粒组成。
3) 1#合金和2#合金的最大吸氢量分别为1.854%和1.835%,吸氢平台压分别为(5.83~7.67)×105 Pa和(8.19~9.92)×105 Pa,放氢平台压分别为(2.81~4.35)×105 Pa和(3.24~5.48)×105 Pa,1#合金的吸放氢平台压均比2#要低,即经BaZrO3坩埚熔炼后的TiFe基储氢合金,具有不弱于石墨坩埚所熔炼合金的储氢性能,这表明BaZrO3坩埚真空感应熔炼技术是一种制备TiFe基储氢合金的新型技术。
| [1] | Reilly J J, Wiswall R H. Formation and properties of iron titanium hydride[J]. Inorganic Chemistry, 1974, 13:218-222.( 1) 1) |
| [2] | Suriñach S, Baró M D, Segura J, et al. Amorphization of soft magnetic alloys by the mechanical alloying technique[J]. Materials Science and Engineering A, 1991, 134(91):1368-1371.( 1) 1) |
| [3] | 赵强,薛建伟,杜志刚,等.TiFe系贮氢合金研究进展[J].山西化工,2005,25(2):1-7. ZHAO Qiang, XUE Jianwei, DU Zhigang, LI Jinping. Research progress of TiFe-based hydrogen storage alloy[J]. Shanxi Chemical Industry, 2005, 25(2):1-7. (in Chinese)( 1) 1) |
| [4] | 马建新,王新华,葛红卫,等.FeTi系贮氢合金的研究进展[J].材料科学与工程,1999,17(1):65-69. MA Jianxin, WANG Xinhua, GE Hongwei, et al. Recent Research and Development on FeTi System Hydrogen Storage alloy[J]. Journal of Materials Science and Engineering, 1999, 17(1):65-69. (in Chinese)( 1) 1) |
| [5] | Reilly J J, Wiswall R H. The reaction of hydrogen with alloys of magnesium and nickel and the formation of Mg2NiH4[J]. Inorganic Chemistry, 1968, 7(11):2254-2256.( 1) 1) |
| [6] | Cuevas F. Mechanochemical synthesis of hydrogen storage materials[J]. Progress in Materials Science, 2013, 58(1):30-75.( 1) 1) |
| [7] | Zou X, Lu X, Ding W. Direct synthesis of TiFe alloy from mixed metal oxides[J]. Rare Metal Materials and Engineering, 2011, 40(1):169-172.( 1) 1) |
| [8] | 廖先杰,翟玉春,谢宏伟,等.700℃熔盐电解制备固态钛铁合金化合物[J].材料研究学报,2009,23(2):133-137. LIAO Xianjie, ZHAI Yuchun, XIE Hongwei, et al. Preparation of solid state Fe-Ti alloy compound by FFC in molten salts at 700℃[J]. Chinese Journal of Materials Research, 2009, 23(2):133-137. (in Chinese)( 1) 1) |
| [9] | Pal U B, Iv A C P. The use of solid-oxide-membrane technology for electrometallurgy[J]. Jom the Journal of the Minerals Metals & Materials Society, 2007, 59(5):44-49.( 1) 1) |
| [10] | 胡子龙.储氢材料[M].北京:化学工业出版社,2002. HU Zilong. Hydrogen storage materials[M]. Beijing:Chemical Industry Press, 2002. (in Chinese)( 1) 1) |
| [11] | Ye F, Yang M C, Sun X K, et al. The formation of TiFe nanoparticles by gas condensation method[J]. Nanostructured Materials, 1997, 9(1-8):113-116.( 1) 1) |
| [12] | Liu T, Shao H, Li X. Synthesis and characteristics of Ti-Fe nanoparticles by hydrogen plasma-metal reaction[J]. Intermetallics, 2004, 12(1):97-102.( 1) 1) |
| [13] | 徐海鸥,陈长聘,王澂,等.Ti1.2Fe+x%Mg(x=1,3,5)合金的贮氢特性[J].稀有金属材料与工程, 2003,32(3):220-223. XU Haiou, CHEN Changpin, WANG Wei, et al. Hydrogen storage properties of Ti1.2Fe+x%Mg(x=1,3,5) alloys[J]. Rare metal materials and engineering, 2003, 32(3):220-223. (in Chinese)( 1) 1) |
| [14] | Kuang J P, Harding R A, Campbell J. Investigation into refractories as crucible and mould materials for melting and casting (-TiAl alloys[J]. Materials Science and Technology, 2000, 16(9):1007-1016.( 1) 1) |
| [15] | Barbosa J, Ribeiro C S, Teodoro O M N D, et al. Evaluation of Y2O3 as front layer of ceramic crucibles for vacuum induction melting of TiAl-based alloys[J]. Journal of Solid State Chemistry, 2005, 157(2):241-249.( 1) 1) |
| [16] | Sadrnezhad S K, Raz S B. Interaction between refractory crucible materials and the melted NiTi shape-memory alloy[J]. Metallurgical and Materials Transactions B, 2005, 36(3):395-403.( 1) 1) |
| [17] | Os'kina T E, Wehler D, Piel H, et al. A new method of YBa2Cu3O7-x single-crystal growth in Al2O3 crucibles with layered protective covers[J]. Physica C:Superconductivity, 1995, 242(1/2):85-89( 1) 1) |
| [18] | Liang R, Dosanjh P, Bonn D A, et al. Growth and properties of superconducting YBCO single crystals[J]. Physica C:Superconductivity, 1992, 195(1/2):51-58.( 1) 1) |
| [19] | 张钊,朱凯亮,刘岚洁,等.BaZrO3坩埚的制备及与钛合金熔体的界面反应[J].硅酸盐学报,2013,41(9):1278-1283. ZHANG Zhao, ZHU Kailiang, LIU Lanjie, et al. Preparation of BaZrO3 crucible and its interfacial reaction with molten Titanium alloys[J].Journal of the Chinese Ceramic Society, 2013, 41(9):1278-1283. (in Chinese)( 1) 1) |
| [20] | 刘岚洁,陈光耀,张钊,等.BaZrO3耐火材料与TiM(M=Fe,Ni)熔体的界面反应[J].热加工工艺,2013,42(11):49-54. LIU Lanjie, CHEN Guangyao, ZHANG Zhao, et al. Interface reaction between refractory BaZrO3and TiM(M=Fe,Ni) melt[J]. Hot Working Technology, 2013, 42(11):49-54. (in Chinese)( 1) 1) |
| [21] | 邢方圆,陈光耀,朱凯亮,等.大尺寸BaZrO3坩埚的制备及其在在TiNi形状记忆合金熔炼中的应用[J].太原理工大学学报,2014,45(2):172-175. XING Fangyuan, CHEN Guangyao, ZHU Kailiang, et al. Preparation of large size BaZrO3 crucible and its application to the melting of TiNi shape memory alloy[J]. Journal of Taiyuan University of Technology, 2014, 45(2):172-175. (in Chinese)( 1) 1) |
| [22] | Busch G, Schlapbach L, Stucki F. Hydrogen storage in FeTi:Surface segregation and its catalytic effect on hydrogenation and structural studies by means of neutron diffraction[J]. International Journal of Hydrogen Energy, 1979, 4(1):29-39.( 2) 2) |
 2016, Vol. 39
2016, Vol. 39

