2. 国网重庆市电力公司电力科学研究院, 重庆 401123;
3. 四川宇峰科技发展有限公司, 四川 绵阳 621000
2. Electric Power Research Institute, State GridChongqing Electirc Power Company, Chongqing 401123, China;
3. Sichuan Yufeng Science andTechnology Development Co., Ltd., Mianyang, Sichuan 621000, China
血管性疾病是当今人类致死和致残的主要疾病。目前,中国每年死于该类疾病的人数约占中国年总死亡人数的50%,在幸存患者中致残率高达七成,同时中国每年用于该类疾病的花费高达数百亿元。研究表明,作为慢性病的心血管疾病,若能在临床发病前的早期阶段,及时准确地检测出心血管参数的变化,预测出心血管疾病的危险因素,将是最终降低心血管疾病发生率的唯一出路[1]。因此,研制出一种能用于检测早期阶段动脉血管状态变化的仪器,具有很强的临床应用价值和社会意义。
基于临床应用考虑,研究者近几年多倾向于采用基于动脉弹性腔理论和示波法原理的技术来实现对动脉血管状态变化的早期无创检测[2-4]。天津大学赵学玲等2008年设计了基于ARM的无创心血管功能检测系统,能同时测量10项心血管参数,并进行了30人的初步实验[5]。2008年澳门大学Li等实现了一种基于嵌入式平台的移动式脉搏波分析仪,并在其课题组范围内进行了评估测试[6]。瑞士CSEM研究所Josep Solà等2011年通过安置于胸腔的传感器测量出中心动脉的脉搏波传递时间,用此来评估动脉硬化状态[7]。澳大利亚Artech medical公司研制的Sphygmocor device®在桡动脉压力波中利用传递函数计算中央动脉压、脉搏波传播波速(pulse wave velocity,PWV)和主动脉弹性,以此来评估血管内皮功能[8]。匈牙利TensioMed公司设计的Arteriograph通过充放气臂部袖带记录到的压力脉搏波,采用脉搏波分析技术估算主动脉PWV[9]。法国Artech公司研制的Complior System®通过安置在体表动脉处的两个压力传感器测量从颈部到股部的PWV[10]。笔者课题组从2002起开展该课题研究,研制出YF/XGYD系列动脉硬化检测仪[11-12],该仪器已经通过了临床论证测试。
但是现有仪器或者体积较大、价格昂贵,或者测量参数单一,均不适合社区医院、卫生院和巡回医疗车等基层医疗机构使用。针对这些缺点,笔者按照体积小、性价比高、操作简便以及多参数测量的设计原则,设计了一种基于ARM和WinCE的便携式无创动脉硬化检测仪(portable noninvasive detecting instrument for arteriosclerosis,PNDIA)。该仪器通过对分别安置于人体上臂肘关节附近和腕部的袖带同时充气,分析在放气过程中所测的脉搏波波形和袖带压力变化曲线,自动计算得出评判动脉血管状态的动脉硬化因子,并在打印报告中给出诊断参考。
1 动脉硬化评判因子及算法PNDIA各项测量参数的算法原理是以将人体血液循环系统等效为一个集总参数电路的假设为基础[13],它用有限数量的分立元件来模拟血液循环系统的分布特性,将电压等效为血压,电流等效为血流,电阻等效为血流阻力,电感等效为血流惯性,电容等效为血管中的动脉顺应性。临床研究表明,PWV和动脉硬化指数(arterial stiffness index,ASI)与动脉硬化程度有密切的相关性[14],因此,笔者在PNDIA中主要采用这两项指数作为评判病人动脉硬化程度的评判因子。
1.1 PWV算法原理按照公式(1)来计算PWV:
| $ {\rm{PWV = }}\Delta L/\Delta t, $ | (1) |
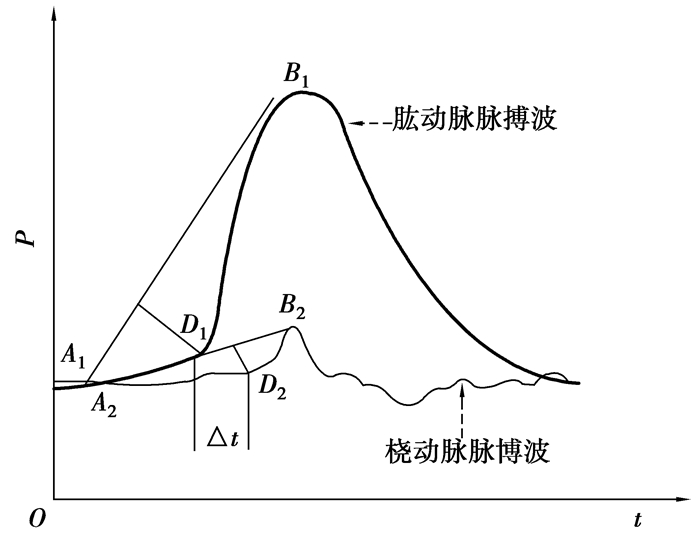
式中:ΔL为臂部肱动脉处袖带中心点到腕部桡动脉处袖带中心点的距离,PNDIA通过身高进行估算;Δt为脉搏波传播通过这段距离的时间。为了计算Δt需要先求得脉搏波的起跳点(D点),根据最值原理,分别找出同一个心动周期中肱动脉和桡动脉脉搏波的波峰点和波谷点(图 1中,肱动脉和桡动脉脉搏波的峰值点和波谷点分别为B1、B2、A1、A2),并连接波峰点和波谷点为一直线(图 1中,肱动脉和桡动脉分别为A1B1、A2B2),然后在肱动脉脉搏波波形曲线上找到一个到直线段A1B1距离最大的点,将该点设为起跳点(图 1中的D1点),用相同的方法找出桡动脉脉搏波波形曲线上的起跳点(图 1中的D2点),最后计算脉搏波从D1点到D2点的传播时间得到Δt。
|
图 1 PWV计算原理示意图 |
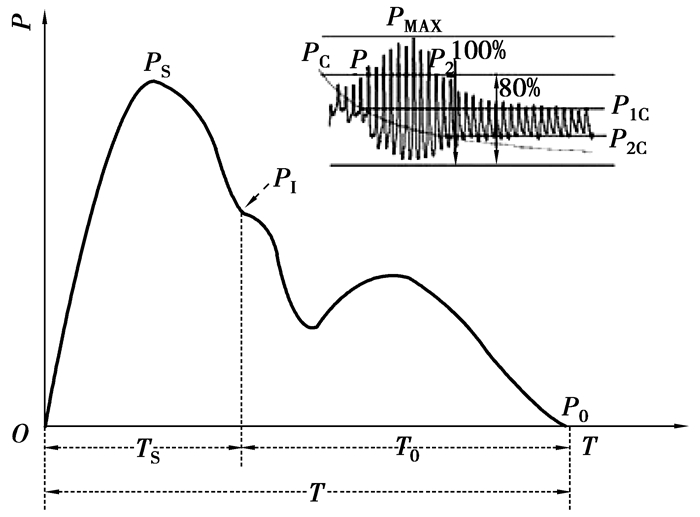
图 2右上小图表示PNDIA在袖带放气过程中(PC为袖带放气曲线)获得的脉搏波振荡曲线。为了计算ASI,首先要确定最大脉搏波的峰值PMAX,然后在PMAX前后分别找到最接近80%PMAX的脉搏波波峰(图 2中P1、P2),P1和P2分别对应袖带放气曲线PC上的点P1C和P2C,最后,由公式ASI = k×(P1C-P2C)得到ASI,其中k是由受试者的年龄、身高和体重得出的修正系数。
|
图 2 ASI及其他参数计算原理示意图 |
图 2中PI所指处为脉搏波拐点(重搏波切迹),此点大致可将心动周期T划分为收缩期TS和舒张期TD。PNDIA在一个心动周期T中进行采样,用采样率除以在一个心动周期中得到的采样点数可计算得出心率(HR);用在收缩期TS中的采样点数除以采样率,可计算得出左心室收缩时间(ET)。收缩压PS和舒张压PD基于改进的示波法计算得出,其他检测参数,如平均压PM、脉压PP、每搏心输出量SV、每分心输出量CO及血管外周阻力TRP的计算方法见公式(2)~(6)。
| $ {P_\rm{M}} = {P_\rm{D}} + \frac{{\int_0^T {p\left( t \right){\rm{d}}t} }}{T}\left( {{\rm{mmHg}}} \right), $ | (2) |
| $ {P_\rm{P}} = {P_\rm{S}} - {P_\rm{D}}\left( {{\rm{mmHg}}} \right), $ | (3) |
| $ \begin{array}{l} {S_{\rm{V}}} = - 6.6 + 0.25 \times \left( {{T_\rm{S}} - 35} \right) - 0.62 \times HR + \\ 40.4 + BSA - 0.51 \times A\;\;\;\left( {{\rm{mL}}} \right), \end{array} $ | (4) |
| $ 其中^{[15]}:BSA = 0.007 184 \times {W^{0.425}} \times {H^{0.725}} \\ CO = {S_{\rm{V}}} \times HR/1000 \;\;\; \left( {{\rm{L}}/\min } \right), $ | (5) |
| $ {\rm{TRP}} = k \times {P_{\rm{M}}}/CO\;\;\;\;\left( {{\rm{dyne}} \cdot {\rm{s}}/{\rm{c}}{{\rm{m}}^5}} \right), $ | (6) |
其中:k值是由受试者的年龄(A)、身高(H)和体重(W)得出的修正系数。
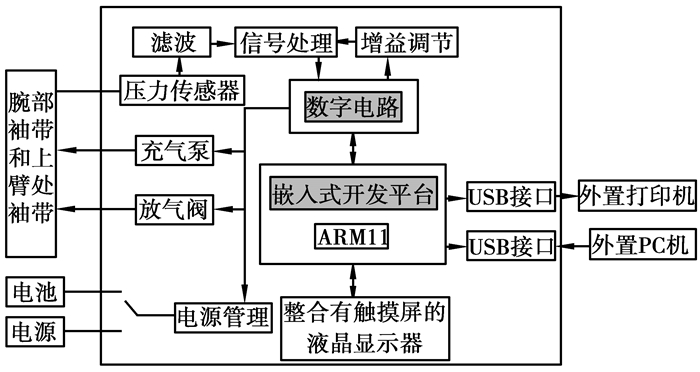
2 仪器的硬件设计PNDIA的硬件架构如图 3所示。整台仪器以一块基于ARM11的嵌入式硬件平台为核心,包括模拟信号检测和处理电路、数字电路、充/放气自动控制电路、液晶触摸显示屏、电源管理等。
|
图 3 PNDIA的硬件架构 |
采用RISC架构的ARM(Advanced RISC Machines)微处理器具有性能高、体积小、功耗低、成本低的优点,是目前嵌入式系统行业非常流行的处理器芯片。整台仪器的核心采用一块嵌入式开发平台(飞凌S3C6410开发板,OK6410-B)(图 4(a)),该开发平台采用Samsung S3C6410处理器(ARM1176JZF-S内核),256MB DDR SDRAM,2GB Nand Flash。Nand Flash上固化了嵌入式操作系统WinCE以及动脉硬化参数分析软件并同时用来存储测量数据,DDR SDRAM则用于运行WinCE及上述分析软件。该嵌入式系统平台具有多种类型的硬件接口。其中,通过一块串口扩展板(图 4(b))连接自行研发的脉搏波信号测量电路板上的RS232串口;含有一个使用MiniUSB插座的USB Slave接口,其可用于PNDIA与PC机间的数据交换;并且,通过一个38路的GPIO接口来连接一块7寸整合有触摸屏的液晶显示屏(群创AT070TN83,800×480像素)。

|
图 4 PNDIA内部硬件组成 |
PNDIA在人体上臂靠近肘关节的肱动脉处和腕部的桡动脉处分别绑置大小不同的袖带,并通过充放气来获取脉搏波信号,笔者采用美国Motorola公司生产的MPX5050DP压力传感器来作为模拟信号前端采集器,该传感器具有线性度好、方差小、精度高及抗干扰的优点,能获取失真小的脉搏波信号,提高了在ARM中所加载软件计算各种动脉硬化评判因子的可靠性。在压力传感器的信号输出之后增加了一个电压跟随器用以消除因传感器阻抗不同、带负载能力不同所造成的信号异常情况。
压力传感器输出的信号中混合有脉搏波信号、袖带压信号及由其生成的直流分量,并同时伴随有大量的噪声。研究发现人体脉搏波信号绝大部分集中在0~12 Hz,而肱动脉和桡动脉处的脉搏波信号频率范围主要在0.6~6.4 Hz。PNDIA通过3组滤波器将传感器输出的信号滤除噪声并分离为袖带压信号、肱动脉信号和桡动脉信号,如图 4上部电路板中白色矩形框内所示,最上端的一组由截止频率为0.6 Hz高通滤波器和截止频率为6.4 Hz低通滤波器共同构成的带通滤波器将传感器(图 4(c))获取的肱动脉处信号滤去噪声获得肱动脉脉搏波信号;中间的一组截止频率为0.5 Hz低通滤波器将传感器(图 4(c))获取的信号滤去脉搏波信号和高频干扰信号后得到袖带压信号,同时在其前端置一个1 μF电容来滤除直流分量;最下端的一组带通滤波器(同第一组)从传感器(图 4(d))获取的信号中滤波获得桡动脉脉搏波信号。
经过滤波器处理后输出的脉搏波信号仍然比较微弱,笔者在滤波器后设计了增益调节电路来调整信号的幅度,从而使输出信号波形幅值被调整到满足心血管参数分析的范围之内,同时也便于仪器中模/数转换芯片ADC进行可靠准确的采样。同时仪器采用一个电平调整电路将脉搏波信号的电平提升到0~3.3 V用以满足ADC芯片的模数转换电压范围。另外,为了保护ADC芯片不会因为基线漂移引起电压幅值超过3.3 V而损坏,设计了一对稳压管对经过电平调整后的信号进行钳位。
2.3 数字电路和电机充放气控制电路基于设计要求和成本控制,在数字电路和电机充放气控制电路(图 4上部电路板中白色矩形框外部)中采用C8051F020微处理器中的一个片内12位SAR ADC将上述模拟信号检测和处理电路中得到的模拟信号转换成数字信号,并通过RS232串口上传给嵌入式开发平台,应用其上固化的动脉硬化参数分析软件实时显示测量中的脉搏波形,并在测量结束后自动计算得出受试者各项心血管动力学参数。测量过程中,根据动脉硬化参数分析软件中的设置,通过C8051F020微处理器来控制袖带的自动充放气,当C8051F020中相应的I/O端口给出低电平时,电磁阀接通电源,同时阻断阀(图 4(e))导通,充气泵(图 4(f),MINI PUMP KPM27D)同时对两个袖带充气到预设的压力值(≥180 mmHg),并由动脉硬化参数分析软件自动判断血管是否阻断,若阻断,则C8051F020中相应的I/O端口给出一个高电平信号,断开充气泵电源,停止充气,同时闭合阻断阀,阻断两个袖带气路的联系。在放气过程中,由于只有在袖带压力高于40 mmHg,并且放气速度控制在3~6 mmHg/s时所获取的生理信号对分析软件有应用价值,因此,通过实验研究,分别在电磁阀g & h(图 4)之前安装了毛细玻璃管节流阀(图 4中箭头处),并且通过软件设置,首先分别导通电磁阀g & h(图 4)将袖带中气压缓慢释放到40 mmHg,以便获取所需的生理信号,然后再分别导通电磁阀i & j(图 4)迅速将袖带气压从40 mmHg释放到0 mmHg。
3 仪器的软件设计PNDIA采用嵌入式实时多任务操作系统WinCE 6.0 R3,它延伸了台式机Windows操作系统的外部特征,在内部用嵌入式实时操作系统的技术来实现Win32 API的子集,支持强大的通讯和图形显示功能[16]。动脉硬化参数分析软件是在该操作系统上用LabVIEW Touch Panel Module 8.5.1 For WinCE开发而成,其主要功能模块如下:
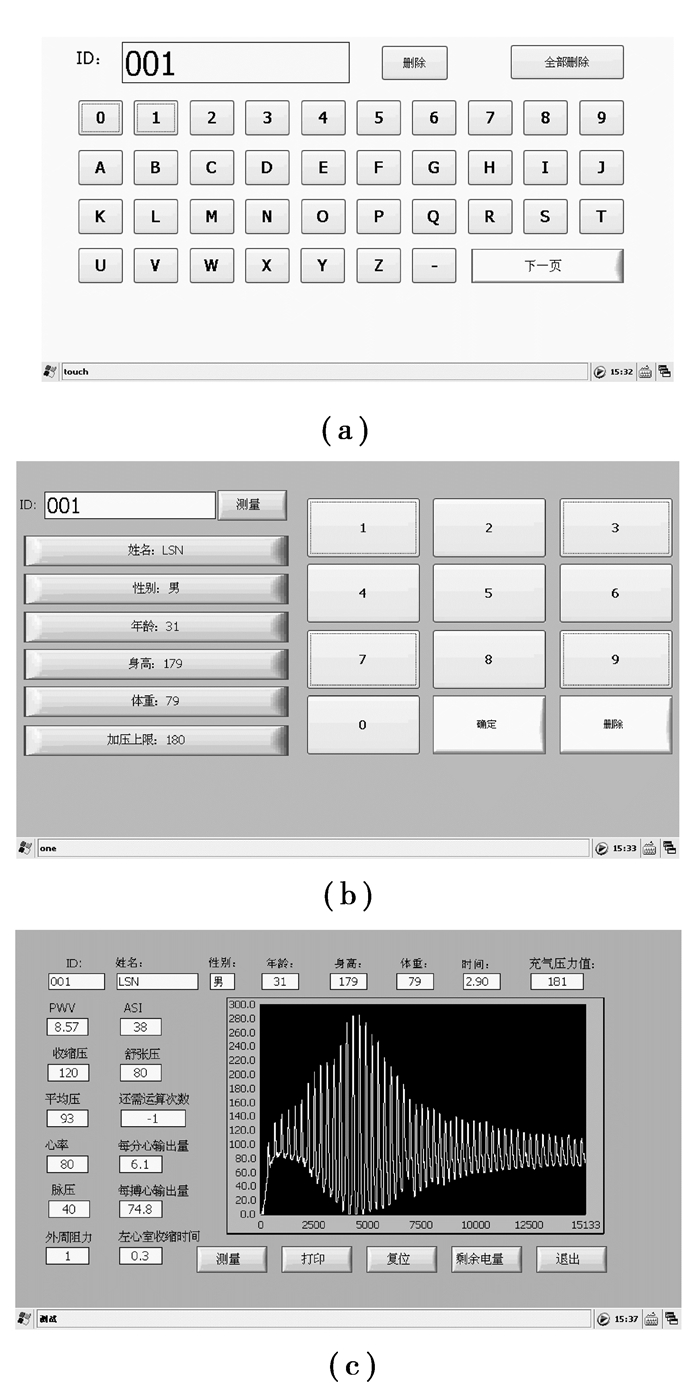
人机交互界面模块。人机交互界面如图 5所示,主要实现受试者信息输入、控件选择和测试结果输出显示等功能,图 5(a)为受试者ID输入界面;图 5(b)为受试者ID输入完成后测量准备界面,在该界面上可查看受试者姓名、性别、年龄、身高、体重及袖带加压上限等值,并且点击测量按钮框可开始进行测量;图 5(c)为测量结果显示界面,该界面上显示了受试者的各项检测参数值及动脉脉搏波振荡波形,并且可在该界面中点击不同的按钮框实现重新测量、打印、复位及查看电池剩余电量等功能。
|
图 5 PNDIA软件界面 |
数据采集模块。利用LabVIEW中VISA(virtual instrument software architecture)函数编程来实现同硬件的串口通信,并且使用自定义的协议保证通信安全。在串口通信前,需在MAX(NI measurement & automation explorer)中将通信双方的波特率、数据位、停止位、奇偶校验位和流控制5个参数设置相同。软件中波特率设置为38 400 bit/s。
信号预处理模块。软件中通过滑动平均滤波处理和合理性检查消除硬件电路滤波后脉搏波信号中仍然存在的随机干扰、奇异邻波及奇异尖峰。
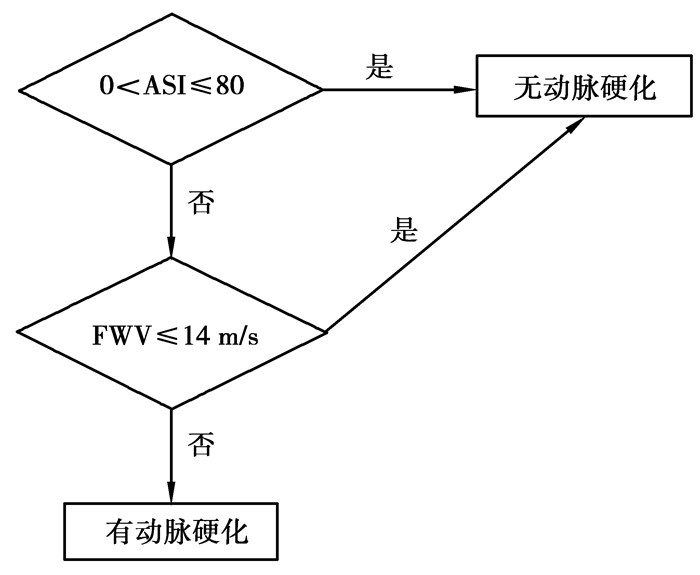
检测参数计算模块。通过LabVIEW中各种函数编程,按照前述算法计算出受试者的各项动脉硬化检测参数,并以ASI作为主要指标来评判受试者是否动脉硬化,其判断流程图如图 6所示,图 5(c)中显示该受试者ASI值为38,PWV为8.57 m/s,根据动脉硬化判断流程图,PNDIA在打印报告中给出该受试者无动脉硬化的诊断。
|
图 6 动脉硬化判断流程图 |
记录功能模块。将受试者信息及其各项检测参数存储在Nand Flash上或通过USB接口传输到外置打印机打印。
4 实验分析与结果依照国家《医疗器械临床试验规定》,对PNDIA的稳定性和可靠性进行了前期可行性实验测试。
4.1 稳定性实验为了评估PNDIA的稳定性,选取了项目组一名健康成员(男性,31岁)作为受试者。在同一天08:30—11:30、13:30—17:10两个时间段内,以20 min为间隔,共测量22次。在每次测试前,受试者需要静息10 min,并且不能抽烟和喝茶及咖啡等饮料。测试时,受试者采用坐姿,分别在其左臂肱动脉和桡动脉处绑置大小不同的两个袖带。在记录好受试者的身高、年龄、体重等个人资料后开始测量,测量过程中,受试者需要放松并保持安静,整个测量过程大约3 min。这样得到22组数据,每组11项参数。对这名受试者的测量结果进行了统计学分析。表 1是稳定性实验结果,由表 1可以看出,各检测参数的相对标准误差均在1%~5%之间,实验表明笔者开发的仪器稳定性良好。
| 表 1 稳定性实验结果 |
为了评估PNDIA的可靠性,选取了30名受试者作为研究对象。对照仪器采用目前临床上使用广泛的OMRON BP203RPEⅢ动脉硬化检测装置,该仪器测量时,需要受试者平躺在检测床上,在受试者左右臂肱动脉处以及左右下肢踝关节处各绑置一个袖带,采用同时充放气的方式测量受试者的心血管参数,并且通过PWV和踝臂指数(ABI)等参数来判断受试者的动脉血管状态。整个实验均在一间室温26 ℃、通风良好的实验室开展。在受试者静息15 min后,首先用传统的血压听诊法(Auscultatory)测量这名受试者的收缩压和舒张压;然后静息15 min,用PNDIA测量一次;最后再次静息15 min,用OMRON动脉硬化检测装置对该名受试者再测量一次;并且在测量过程中,受试者需要放松并保持安静。测试完成后,用SPSS软件对数据进行了线性回归分析,显著性水平设置为0.01。
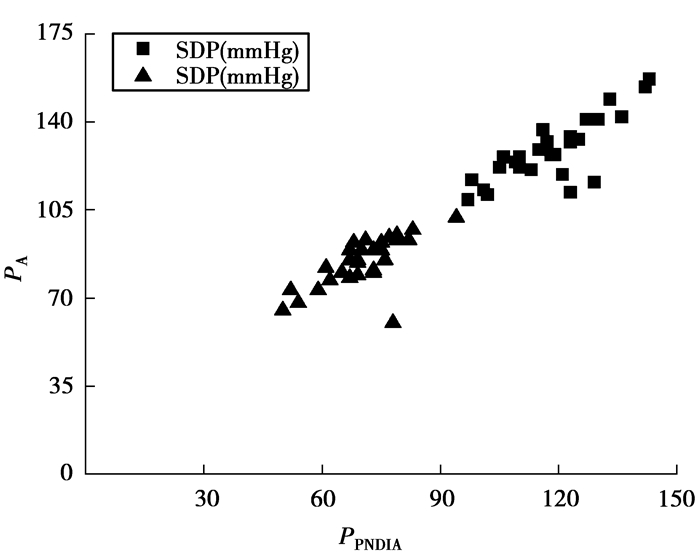
听诊法和PNDIA获得的收缩压和舒张压散点图如图 7所示,通过计算,得出相关系数r=0.95,双侧Pearson检验P=0 < 0.001,有统计学意义,说明两种方法测得的血压值高度相关。
|
图 7 收缩压和舒张压的散点图 |
表 2列出了PNDIA和对照仪器对应检测参数的测量结果,测量结果用均值(Mean)±标准差(SD)表示。从表 2可知,PNDIA同对照仪器具有优良的相关性,其中PWV的相关系数为0.96,而PWV是评判动脉硬化状态的最重要指标之一,实验表明PNDIA具有良好的可靠性。
| 表 2 PNDIA和对照仪器的测量结果 |
另外,PNDIA和对照仪器均判断出其中两名受试者动脉血管硬化并且血管中有斑块形成,用彩色多普勒超声诊断仪测量这两名受试者的颈总动脉内中膜厚度(intima-media thickness, IMT)均大于0.8 mm,同时发现有斑块生成,如表 3所示,进一步验证了PNDIA的可靠性。
| 表 3 两名动脉硬化受试者的测量结果 |
笔者设计并实现了一套基于ARM和WinCE的便携式动脉硬化无创检测仪。实验表明,该仪器重复性好,性能稳定,与同类仪器相比,具有体积小、重量轻、操作方便、成本低等优点,特别适合基层医疗机构用于动脉硬化程度和心血管功能的快速无创检测。随着进一步临床试验的开展和ARM处理器性能的提高,在下一步研究中,计划设计智能专家系统和网络通信模块,使该仪器能通过对比临床病例数据库,自动分析测量参数,智能化地判断病人心血管状态并且给出详尽的专家建议,而且能通过网络通信模块将病人检测记录同步上传到医生办公室电脑中进行保存。
| [1] |
王宏宇, 张瑞岩, 罗建方, 等.
中国血管病变早期检测技术应用指南(2011第二次报告)[J]. 心血管病学进展, 2011, 32(3): 318–323.
WANG Hongyu, ZHANG Ruiyan, LUO Jianfang, et al. Chinese guideline for early vascular disease detection (2011 second report)[J]. Advances in Cardiovascular Diseases, 2011, 32(3): 318–323. (in Chinese) |
| [2] | Liu S H, Wang J J, Wen Z C. Extraction of an arterial stiffness index from oscillometry[J]. Journal of Medical and Biological Engineering, 2007, 27(3): 116–123. |
| [3] | Westerhof N, Lankhaar J W, Westerhof B E. The arterial Windkessel[J]. Medical and Biological Engineering and Computing, 2009, 47(2): 131–141. DOI:10.1007/s11517-008-0359-2 |
| [4] | 赵学玲. 基于脉搏波的无创心血管检测技术若干关键问题研究[D]. 天津: 天津大学, 2009. |
| [5] |
赵学玲, 陈小红, 刘瑾, 等.
基于ARM的无创心血管功能检测系统[J]. 纳米技术与精密工程, 2008, 6(5): 388–393.
ZHAO Xueiling, CHEN Xiaohong, LIU Jin, et al. Non-invasive cardiovascular monitoring system based on ARM[J]. Nanotechnology and Precision Engineering, 2008, 6(5): 388–393. (in Chinese) |
| [6] | Li B N, Fu B B, Dong M C. Development of a mobile pulse waveform analyzer for cardiovascular health monitoring[J]. Computers in Biology and Medicine, 2008, 38(4): 438–445. DOI:10.1016/j.compbiomed.2008.01.008 |
| [7] | Solà J, Chételat O, Sartori C, et al. Chest pulse-wave velocity:a novel approach to assess arterial stiffness[J]. IEEE Transactions on Biomedical Engineering, 2011, 58(1): 215–223. DOI:10.1109/TBME.2010.2071385 |
| [8] | Boutouyrie P. New techniques for assessing arterial stiffness[J]. Diabetes & Metabolism, 2008, 34(Sup1): 21–26. |
| [9] | Segers P, Kips J, Trachet B, et al. Limitations and pitfalls of non-invasive measurement of arterial pressure wave reflections and pulse wave velocity[J]. Artery Research, 2009, 3(2): 79–88. DOI:10.1016/j.artres.2009.02.006 |
| [10] | Boutouyrie P, Briet M, Collin C, et al. Assessment of pulse wave velocity[J]. Artery Research, 2009, 3(1): 3–8. DOI:10.1016/j.artres.2008.11.002 |
| [11] |
陈义清, 何为.
用示波法计算动脉顺应性的研究与实现[J]. 重庆大学学报:自然科学版, 2005, 28(9): 35–38.
CHEN Yiqing, HE Wei. Research and realization of calculating artery compliance using oscillometric method[J]. Journal of Chongqing University:Natural Science Edition, 2005, 28(9): 35–38. (in Chinese) |
| [12] | 何为, 余传祥. 心血管动力学参数测量原理和临床应用[M]. 北京: 科学出版社, 2010. |
| [13] |
何为, 肖汉光, 刘兴华.
上肢动脉系统的三段式电网络建模与仿真[J]. 重庆大学学报, 2012, 35(5): 83–88.
HE Wei, XIAO Hanguang, LIU Xinghua. Modeling and simulation of the upper limb artery system using three-section electric network model[J]. Journal of Chongqing University, 2012, 35(5): 83–88. DOI:10.11835/j.issn.1000-582X.2012.05.014 (in Chinese) |
| [14] | Fu M R, Cammen T J, Hofman A, et al. Arterial stiffness and risk of coronary heart disease and stroke:the rotterdam study[J]. Circulation, 2006, 113(2): 657–663. |
| [15] | Rietzschel E R, Boeykens E, De B M L, et al. A comparison between systolic and diastolic pulse contour analysis in the evaluation of arterial stiffness[J]. Hypertension, 2001, 37(6): 15–22. DOI:10.1161/01.HYP.37.6.e15 |
| [16] |
竺乐庆, 张三元, 幸锐.
基于ARM与WinCE的掌纹鉴别系统[J]. 仪器仪表学报, 2009, 30(12): 2624–2628.
ZHU Leqing, ZHANG Sanyuan, XING Rui. Palmprint identification system based on ARM and WinCE[J]. Chinese Journal of Scientific Instrument, 2009, 30(12): 2624–2628. (in Chinese) |
 2014, Vol. 37
2014, Vol. 37



