直接还原是将铁矿石在低于熔化温度下被直接还原成固态金属产品的炼铁技术,它有效地克服了传统高炉炼铁高能耗、流程长等弱点, 已成为钢铁冶炼技术的研究热点[1-3]。根据还原剂形态的不同,可将直接还原分为气基法和煤基法。气基竖炉炼铁产量达到了直接还原铁总产量的90%以上[2]。而竖炉内还原铁矿石的主要成分则是H2及CO。采用CO及H2来还原铁矿,还原气循环利用率高,在适当情况下还可以增加H2含量、降低CO含量,减少了CO2的排放[4-5]。H2和CO还原铁矿石过程中的反应动力学,是当前研究竖炉含铁球团还原反应过程的重要课题[6-17]。而这两种气体混合后竖炉内还原铁块石的动力学模型还未见报道[9, 11, 13, 14]。笔者结合竖炉内球团矿还原模拟实验,通过分析CO和H2还原球团矿过程中的反应速率,提出混合气还原时的反应动力学模型,为研究竖炉内球团矿还原反应动力学提供一定的理论参考。
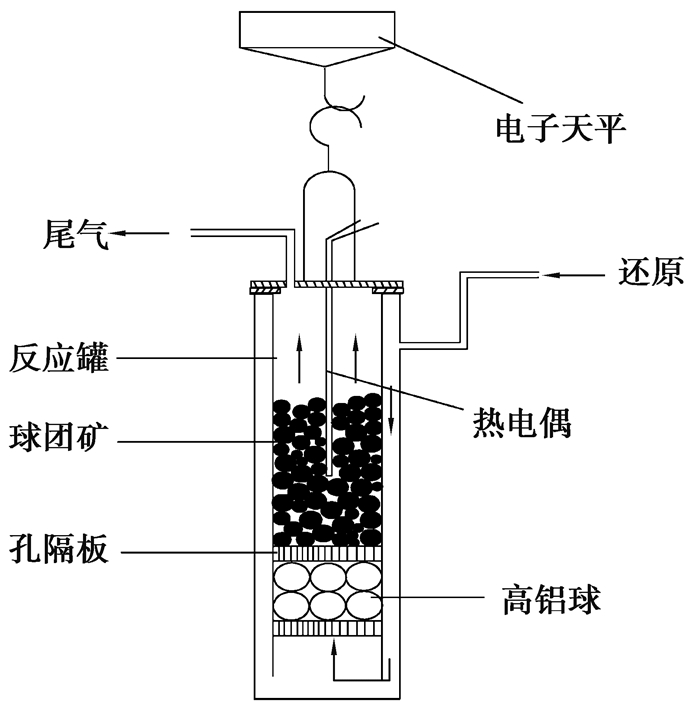
1 实验原料及装置实验中选用的是某钢厂进口球团矿,其成分见表 1。图 1为还原炉及相应装置的示意图,还原炉为三段式控温反应炉。CO的指标纯度为99.5%,H2纯度为99.9%,每次实验球团矿用量约2.0 kg。实验开始时,先通入N2约3 min,在还原炉升温的同时通入还原气,通过改变料层温度停留时间来模拟实际竖炉内的温度变化。还原过程中,电子天平计算失重量,测量达到一定还原度时所需的时间,达到指定还原要求后,改通N2约3 min并降温至室温状态。采用全自动氮吸附仪测定样品气孔状态,结合样品真体积计算得到气孔率。实验过程中,保持气体流量0.627 m3/h,常压操作。
|
图 1 实验装置图 Figure 1 The test device schematic diagram |
| 表 1 球团矿成分及含量 Table 1 Chemical compositions and content of the pellets |
CO还原铁氧化物的化学反应如下:
| $ \left(\text{1/3} \right)\text{F}{{\text{e}}_{\text{2}}}{{\text{O}}_{\text{3}}}\text{+CO=}\left(\text{2/3} \right)\text{Fe+C}{{\text{O}}_{\text{2}}}, $ |
CO还原球团矿石的还原速率,按下面的公式计算[18],mol/(L· min)。
| $ R=\frac{\text{ }\!\!\pi\!\!\text{ }d_{\text{p}}^{2}{{\varphi }^{-1}}N\cdot 273P'\left(x-{{x}^{*}} \right)/22.4t}{\frac{1}{{{k}_{\text{f}}}}+\frac{0.5{{d}_{\text{P}}}\left[{{\left(1-{{f}_{\text{s}}} \right)}^{-1/3}}-1 \right]}{{{D}_{\text{s}}}}+\frac{1}{{{\left(1-{{f}_{\text{s}}} \right)}^{2/3}}k}\text{ }\!\!\times\!\!\text{ }\frac{K}{K+1}}, $ | (1) |
其中,1/kf为还原过程的外扩散阻力;分母中第二项为还原过程的内扩散阻力;相应的第三项为还原过程界面化学反应阻力;Ds为还原铁相的CO内扩散系数,m2/h;P'为床内压力,取P'=1.0×105Pa;k为还原反应的速度常数,m/h;dp为球团矿石粒度,取平均值11 mm;φ为球团矿石形状系数,球团形状接近圆球,取为1;N为单位容积床内球团矿石个数,取N=779 527;t为颗粒温度,K;kf为界膜传质系数,m/h;fs为球团矿还原度,fs=(m0-mt)/m0,m0、mt分别为反应前和反应t时刻球团矿中与铁结合的氧质量;x、x*分别为床内初始时和平衡时CO的物质的量分数,x=1,x*=1/(1+K)。
式(1)中,K为间接还原反应平衡常数,随着还原反应的进行,还原度发生变化,K的表达式也相应发生变化[19]。
t≤575 ℃时
| $ {{f}_{\text{s}}}<0.111, K=\exp \left(4.91+6.235/t \right), \text{F}{{\text{e}}_{\text{2}}}{{\text{O}}_{\text{3}}}\to \text{F}{{\text{e}}_{\text{2}}}{{\text{O}}_{4}}, $ | (2) |
| $ {{f}_{\text{s}}}>0.111, K=\exp \left(-0.7625+543.3/t \right), \text{F}{{\text{e}}_{\text{2}}}{{\text{O}}_{4}}\to \text{Fe}; $ | (3) |
t>575 ℃时
| $ {{f}_{\text{s}}}<0.111, K=\exp \left(4.91+6.235/t \right), \text{F}{{\text{e}}_{\text{2}}}{{\text{O}}_{\text{3}}}\to \text{F}{{\text{e}}_{\text{2}}}{{\text{O}}_{4}}, $ | (4) |
| $ 0.111<{{f}_{\text{s}}}<0.333, K=\exp \left(2.13-2050/t \right), \text{F}{{\text{e}}_{3}}{{\text{O}}_{4}}\to \text{FeO, } $ | (5) |
| $ {{f}_{\text{s}}}>0.333, K=\exp \left(-2.642+2164/t \right), \text{FeO}\to \text{Fe}\text{.} $ | (6) |
其余参数按照下式计算:
| $ k\text{=347exp}\left(-3460/t \right), $ | (7) |
| $ sh=2.0+0.55{{\left(Re \right)}^{1/2}}{{\left(Sc \right)}^{1/3}}, $ | (8) |
| $ {{D}_{s}}=D{{\varepsilon }_{\text{v}}}\xi, $ | (9) |
| $ D=\frac{\left(1\text{ }\!\!\times\!\!\text{ }{{10}^{-3}} \right){{T}^{1.75}}}{P{{\left(v_{\text{A}}^{\frac{\text{1}}{\text{3}}}+v_{\text{B}}^{\frac{\text{1}}{\text{3}}} \right)}^{2}}}\sqrt{\frac{1}{{{M}_{\text{A}}}}+\frac{1}{{{M}_{\text{B}}}}}. $ | (10) |
式中:D为CO与CO2之间的互扩散系数,m2/h;MA、MB为两气体的分子量,g/mol;εv为还原铁相的气孔率,εv=0.53+0.47εp;εp为未还原矿石的气孔率;ξ为还原铁相的迷宫度,ξ=0.238εp+0.04(0.15≤εp≤0.5);υA、υB为两气体的扩散体积,cm3/mol,相应数据见文献[19]。
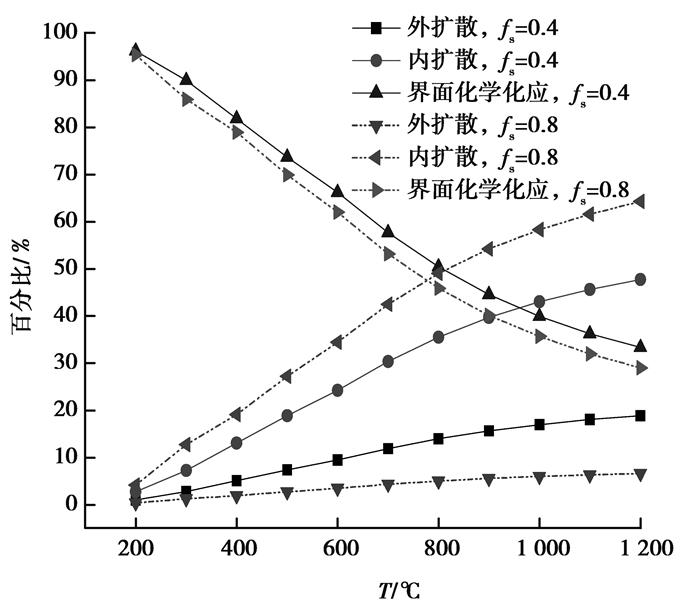
根据式(1)-(10),计算得到不同还原度下外扩散阻力、内扩散阻力及化学反应阻力随温度的变化,如图 2所示。
|
图 2 CO还原时阻力的变化 Figure 2 Resistance changes with CO reducing |
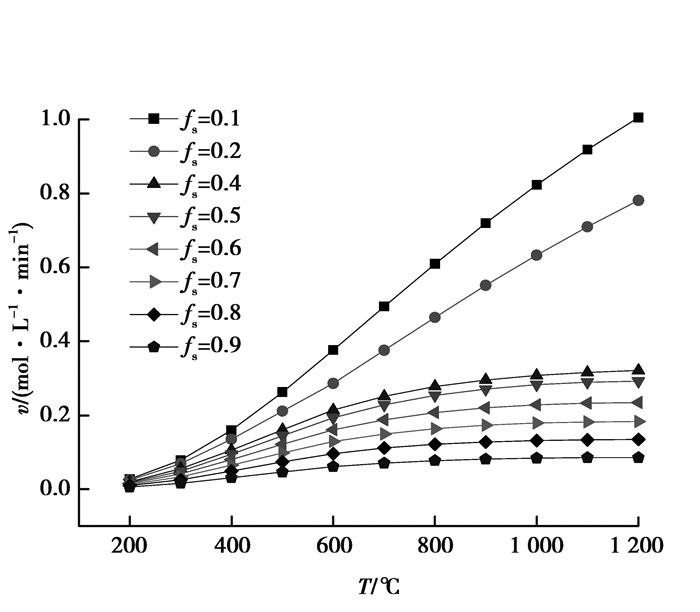
CO还原球团矿时,扩散阻力所占百分比均随温度增大而升高,而界面化学反应阻力所占比例则相应降低。当温度较低时,界面还原反应速率较低,此时,界面化学反应为限制环节;随着温度升高,界面处还原反应速率逐渐增大,其影响相应减小,此时,球团矿中由熔融产物层产生,内扩散阻力增大,该升温还原阶段为界面化学反应和内扩散混合控制;当温度超过800 ℃时,熔融产物逐渐增厚,界面处还原反应速率继续增大,内扩散阻力成为限制环节。结合图 3所示,相同温度条件下,当还原度较小时,还原反应速率较快;fs=0.1及0.2时,反应速率随温度呈现出线性变化,这主要是因为低还原度下,扩散阻力及界面化学反应阻力随温度变化较小。图 2中,随着反应进行,还原度相应增大,反应界面逐渐深入到球团内部,内扩散阻力增加,而外扩散阻力所占比例相应减少,界面化学反应阻力所受影响较小
|
图 3 CO还原时反应速率变化 Figure 3 Reduction rate changes with CO reducing |
H2还原铁氧化物的计算与CO类似,如式(11)所示[18]。
| $ R=\frac{\text{ }\!\!\pi\!\!\text{ }d_{\text{p}}^{2}{{\varphi }^{-1}}N\cdot 273P'\left(\omega -{{\omega }^{*}} \right)/22.4t}{\frac{1}{k{{'}_{\text{f}}}}+\frac{0.5{{d}_{\text{P}}}\left[{{\left(1-{{f}_{\text{s}}} \right)}^{-1/3}}-1 \right]}{D{{'}_{\text{s}}}}+\frac{1}{{{\left(1-{{f}_{\text{s}}} \right)}^{2/3}}k'}\text{ }\!\!\times\!\!\text{ }\frac{K}{K'+1}}, $ | (11) |
其中,
t<575 ℃时
| $ k\text{=102}\text{.78}t\text{exp}\left(-1792.16/t \right), $ | (12) |
| $ K\text{=exp}\left(8.883-2025.48/t \right). $ | (13) |
t>575 ℃时
| $ k\text{=82}\text{.50}t\text{exp}\left(-1840.27/t \right), $ | (14) |
| $ K\text{=exp}\left(1.0837-415.18/t \right). $ | (15) |
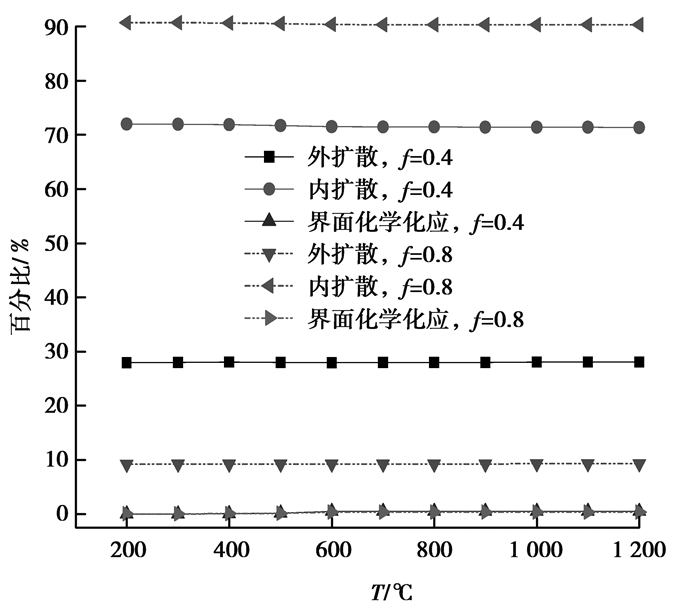
如图 4所示,H2还原铁氧化物时,温度变化对各项阻力几乎没有影响。扩散阻力占绝大部分,界面化学反应阻力所占比例几乎为零。
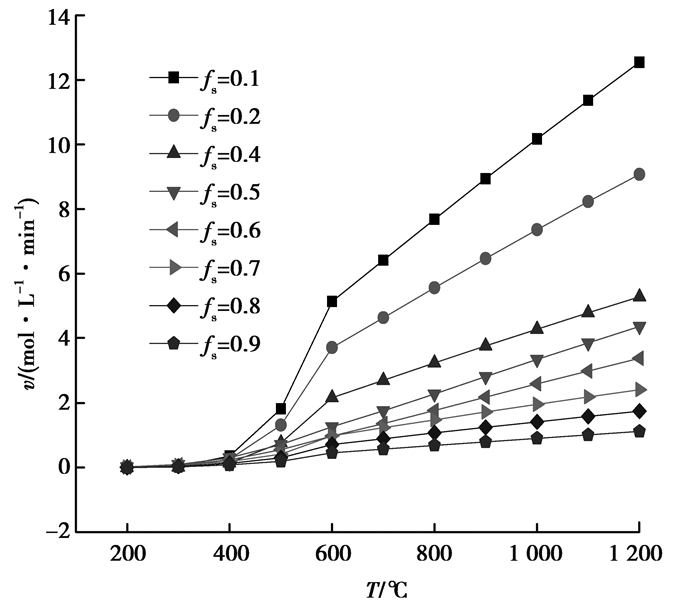
结合图 5,相同温度下,反应速率随还原度增大而降低。还原度增大时,还原所产生的熔融产物增多,内扩散阻力增大,降低了反应速率。温度升高时,界面还原反应速率和扩散速率均增大,使得反应速率增大,特别是还原度较小时,反应速率增大较快。低还原度下,即fs=0.1及0.2时,扩散阻力及界面化学反应阻力随温度变化较小,与CO还原一样,反应速率随温度也表现出线性增加。
|
图 4 H2还原时阻力的变化 Figure 4 Resistance changes with H2 reducing |
|
图 5 H2还原时速率随温度的变化 Figure 5 Reduction rate changes with H2 reducing |
实际生产中,还原气均是CO与H2的混合物,造气方式不同,H2和CO的含量也不同。根据上述计算结果,假设不考虑混合气中CO与H2的交互作用,提出式(16)来计算还原气还原球团矿时的反应速率:
| $ {{R}_{混合}}={{R}_{\text{CO}}}\text{ }\!\!\times\!\!\text{ }\varphi \left(\text{CO} \right)+{{R}_{\text{H2}}}\text{ }\!\!\times\!\!\text{ }\varphi \left({{\text{H}}_{\text{2}}} \right). $ | (16) |
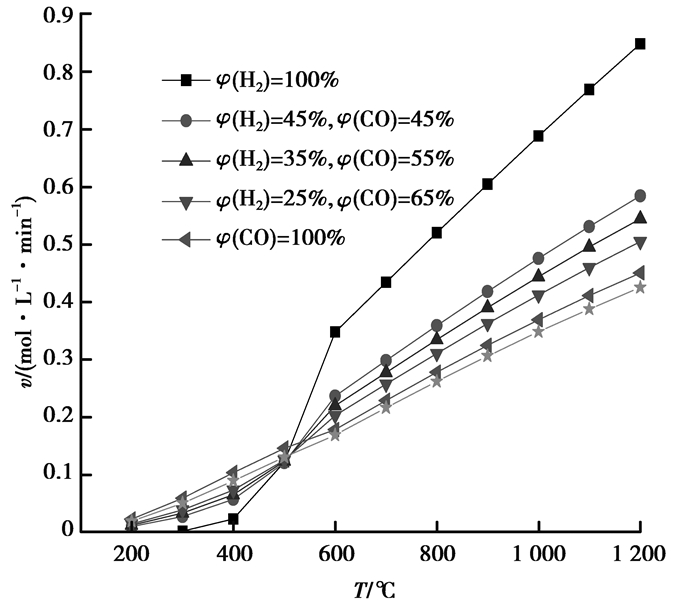
图 6反映了当fs=0.2时,不同氢碳比的还原气还原球团矿时反应速率随温度的变化关系。混合气反应速率均随温度升高而增大,当温度小于500 ℃时,混合气及纯CO还原速率均大于纯H2还原时的速率;当温度大于500 ℃时,采用纯H2还原时的反应速率显著增大,且均大于其余成分的还原速率。同时,随着CO体积分数的增加。H2的体积分数降低,反应速率降低。
|
图 6 不同氢碳比还原时速率变化(fs=0.2) Figure 6 Resistance changes with different H2/CO reducing |
CO还原Fe2O3的反应从141 ℃开始明显发生,而H2还原Fe2O3的反应从280 ℃才开始明显发生,因此,低温时CO的速率要高于H2。CO还原球团矿反应整体上属于放热反应,而H2还原时属于吸热反应,温度较低时,CO体积分数增大,放热增多,有利于增大反应速率,而当温度升高时,此时条件更有利于吸热反应,使得H2体积分数增多时,反应速率增大。同时,高温下H2的扩散系数及其在氧化铁上的吸附能力大于CO,使得反应速率加快。
为验证反应速率模型的准确性,将反应速率模型计算所得理论值与实验值作对比,见表 2。数据结果显示,理论计算模型与实验结果平均误差小于10%,表明利用该模型能够细致研究铁矿石的反应动力学。
| 表 2 计算结果与实验结果对比 Table 2 Comparation of the results between calculation and experiment |
通过分析CO和H2还原球团矿石的速率,提出混合气反应速率模型,研究球团矿还原的反应动力学,得到如下结论:
1) CO还原球团矿时,扩散阻力所占比例随着温度的升高均增大,且内扩散阻力所占比例增大速率明显大于外扩散阻力,界面化学反应阻力所占比例则随着温度升高而降低,温度高于800 ℃时,内扩散成为速率控制环节;内扩散阻力所占比例随还原度增大而升高,外扩散阻力及界面化学反应阻力所占比例随还原度的增大均降低。
2) H2还原球团矿时,内外扩散阻力及界面化学反应阻力所占比例随温度变化不大,内外扩散阻力所占比例较大;内扩散阻力所占比例随还原度的升高而升高,外扩散阻力所占比例相对下降;H2还原球团矿过程中,内扩散属于速率控制环节。
3) CO和H2分别还原球团矿时,反应速率均随着温度的升高而升高,随着还原度的升高而降低,当温度高于750 ℃时,CO还原时反应速率增大已不明显。CO和H2混合气还原球团矿时,反应速率随温度的升高而增大,且温度低于500 ℃时,随着CO体积分数的增加,反应速率降低。理论模型与实验结果能够保持一致,可以采用该模型研究球团矿的反应动力学。
| [1] |
全球直接还原铁产量未来增长潜力巨大[N].世界金属导报, 2013-09-03(FO2). Globle Direct Reduced Iron Production have Great Potential for Future Growth[N].The World Metal Guides, 2013-09-03(FO2).(in Chinese) |
| [2] |
魏国, 赵庆杰, 董文献, 等.
直接还原铁生产概况及发展[J]. 中国冶金, 2004(9): 18–22.
WEI Guo, ZHAO Qingjie, DONG Wenxian, et al. Preseent status and development trends of world direct reduction processes[J]. China Metallurgy, 2004(9): 18–22. (in Chinese) |
| [3] |
徐匡迪.
低碳经济与钢铁工业[J]. 钢铁, 2010, 45(3): 1–12.
XU Kuangdi. Low carbon economy and iron and steel industry[J]. Iron and Steel, 2010, 45(3): 1–12. (in Chinese) |
| [4] | Ta Kao H, Osamu T, Laso K. The development of new iron making processes[J]. KOBELCO Technology Review, 2015(26): 92–97. |
| [5] |
冯燕波, 曹维成, 杨双平, 等.
中国直接还原技术的发展现状及展望[J]. 中国冶金, 2006, 16(5): 10–13.
FENG Yanbo, CHAO Weicheng, YANG Shuangping, et al. Development and prospect on direct reduction technology in china[J]. China Metallurgy, 2006, 16(5): 10–13. (in Chinese) |
| [6] |
唐惠庆, 郭兴敏, 张圣弼, 等.
CO/CO2气氛下含碳球团还原动力学模型及其应用[J]. 钢铁研究学报, 2000, 12(6): 1–6.
TANG Huiqing, GUO minxing, ZHANG Shengbi, et al. Mathematical model for direct reduction of carbon-containing pellet and its application[J]. Journal of Iron and Steel Research, 2000, 12(6): 1–6. (in Chinese) |
| [7] |
庞建明, 郭培民, 赵沛, 等.
低温下氢气还原氧化铁的动力学研究[J]. 钢铁, 2008, 43(7): 7–11.
PANG Jian ming, GUO Pei min, ZHAO Pei, et al. Study on kinetics of hematite reduction by hydrogen at low temperature[J]. Iron and Steel, 2008, 43(7): 7–11. (in Chinese) |
| [8] |
李永全, 周渝生.水煤气条件下球团矿竖炉还原过程研究[C]//中国金属学会2003中国钢铁年会论文集(2), 2003: 281-287. LI Yongquan, ZHOU Yusheng.the study of pellets reduction processes by shaft reduction: china steel annual meeting, beijing, 2003[C]//Chinese society for metals proceedings of 2003 annual meeting of China's iron and steel (2), 2003:281-287.(in Chinese) |
| [9] |
陈庚.气基还原氧化铁动力学机理研究[D].大连:大连理工大学, 2011. CHEN Geng.The kinetics of the gas based reduction of iron oxide[D].Dalian: Dalian University of Technology, 2011.(in Chinese) http://www.oalib.com/references/19416037 |
| [10] |
庞建明, 郭培民, 赵沛, 等.
氢气还原氧化铁动力学的非等温热重方法研究[J]. 钢铁, 2009, 44(2): 11–14.
PANG Jian ming, GUO Peimin, ZHAO Pei, et al. Kinetics of reduction of hematite by h2 using nonisothermal thermogravimetric method[J]. Iron and Steel, 2009, 44(2): 11–14. (in Chinese) |
| [11] |
李向伟, 陈令坤, 王炜.
球团矿富氢还原的动力学研究[J]. 材料与冶金学报, 2013, 12(4): 241–245.
LI Xiangwei, CHEN Lingkun, WANG Wei. Kinetics of rich hydrogen reduction of pellet[J]. Journal of Materials and Metallurgy, 2013, 12(4): 241–245. (in Chinese) |
| [12] | Luo S, Yi C, Zhou Y. Direct reduction of mixed biomass-Fe2O3 briquettes using biomass-generated syngas[J]. Renewable Energy, 2011, 36(12): 3332–3336. DOI:10.1016/j.renene.2011.05.006 |
| [13] | Ribbenhed M, Thorén M, Sternhufvud C. CO2 emission reduction costs for iron ore-based steelmaking in Sweden[J]. Journal of Cleaner Production, 2008, 16(1): 125–134. DOI:10.1016/j.jclepro.2006.11.007 |
| [14] | Kim Y, Worrell E. International comparison of CO2 emission trends in the iron and steel industry[J]. Energy Policy, 2002, 30(10): 827–838. DOI:10.1016/S0301-4215(01)00130-6 |
| [15] |
陈淼, 李家新, 李学付.
高温下不同氢气含量混合气体还原浮氏体的实验研究[J]. 金属材料与冶金工程, 2007, 35(1): 19–22.
CHEN Miao, LI Jiaxin, LI Xuefu. Experiment Study on Wustite Reduction with Compound Gases of Different Hydrogen Content at High Temperature[J]. Metal Materials and Metallurgy Engineering, 2007, 35(1): 19–22. (in Chinese) |
| [16] | Weiss B, Sturn J, Voglsam S, et al. Industrial fluidised bed direct reduction kinetics of hematite ore fines in H2 rich gases at elevated pressure[J]. Chemical Engineering Science, 2011, 66(4): 703–708. DOI:10.1016/j.ces.2010.11.024 |
| [17] | Yi L, Huang Z, Jiang T. Sticking of iron ore pellets during reduction with hydrogen and carbon monoxide mixtures: Behavior and mechanism[J]. Powder Technology, 2013, 235(2): 1001–1007. |
| [18] |
鞭岩, 森山昭, 等. 冶金反应工程学[M]. 北京: 科学出版社, 1981: 281-287.
BIAN Yan, SHEN Shanzhao, et al. Metallurgical Reaction Engineering[M]. Beijing: Science Publishing Company, 1981: 281-287. (in Chinese) |
| [19] |
秦洁.竖炉生产海绵铁过程的还原特性及碳行为研究[D].重庆:重庆大学, 2008. QIN Jie.Study on reductive characteristic and the behavior of carbon during producing sponge iron in shaft furnace[D].Chongqing: Chongqing University, 2008.(in Chinese) http://cdmd.cnki.com.cn/Article/CDMD-10611-2009049626.htm |
 2015, Vol. 38
2015, Vol. 38

