过氧化氢(H2O2)是参与环境和生物过程中的一种重要化合物[1]。因具有氧化漂白、高效杀菌和易分解等特点,H2O2被广泛用于食品和工业生产中。但超量或非法添加H2O2,易导致环境污染。已证明H2O2是环境中氧化SO2生成H2SO4最为有效的氧化剂,而形成的H2SO4是引起酸雨的主要原因,这是全球严重的环境问题[2]。因此,检测雨水中H2O2的含量可为环境信息提供重要的指标。
已有多种测定H2O2的方法报道,包括滴定分析法[3]、荧光分析法[4-5]、分光光度法[6-7]、电化学法[8]等。这些方法各有优点,但存在着选择性差和灵敏度低等不足。化学发光法具有灵敏度高、线性范围宽、仪器设
备简单、操作方便和分析快速等优点,并已得到了广泛研究与应用[9-11]。
纳米材料由于具有特殊的物理和化学性质被广泛应用于各个领域中。近年来,纳米材料也被应用于化学发光分析中,被用来开发各种新型的高灵敏、高选择性的检测方法和器件[12-13]。ZnO NPs是一种n型半导体化合物,表现出很好的光催化活性,具有制备简单、价格便宜和形貌易控制等优点,已被广泛应用于光催化[14-15]、工业催化[16]、气体传感器[17]和太阳能电池[18]等中。Li等[19]发现ZnONPs促进Luminol-H2O2化学发光现象,并研究了ZnO纳米粒径大小对Luminol-H2O2发光的影响。笔者在前人研究的基础上,系统研究了该方法的分析特性和影响因素,并结合流动注射技术,建立了流动注射化学发光分析方法,并应用于雨水中微量H2O2含量的测定。该方法具有简单、快速、灵敏度高、线性范围宽及重现性好等特点。
1、 实验部分 (1.1) 仪器与试剂IFFM-E型流动注射化学发光分析仪(西安瑞迈分析仪器有限公司);UV-2450紫外-可见分光光度计(日本SHIMADZU公司);电子天平(日本SHIMADZU公司);数显恒温磁力搅拌器(金坛市双捷实验仪器厂);高速冷冻离心机GL-16A(上海菲洽尔分析仪器有限公司);KQ-100B型超声波清洗器(昆山市超声仪器有限公司);DELTA320 pH计(梅特勒托利多仪器有限公司);艾柯DZG-303A纯水制备仪(成都唐氏康宁科技发展有限公司);ZEISS Libra200透射电镜(德国ZEISS公司)。
Luminol(Aladdin公司);甲醇(分析纯,重庆川东化工有限公司);EDTA、Na2CO3、NaHCO3、Zn(CH3COO)2·2H2O和NaOH(分析纯,成都市科龙化工试剂厂);实验用水为去离子水。
(1.2) 标准溶液的配制准确称取0.442 9 g luminol,用0.1 mol/L NaOH溶液溶解,并定容至250 mL棕色容量瓶中,配制成10 mmol/L鲁米诺储备液,在4 ℃下避光保存,放置7 d后使用。根据需要,用0.1 mol/L Na2CO3-NaHCO3(pH 9.83)缓冲溶液稀释成所需浓度,即配即用。
(1.3) ZnO纳米颗粒(ZnO NPs)的制备参照文献[20]制备ZnO NPs:称取3.2927 g Zn(CH3COO)2·2H2O(0.03 mol),溶于100 mL的甲醇溶液。在室温常压下,超声10 min,得到澄清透明的溶液。将溶液转移到圆底烧瓶中,在反应温度60 ℃下回流,用磁力搅拌器不断搅拌,反应24 h,反应结束后冷却到室温。转速为1 300 r/min离心分离10 min。先用甲醇洗涤除去副产物,然后用水洗涤甲醇,得到单相ZnO NPs。重复实验,制备一定量的ZnO NPs。电镜分析结果表明,制备的ZnO NPs形状为球形,粒径为36 nm。
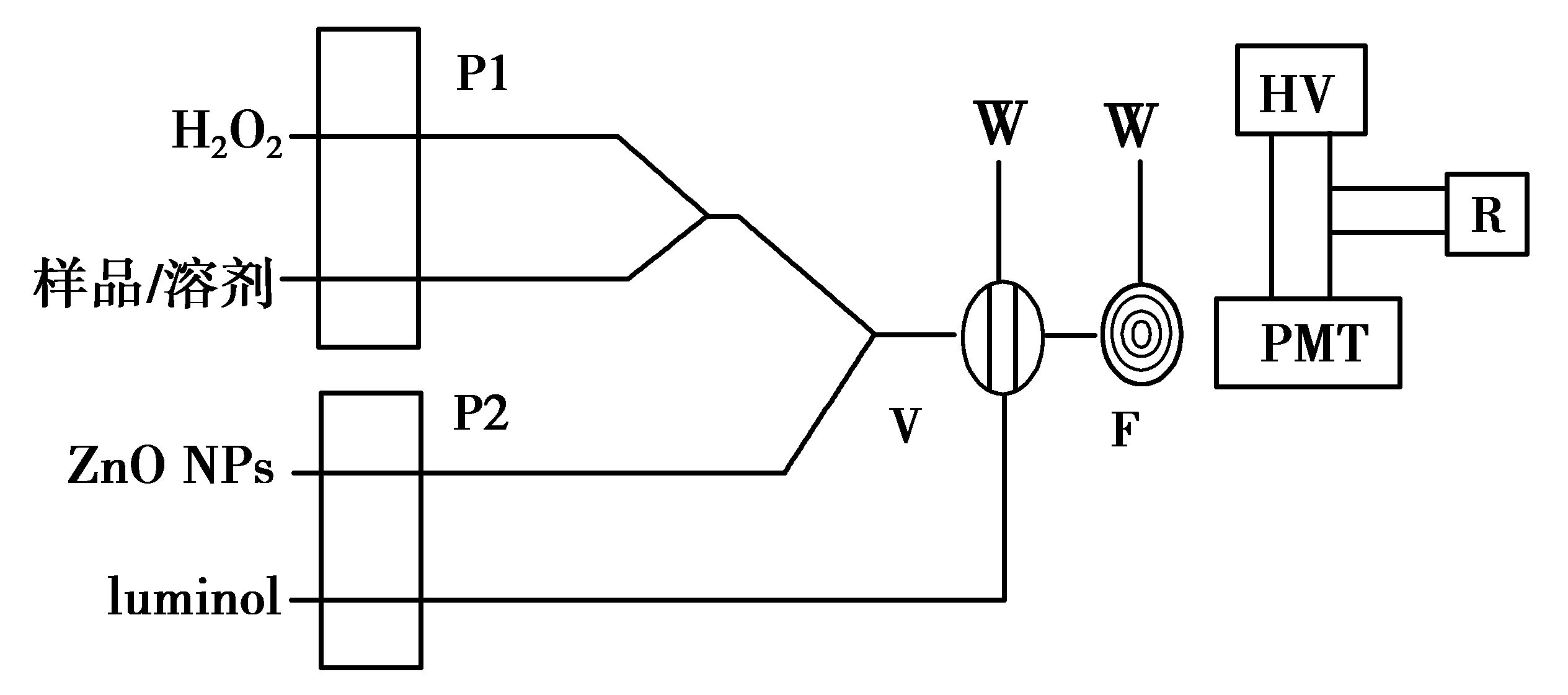
(1.4) 化学发光的测定采用图 1所示流路研究luminol-ZnO NPs-H2O2的化学发光。实验条件:luminol浓度为0.10 mmol/L;luminol溶液pH为9.83;ZnO NPs质量浓度为0.10 g/L;H2O2浓度为0.10 mmol/L;蠕动泵转速为20 r/min。
|
图 1 化学发光流路图 Figure 1 Diagram of flow injection CL system |
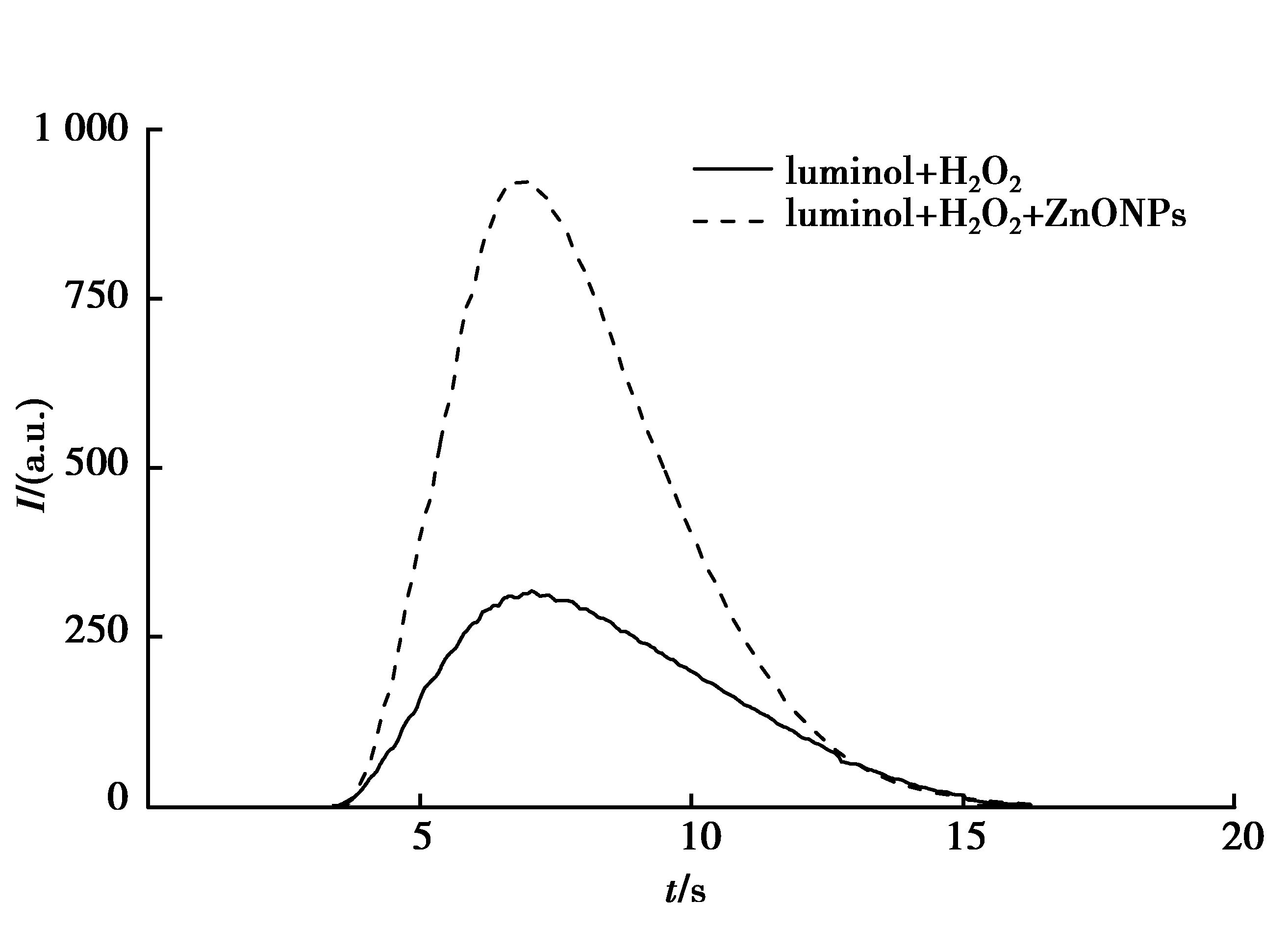
考察在luminol-H2O2体系中添加ZnO NPs后的影响,结果如图 2所示。在没有ZnO NPs存在的条件下,luminol-H2O2有微弱的化学发光。ZnO NPS是一种半导体材料,在光照条件下,当一个具有超过半导体的隙带能量的光子射入ZnO NPs,一个电子从价带被激发到导带,其后留下了一个空穴。被激发到导带上的电子容易被溶解在溶液中的氧气捕获,生成超氧阴离子自由基(O2·—),O2·—经过一系列过程可快速转变为羟基自由基(·OH)[21]。同时价带的空隙把周围环境中的羟基变成·OH。因此,加入的ZnO NPs可催化分解H2O2产生一些活性中间产物如·OH和O2·—[22-23],而这些自由基与luminol反应生成luminol自由基。Luminol自由基和·OH反应,从而增强化学发光,其增强倍数大约为3倍。ZnO NPs的加入,增强了luminol-H2O2化学发光,放大发光信号,提高灵敏度。
|
图 2 ZnO NPs对luminol-H2O2化学发光的影响 Figure 2 Enhancement of luminol-H2O2 CL by ZnO NPs |
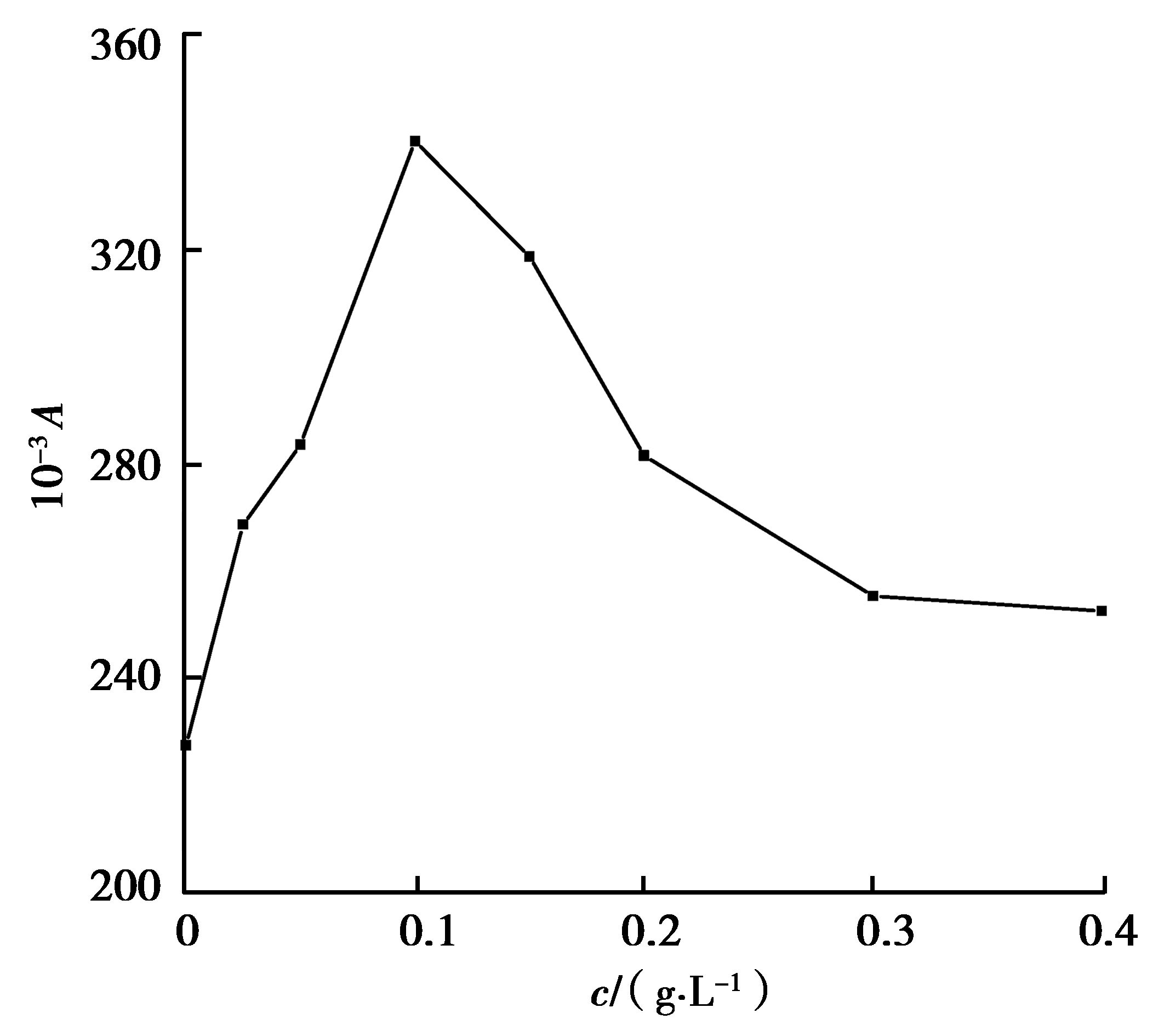
考察ZnO NPs质量浓度对化学发光的影响,其结果如图 3所示。ZnO NPs质量浓度在0.025~0.10 g/L时,化学发光峰面积(A)随ZnO NPs质量浓度增加而增加,当质量浓度达到0.10 g/L时,峰面积达到最大;当ZnO NPs质量浓度大于0.10 g/L时,该体系化学发光的峰面积随着ZnO NPs质量浓度的增大而减小。可能的原因是ZnO NPs质量浓度的增大而发生聚集降低光催化性能,从而影响产生自由基的速率[24]。当ZnO NPs发生聚集时,质量传递和遮蔽效应可能也会降低自由基的生成,纳米粒子表面活性理论也表明活性表面对纳米颗粒的反应速率起着重要的作用[25]。后续研究选择ZnO NPs质量浓度为0.10 g/L。
|
图 3 ZnO NPs质量浓度对化学发光的影响 Figure 3 Effect of the mass concentration of ZnONPs solution on CL |
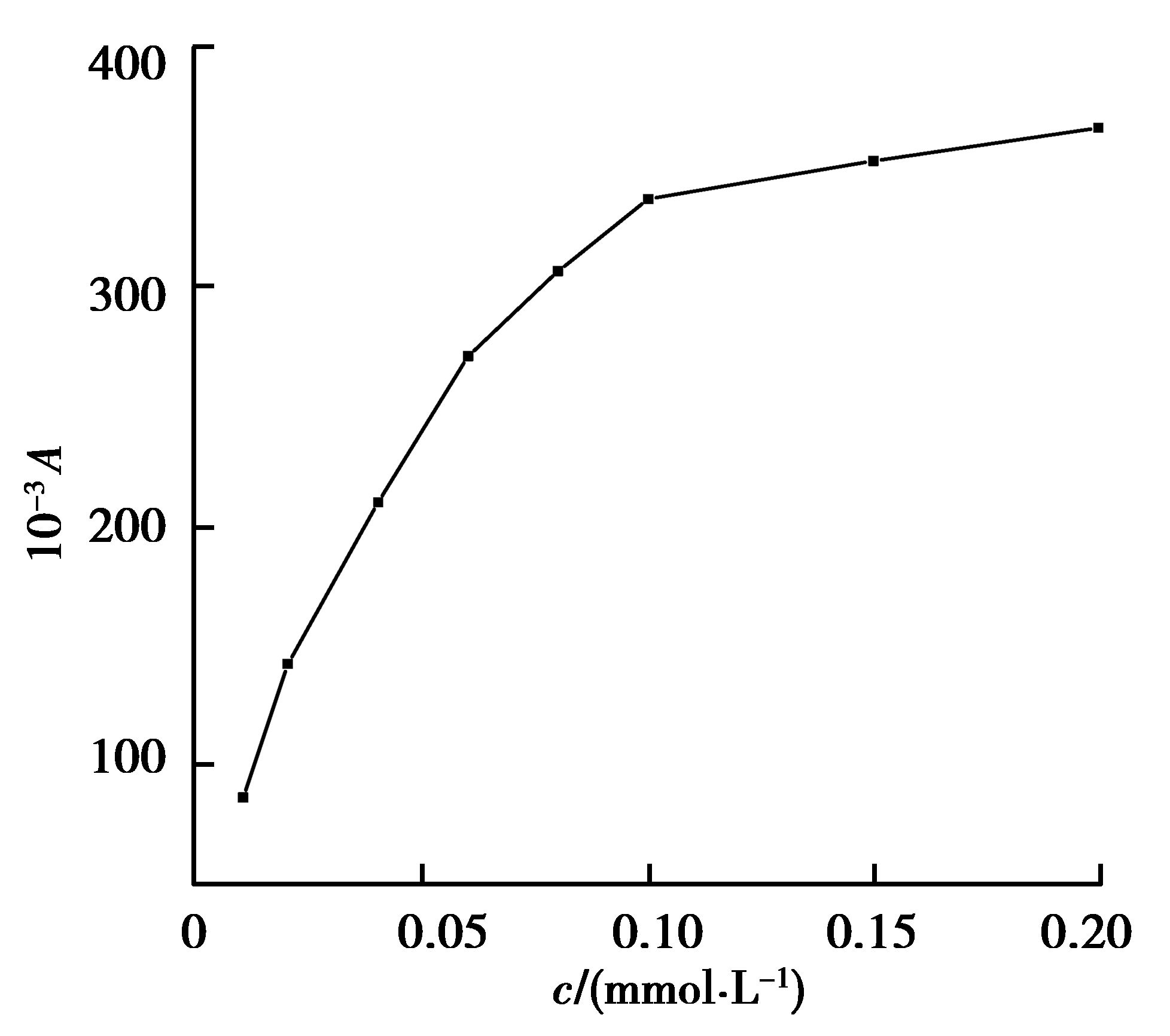
Luminol浓度会影响化学发光,结果如图 4所示。当luminol浓度范围在0.01~0.10 mmol/L时,化学发光峰面积随着luminol浓度增加而增大,当luminol浓度大于0.10 mmol/L时,化学发光峰面积增加不明显,趋于平衡。后续研究采用luminol的浓度为0.10 mmol/L。
|
图 4 luminol浓度对化学发光的影响 Figure 4 Effect of the concentration of luminol solution on CL |
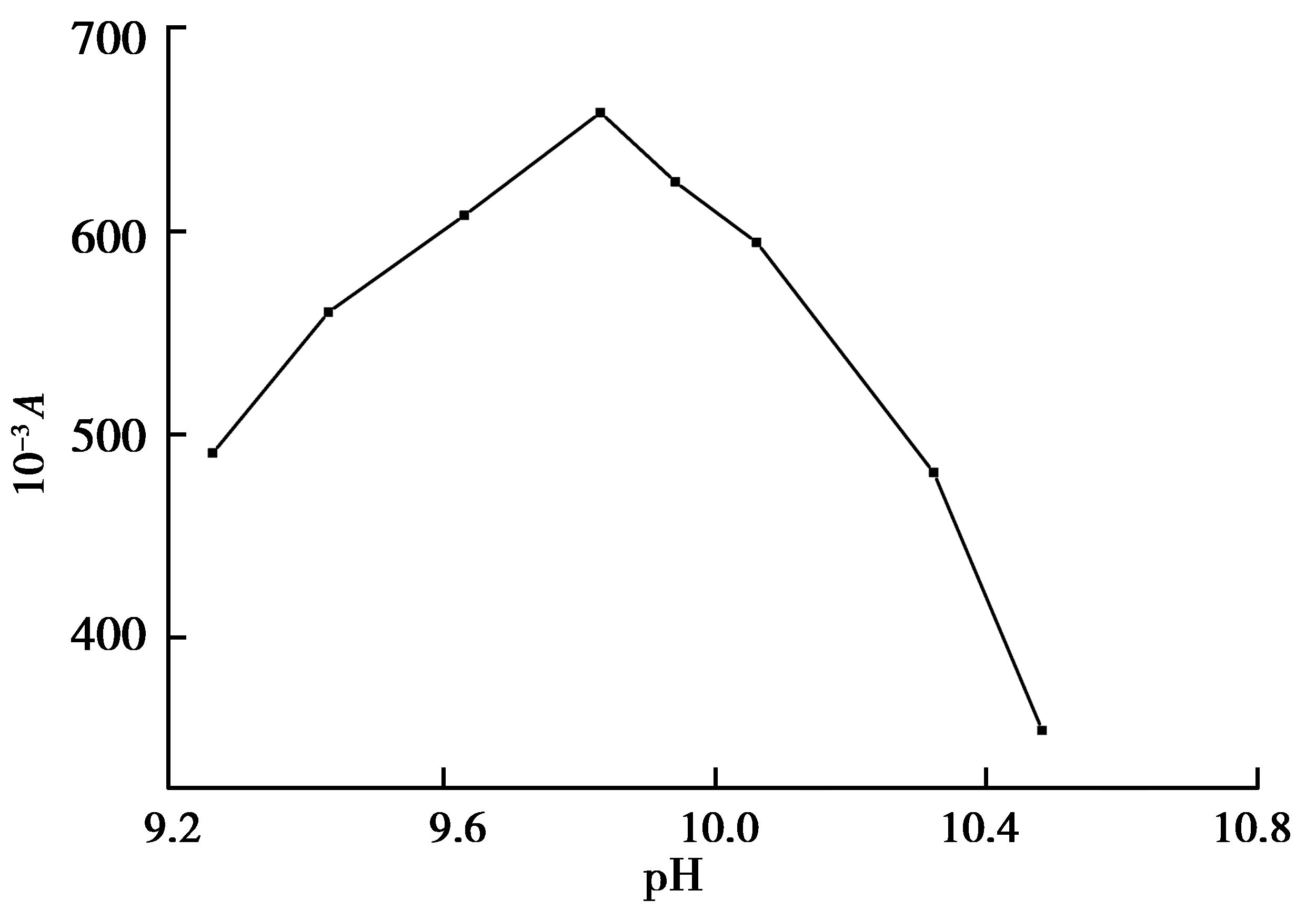
考察luminol溶液pH对化学发光的影响,结果如图 5所示。当luminol溶液pH范围在9.26~9.83时,发光峰面积随着pH的增加而增加,达到9.83时,峰面积达到最大值。当luminol溶液pH大于9.83后,发光峰面积不断下降。luminol在酸性溶液中反应活性很低,在碱性条件下反应活性高,因此luminol溶液pH值在9.26~9.83范围内对luminol的发光具有很大的影响[26]。后续研究采用luminol溶液pH值为9.83。
|
图 5 luminol溶液pH对化学发光的影响 Figure 5 Effect of the pH of luminol solution on CL |
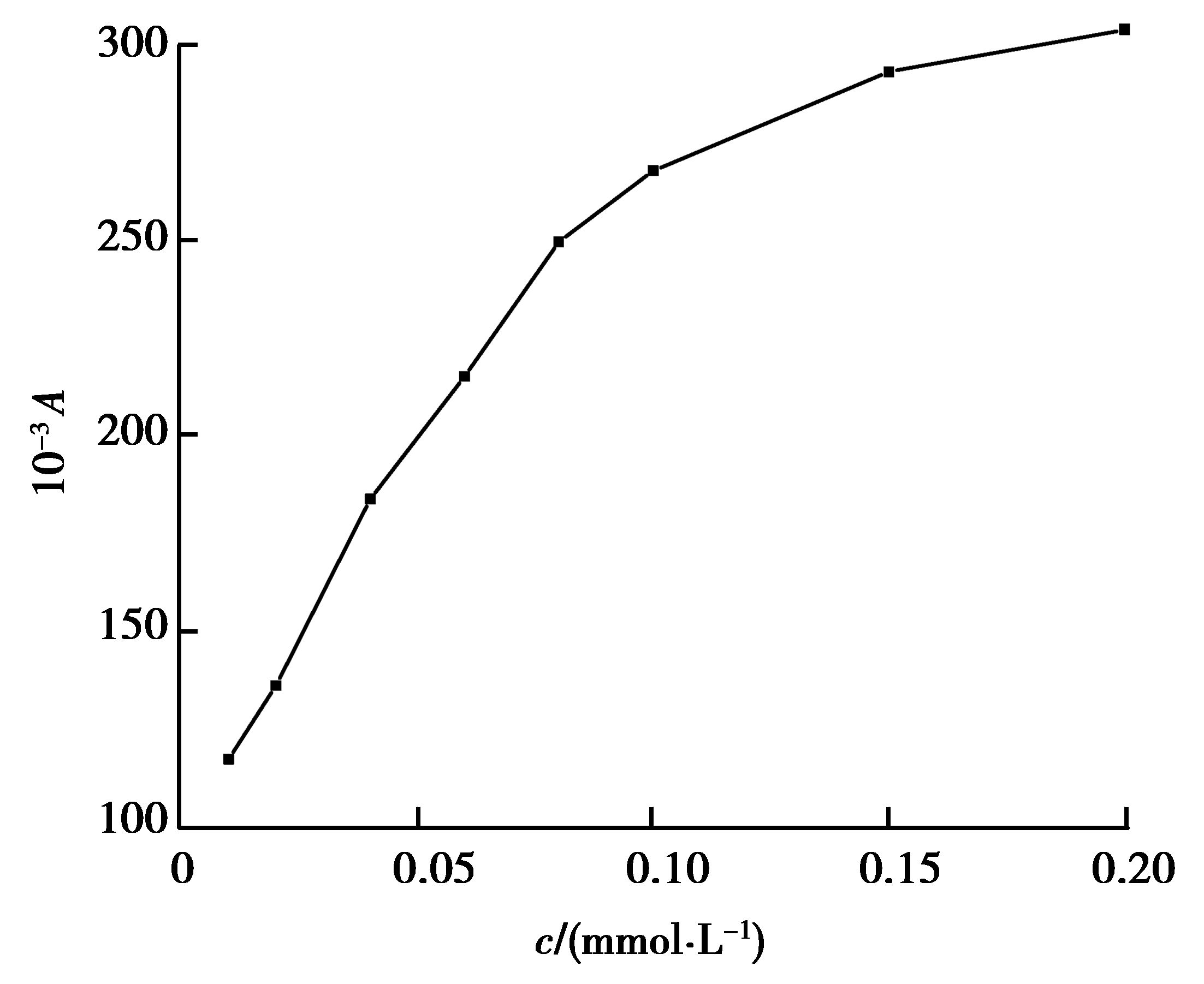
H2O2浓度对luminol-ZnO NPs-H2O2体系化学发光的影响如图 6所示。当 H2O2浓度范围在0.01~0.10 mmol/L时,化学发光峰面积随着H2O2浓度的增加而增加,当H2O2浓度大于0.10 mmol/L后,峰面积增加不明显,趋于平衡。后续研究采用的H2O2浓度为0.1 mmol/L。
|
图 6 H2O2浓度对化学发光的影响 Figure 6 Effect of the concentration of H2O2 solution on CL |
根据优化条件:ZnO NPs质量浓度为0.10 mg/L;luminol浓度为0.10 mmol/L;luminol溶液pH为9.83,测定雨水中H2O2的浓度。实验得到H2O2的浓度在0.06~20 μmol/L范围内,H2O2浓度的对数(lgc)和化学发光峰面积的对数(lg A)具有良好的线性关系,线性关系为lg A=0.751 6lg c+8.719 2(r2=0.995 9,n=11)。根据IUPAC(3σ)规定,计算方法的检出限(LOD)为0.016 μmol/L。平行测定浓度为0.4 μmol/L的H2O2标准溶液11次,其相对标准偏差为2.41%。与采用其他方法测定H2O2含量的文献相比(如表 1),本实验方法能够获得较低的检测限和较宽的线性范围。
| 表 1 其他方法测定H2O2分析参数比较 Table 1 Comparison analysis parameter of this work with some established methods for H2O2 |
为了检查该实验方法的选择性,选择雨水中可能含有的干扰离子,在选定的实验条件下,以浓度为0.4 μmol/L的H2O2进行干扰实验,以相对误差±5%作为干扰水平上限。结果如表 2所示,从表中可以得到除Fe3+以外,其他离子均无明显的干扰,加入适量的NaF可以消除Fe3+的干扰。
| 表 2 干扰离子的影响 Table 2 Effect of coexisting ion |
收集得到不同时间的雨水,过滤后,用标准加入法测定雨水中H2O2的含量,同时对样品进行回收率测定,回收率在95% ~ 102%之间,其结果如表 3所示。
| 表 3 雨水中H2O2的测定结果 Table 3 Resuts of analysis of hydrogen peroxide in rainwater |
笔者基于ZnO NPs能够增强luminol-H2O2化学发光,建立了luminol-ZnO NPs-H2O2流动注射化学发光体系。应用此方法测定雨水中微量H2O2,得到了比较满意的结果。H2O2浓度在0.06~20 μmol/L范围内,H2O2的lg c和lg A具有良好的线性关系,LOD为0.016 μmol/L(3σ),回收率为95%~102%,RSD(n=11)为2.41%。与其他方法相比,此方法具有简便、快速、灵敏、线性范围宽、重现性好等特点。
| [1] |
Wang C L, Mulchandani A.
Ferrocene-conjugated polyaniline-modified enzyme electrodes for determination of peroxides in organic media[J]. Analytical Chemistry , 1995, 67 (6) : 1109–1114.
DOI:10.1021/ac00102a014 ( 0) 0)
|
| [2] |
Sakugawa H, Kaplan I R, Tsai W T, et al.
Atmospheric hydrogen-peroxide[J]. Environmental Science & Technology , 1990, 24 (10) : 1452–1462.
( 0) 0)
|
| [3] |
Klassen N V, Marchington D, Mcgowan H C E.
H2O2 Determination by the I3-Method and by KMnO4 Titration[J]. Analytical Chemistry , 1994, 66 (18) : 2921–2925.
DOI:10.1021/ac00090a020 ( 0) 0)
|
| [4] |
Li J, Dasgupta P K, Tarver G A.
Pulsed excitation source multiplexed fluorometry for the simultaneous measurement of multiple analytes.Continuous measurement of atmospheric hydrogen peroxide and methyl hydroperoxide[J]. Analytical Chemistry , 2003, 75 (5) : 1203–1210.
DOI:10.1021/ac026234d ( 0) 0)
|
| [5] |
Xu C, Zhang Z.
Fluorescence determination of hydrogen peroxide using hemoglobin as a mimetic enzyme of peroxidase[J]. Analytical Sciences , 2001, 17 (12) : 1449–1451.
DOI:10.2116/analsci.17.1449 ( 0) 0)
|
| [6] |
Luo W, Abbas M E, Zhu L, et al.
Rapid quantitative determination of hydrogen peroxide by oxidation decolorization of methyl orange using a Fenton reaction system[J]. Analytica Chimica Acta , 2008, 629 (1-2) : 1–5.
DOI:10.1016/j.aca.2008.09.009 ( 0) 0)
|
| [7] |
Chang Q, Deng K J, Zhu L H, et al.
Determination of hydrogen peroxide with the aid of peroxidase-like Fe3O4 magnetic nanoparticles as the catalyst[J]. Microchimica Acta , 2009, 165 (3/4) : 299–305.
( 0) 0)
|
| [8] |
Upadhyay A K, Ting T W, Chen S M.
Amperometric biosensor for hydrogen peroxide based on coimmobilized horseradish peroxidase and methylene green in ormosils matrix with multiwalled carbon nanotubes[J]. Talanta , 2009, 79 (1) : 38–45.
DOI:10.1016/j.talanta.2009.03.010 ( 0) 0)
|
| [9] |
Qin W.
Flow injection chemiluminescence-based chemical sensors[J]. Analytical Letters , 2002, 35 (14) : 2207–2220.
DOI:10.1081/AL-120015008 ( 0) 0)
|
| [10] |
Su Y Y, Chen H, Wang Z M, et al.
Recent advances in chemiluminescence[J]. Applied Spectroscopy Reviews , 2007, 42 (2) : 139–176.
DOI:10.1080/05704920601184275 ( 0) 0)
|
| [11] |
Zhang L J, Chen Y C, Zhang Z M, et al.
Highly selective sensing of hydrogen peroxide based on cobalt-ethylenediaminetetraacetate complex intercalated layered double hydroxide-enhanced luminol chemiluminescence[J]. Sensors and Actuators B:Chemical , 2014, 193 : 752–758.
DOI:10.1016/j.snb.2013.12.036 ( 0) 0)
|
| [12] |
Su Y Y, Xie Y, Hou X D, et al.
Recent advances in analytical applications of nanomaterials in liquid-phase chemiluminescence[J]. Applied Spectroscopy Reviews , 2014, 49 (3) : 201–232.
DOI:10.1080/05704928.2013.819514 ( 0) 0)
|
| [13] |
Giokas D L, Vlessidis A G, Tsogas G Z, et al.
Nanoparticle-assisted chemiluminescence and its applications in analytical chemistry[J]. Trac Trends in Analytical Chemistry , 2010, 29 (10) : 1113–1126.
DOI:10.1016/j.trac.2010.07.001 ( 0) 0)
|
| [14] |
Stroyuk A L, Granchak V M, Korzhak A V, et al.
Photoinitiation of buthylmethacrylate polymerization by colloidal semiconductor nanoparticles[J]. Journal of Photochemistry and Photobiology A:Chemistry , 2004, 162 (2/3) : 339–351.
( 0) 0)
|
| [15] |
Sydorov D, Smertenko P, Piryatinski Y, et al.
Electrochemically assembled planar hybrid poly (3-methylthiophene)/ZnO nanostructured composites[J]. Electrochimica Acta , 2012, 81 : 83–89.
DOI:10.1016/j.electacta.2012.07.076 ( 0) 0)
|
| [16] |
Moezzi A, McDonagh A M, Cortie M B.
Zinc oxide particles:Synthesis,properties and applications[J]. Chemical Engineering Journal , 2012, 185/186 : 1–22.
DOI:10.1016/j.cej.2012.01.076 ( 0) 0)
|
| [17] |
Karimi M, Saydi J, Mahmoodi M, et al.
A comparative study on ethanol gas sensing properties of ZnO and Zn0.94Cd0.06O nanoparticles[J]. Journal of Physics and Chemistry of Solids , 2013, 74 (10) : 1392–1398.
DOI:10.1016/j.jpcs.2013.04.020 ( 0) 0)
|
| [18] |
Guérin V M, Rathousky J, Pauporté T.
Electrochemical design of ZnO hierarchical structures for dye-sensitized solar cells[J]. Solar Energy Materials and Solar Cells , 2012, 102 : 8–14.
DOI:10.1016/j.solmat.2011.11.046 ( 0) 0)
|
| [19] |
Li S F, Zhang X M, Du W X, et al.
Chemiluminescence Reactions of a Luminol System Catalyzed by ZnO Nanoparticles[J]. Journal of Physical Chemistry C , 2009, 113 (3) : 1046–1051.
DOI:10.1021/jp808312j ( 0) 0)
|
| [20] |
Hosono E, Fujihara S, Kimura T, et al.
Non-basic solution routes to prepare ZnO nanoparticles[J]. Journal of Sol-Gel Science and Technology , 2004, 29 (2) : 71–79.
DOI:10.1023/B:JSST.0000023008.14883.1e ( 0) 0)
|
| [21] |
Lawrence G D, Mavi A, Meral K.
Promotion by phosphate of Fe (Ⅲ)-and Cu (Ⅱ)-catalyzed autoxidation of fructose[J]. Carbohydrate Research , 2008, 343 (4) : 626–635.
DOI:10.1016/j.carres.2007.12.016 ( 0) 0)
|
| [22] |
Biparva P, Abedirad S M, Kazemi S Y.
ZnO nanoparticles as an oxidase mimic-mediated flow-injection chemiluminescence system for sensitive determination of carvedilol[J]. Talanta , 2014, 130 : 116–121.
DOI:10.1016/j.talanta.2014.06.036 ( 0) 0)
|
| [23] |
Li S F, Zhang X M, Du W X, et al.
Chemiluminescence Reactions of a Luminol System Catalyzed by ZnO Nanoparticles[J]. Journal of Physical Chemistry C , 2009, 113 (3) : 1046–1051.
DOI:10.1021/jp808312j ( 0) 0)
|
| [24] |
Buxton G V, Greenstock C L, Helman W P, et al.
Critical-review of rate constants for reactions of hydrated electrons,hydorogen-atoms and hydroxyl radicals (.OH/.OH) in aqueous-solution[J]. Journal of Physical and Chemical Reference Data , 1988, 17 (2) : 513–886.
DOI:10.1063/1.555805 ( 0) 0)
|
| [25] |
Hotze E M, Bottero J Y, Wiesner M R.
Theoretical Framework for Nanoparticle Reactivity as a Function of Aggregation State[J]. Langmuir:the Acs Journal of Surfaces & Colloids , 2010, 26 (13) : 11170–11175.
( 0) 0)
|
| [26] |
Xu H, Su K H, Che W R, et al.
Theoretical study on the chemiluminescence mechanisms of luminol-DMSO-NaOH system[J]. Acta Chimica Sinica , 2006, 64 (19) : 1981–1987.
( 0) 0)
|
| [27] |
Hanaoka S, Lin J M, Yamada M.
Chemiluminescent flow sensor for H2O2 based on the decomposition of H2O2 catalyzed by cobalt (Ⅱ)-ethanolamine complex immobilized on resin[J]. Analytica Chimica Acta , 2001, 426 (1) : 57–64.
DOI:10.1016/S0003-2670(00)01181-8 ( 0) 0)
|
| [28] |
徐金荣, 陈忠明.
高效液相色谱-荧光检测法测定环境样品中的过氧化物[J]. 色谱 , 2005, 23 (4) : 366–369.
XU Jinrong, CHEN Zhongming.
Determination of peroxides in environmental samples by high performance liquid chromatography with fluorescence detection[J]. Chinese Journal of Chromatography , 2005, 23 (4) : 366–369.
( 0) 0)
|
 2016, Vol. 39
2016, Vol. 39

