镍是生产不锈钢、耐热钢、耐蚀钢及镍基合金等材料的重要合金元素[1-3]。自然界的镍资源主要分为硫化镍矿和氧化镍矿(即红土镍矿)两大类[4],由于硫化镍矿含镍品位高,容易开采,且提炼工艺简单,因此近几十年来,硫化镍矿首先被大量开发利用。但随着全球镍需求量的不断增加,而可供开采的硫化镍矿逐渐枯竭。因此,红土镍矿逐渐成为生产镍产品的重要来源[5-6]。除了湿法提取工艺外[7-8],目前,国内外主要采用火法冶炼工艺从红土镍矿中提取镍。火法冶炼主要分为两类:一类是还原硫化法生产含铁的镍锍,而另一类则根据红土镍矿的铁、镍品位采用不同的工艺生产含镍铁水,如对含铁量高的低品位红土镍矿采用高炉还原法,对含铁量低的中高品位红土镍矿则采用回转窑或隧道窑直接还原-电炉熔分的方法生产含镍铁水[3, 4, 7]。针对印尼高硅高镁中低品位红土镍矿,基于煤基自还原-细磨-磁选工艺制备镍铁,研究CaF2对红土镍矿自还原过程中含镍金属相的析出与聚集长大行为、金属元素回收率和产品镍含量的影响,为高效利用红土镍矿生产镍铁工艺的开发提供指导。
1 实验研究方法 1.1 原料物理化学性质实验所用红土镍矿来自印尼苏拉威西岛Pomalaa矿区,将原矿在110℃下烘干后用颚式破碎机初破,再用球磨机细磨至-0.125 mm。表 1为红土镍矿化学成分,含镍量为1.4%,铁含量16.18%,主要脉石成分为MgO和SiO2,是一种典型的中低品位红土镍矿。
| 表 1 原材料化学成分/% Table 1 Chemical compositions of the raw material/% |
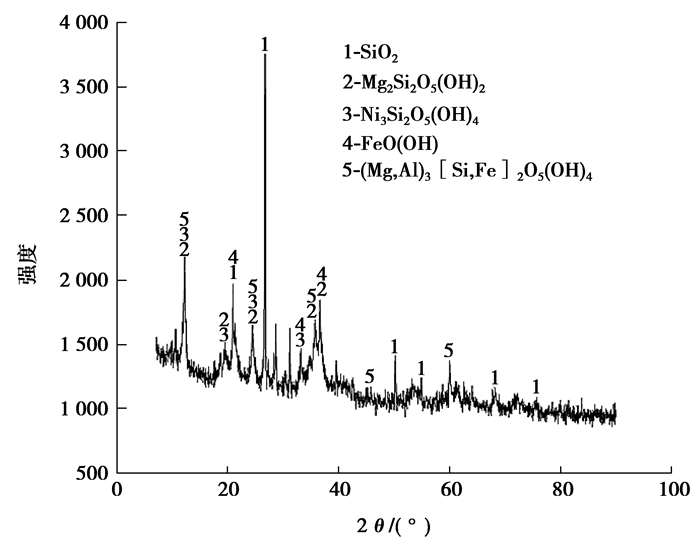
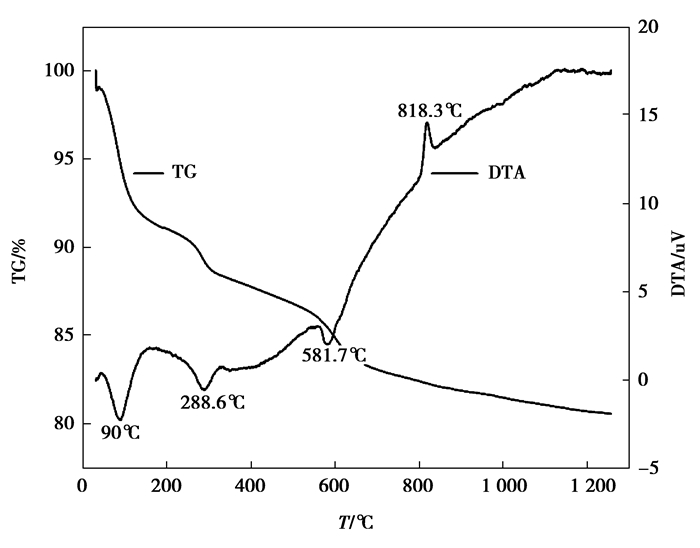
对该红土镍矿进行XRD分析(见图 1),可以看出矿物组成主要为含羟基的硅酸盐类和氧化物类矿物,主要有SiO2(石英)、Mg3Si2O5(OH)4(叶蛇纹石),Ni3Si2O5(OH)4(绿泥石),FeO(OH)(针铁矿),(Mg, Al)3[(Si, Fe)2O5](OH)4(利蛇纹石),镍主要存在于绿泥石中。通过对红土镍矿的热重-差热(TG-DTA)分析(见图 2)可知,红土镍矿在90 ℃的吸热谷表明游离水的脱除,288.6 ℃的吸热谷对应于针铁矿分解成赤铁矿,581.7 ℃的吸热谷为蛇纹石和绿泥石中的羟基水分解脱除所致,蛇纹石脱除羟基后生成的无定型Mg2SiO4在818.3 ℃时结晶变为镁橄榄石时形成放热峰。
|
图 1 红土镍矿X射线衍射图谱 Figure 1 XRD patterns of laterite nickel ore |
|
图 2 红土镍矿TG-DTA曲线 Figure 2 TG-DTA curve of laterite nickel ore |
本研究使用无烟煤作还原剂,粒度为-0.125 mm,化学成分见表 1。内配碳比以无烟煤中碳原子与红土镍矿中铁、镍氧化物所含的氧原子之比表示;混合料中添加一定量的CaF2(分析纯)为熔剂,研究其对还原过程中强化金属相形成的作用。
1.2 实验方法将红土镍矿、无烟煤和CaF2按比例混匀后,添加适量的水润湿,将混合料压成ϕ20 mm×30 mm的圆柱型试样,在110 ℃烘干后备用。由于红土镍矿本身有很好的粘结性能,因此,无需外加粘结剂来提高试样强度。
实验所用还原装置为一台功率为25 kW高温碳管炉,试样在氮气保护下以130~150 ℃/min随炉升温至指定温度后恒温还原15 min,然后随炉冷却至500 ℃取出坩埚,在空气中冷却至室温。还原后的试样经称重、细磨(-0.074 mm)和缩分,其中一部分用于化学分析检测试样中镍、铁含量,另一部分取30 g左右加20倍水调成矿浆后用包有塑料膜的磁铁将带磁性的金属颗粒从矿浆中尽可能分离出来,烘干后称重并分析其铁、镍含量,通过公式(1)和(2)分别计算出金属铁和镍的回收率。
| $ {\mathit{\eta }_{{\rm{Fe}}}}{\rm{ = }}\frac{{{\mathit{m}_{\rm{2}}}{\rm{\cdot}}\mathit{w}{{{\rm{(Fe)}}}_{\rm{2}}}}}{{{\mathit{m}_{\rm{1}}}{\rm{\cdot}}\mathit{w}{{{\rm{(Fe)}}}_{\rm{1}}}}}{\rm{ \times 100\%, }} $ | (1) |
| $ {\mathit{\eta }_{{\rm{Ni}}}}{\rm{ = }}\frac{{{\mathit{m}_{\rm{2}}}{\rm{\cdot}}\mathit{w}{{{\rm{(Ni)}}}_{\rm{2}}}}}{{{\mathit{m}_{\rm{1}}}{\rm{\cdot}}\mathit{w}{{{\rm{(Ni)}}}_{\rm{1}}}}}{\rm{ \times 100\% }}, $ | (2) |
式中:ηFe和ηNi分别为铁和镍的回收率(%); m1和m2分别为细磨后自还原产物在磁选前和磁选后分离出的金属粉末的质量(g);w(Fe)1和w(Fe)2分别为磁选前和磁选后分离出的金属粉末中的铁含量(%);w(Ni)1和w(Ni)2分别为磁选前和磁选后分离出的金属粉末中镍含量(%)。
从形式上看,公式(1)和(2)为磁选工序的金属回收率,但实际上悬浮在矿浆中尺寸十分细小的金属颗粒难以被磁铁吸引。实验中将磁选后的尾矿进行沉淀、烘干后再用磁铁去吸引时,干尾矿仍然有一定磁性,表明其中还存在细小的金属颗粒,但由于固体细粉粒的跟随运动,无法将细粒金属与脉石分离。也就是说,红土镍矿中氧化铁和氧化镍尽管已经被还原成金属原子,但只要它还没有聚集成足够尺寸的颗粒,就不能通过磁选从矿浆中分离出来。在不同的自还原工艺条件下,还原产物中金属元素无论是赋存状态(金属或者氧化物)还是被还原成金属原子后聚集成颗粒的尺寸大小都是不一样的,通过磁选分离也会得到不同的金属回收率。因此,公式(1)和(2)计算的金属回收率实际上反映了自还原过程工艺因素的影响。
2 红土镍矿中铁、镍氧化物还原热力学基础在高温自还原过程中,氧化物的还原反应与无烟煤中固定碳的气化反应同时进行,红土镍矿在还原过程中将发生如下反应[9-10]:
| $ {\rm{C + C}}{{\rm{O}}_{\rm{2}}}{\rm{ = 2CO, \Delta }}{\mathit{G}^\mathit{\theta }}{\rm{ = 166}}\;{\rm{550 - 171}}\mathit{T}{\rm{(J/mol);}} $ | (3) |
| $ {\rm{NiO + C = Ni + CO, \Delta }}{\mathit{G}^\mathit{\theta }}{\rm{ = 134}}\;{\rm{610 - 179}}{\rm{.08}}\mathit{T}{\rm{(J/mol)}}; $ | (4) |
| $ {\rm{NiO + CO = Ni + C}}{{\rm{O}}_{\rm{2}}}, {\rm{\Delta }}{\mathit{G}^\mathit{\theta }}{\rm{ = - 40}}\;{\rm{590 - 0}}{\rm{.42}}\mathit{T}{\rm{(J/mol)}}; $ | (5) |
| $ {\rm{3F}}{{\rm{e}}_{\rm{2}}}{{\rm{O}}_{\rm{3}}}{\rm{ + CO = 3FeO + C}}{{\rm{O}}_{\rm{2}}}, {\rm{\Delta }}{\mathit{G}^\mathit{\theta }}{\rm{ = - 52}}\;{\rm{131 - 41}}\mathit{T}{\rm{(J/mol)}}; $ | (6) |
| $ {\rm{F}}{{\rm{e}}_{\rm{3}}}{{\rm{O}}_{\rm{4}}}{\rm{ + CO = 3FeO + C}}{{\rm{O}}_{\rm{2}}}{\rm{(}}\mathit{T}{\rm{ > 843K)}}, {\rm{\Delta }}{\mathit{G}^\mathit{\theta }}{\rm{ = 35}}\;{\rm{380 - 41}}{\rm{.16}}\mathit{T}{\rm{(J/mol)}}; $ | (7) |
| $ \frac{1}{4}{\rm{F}}{{\rm{e}}_{\rm{3}}}{{\rm{O}}_{\rm{4}}}{\rm{ + CO = }}\frac{3}{4}{\rm{Fe + C}}{{\rm{O}}_{\rm{2}}}{\rm{(}}\mathit{T}{\rm{ < 843K)}}, {\rm{\Delta }}{\mathit{G}^\mathit{\theta }}{\rm{ = - 9}}\;{\rm{832 + 8}}{\rm{.58}}\mathit{T}{\rm{(J/mol)}}; $ | (8) |
| $ {\rm{FeO + CO = Fe + C}}{{\rm{O}}_{\rm{2}}}, {\rm{\Delta }}{\mathit{G}^\mathit{\theta }}{\rm{ = - 17}}\;{\rm{500 + 21}}{\rm{.0}}\mathit{T}{\rm{(J/mol)}}。$ | (9) |
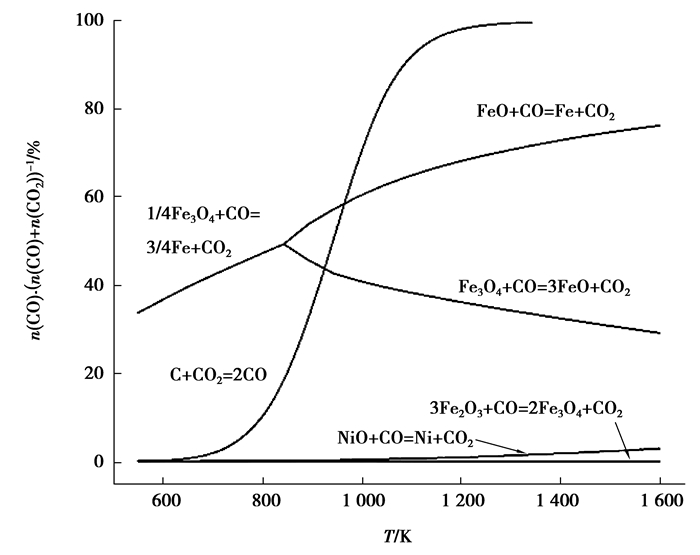
图 3是根据式(3)-(9)计算得到的碳直接还原镍、铁氧化物的热力学平衡曲线图。从图 3可见,高价氧化铁的还原相对比较容易,而低价氧化铁(FeO)的还原必须借助于高温下碳的气化反应才能完成。相比而言,镍氧化物(NiO)的还原要容易得多,理论上讲,NiO在碳的气化反应还未启动的低温阶段,伴随着红土镍矿中羟基水的脱除就能被CO还原为金属镍。根据这一热力学特性,可以通过控制红土镍矿自还原压块的内配碳比来控制压块内部的还原势,从而抑制红土镍矿中氧化铁的还原,使氧化镍优先被还原成金属镍,再通过物理分离获得镍品位较高的镍铁粉。对红土镍矿而言,铁和镍主要赋存于难还原的蛇纹石和绿泥石中,因此,实际的还原过程要复杂得多。
|
图 3 铁、镍氧化物还原平衡气相组成与温度的关系 Figure 3 Relationship between the temperature and the composition of equilibrium gas phase for the reduction of iron oxides and nickel oxides |
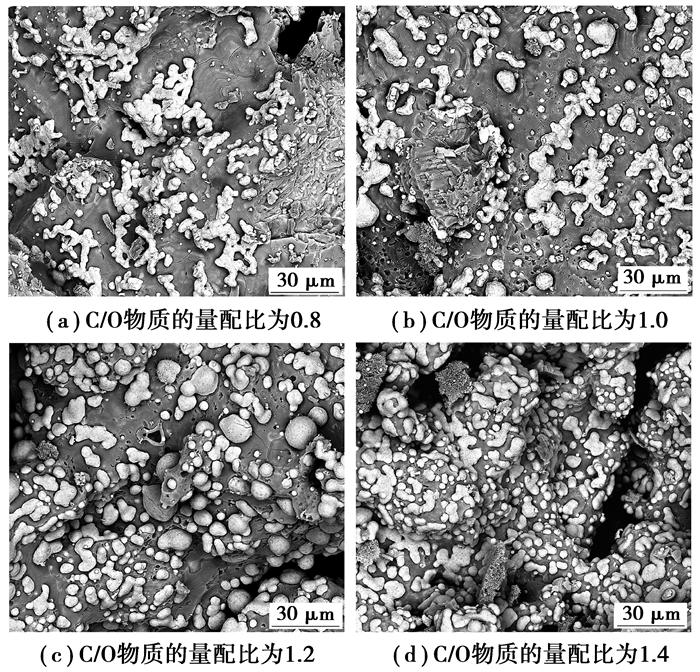
红土镍矿自还原压块中配加5%CaF2,内配碳比分别为0.8、1.0、1.2和1.4。试样在1 250 ℃还原15 min后,将还原产物在扫描电镜下观察其微观结构。图 4给出了不同内配碳比的压块自还原产物断口的微观形貌,图中金属相呈白色,脉石相呈灰色。从图 4可以看出,当配碳比为0.8和1.0时,金属相呈蠕虫状,且数量相对较小;当内配碳比达到1.2时,金属相呈光滑的球状,数量也显著增多;当内配碳比增加到1.4时,金属颗粒数量增加,但尺寸明显变小。由此可见,内配碳比对红土镍矿自还原过程的影响表现为:1)由于赋存于蛇纹石和绿泥石中的铁、镍氧化物还原性差,当内配碳比较低时还原不充分,形成的金属相较少;2)当内配碳比为1.2时,随着压块内部还原势的增强,铁、镍氧化物得到充分还原,金属析出量增大,金属相由蠕虫状逐渐收缩成球状;3)随着内配碳比进一步提高到1.4,还原剂大量过剩,未气化的碳粉对金属相的聚集起到阻碍作用,这一现象与铁矿粉压块自还原过程中金属相聚集的规律十分相似[11]。
|
图 4 不同配碳比的红土镍矿自还原产物在扫描电镜下的形貌 Figure 4 SEM images of self-reduction products of laterite nickel ore with different C/O atomic ratios |
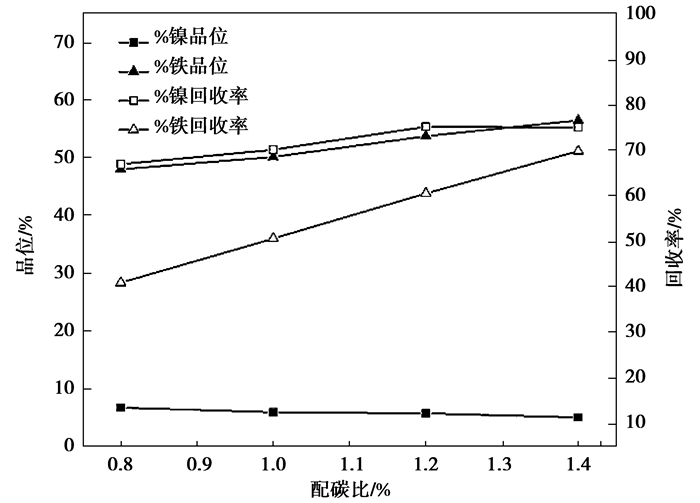
自还原产物通过细磨磁选得到的镍铁粉中镍、铁含量(品位)及金属元素回收率与红土镍矿压块内配碳比的关系如图 5所示。由图 5可见,随着红土镍矿压块内配碳比的增加,磁选产物含镍品位逐渐降低,而含铁品位则逐渐升高。镍和铁的回收率都随内配碳比的升高而升高,但内配碳比对金属铁回收率的影响远比对金属镍的回收率影响大,这一结果也反映出:1)氧化镍比氧化铁更容易被还原;2)较低的内配碳比确实可以抑制红土镍矿中氧化铁的还原,从而提高磁选产品的含镍品位,但相应牺牲金属镍的回收率。
|
图 5 配碳比对磁选产物镍、铁品位及回收率的影响 Figure 5 Effects of C/O atomic ratio on the grade of nickel and iron in ferronickel powders and the recovery rate of metal elements |
红土镍矿自还原压块内配碳比为1.2,CaF2的加入量分别为0%、2%、5%、8%、12%和15%,试样在1250℃下还原15 min,将还原产物在扫描电镜下观察其微观结构如图 6所示。由图 6可见,未添加CaF2的试样,还原产物中金属颗粒非常细小,弥散分布在脉石相中;当添加2%CaF2后,还原产物中金属相开始聚集长大,但金属颗粒仍然很小;随着CaF2加入量从5%增加到12%,金属颗粒粒径不断增大,金属相的聚集效果非常明显。当CaF2量增加到15%后,还原产物中金属颗粒连成一片。金属颗粒的聚集长大对还原产物细磨后的金属与脉石分离具有很好的促进作用,可大大提高金属元素的回收率。

|
图 6 不同CaF2用量下红土镍矿自还原产物在扫描电镜下的形貌 Figure 6 SEM images of self-reduction products of laterite nickel ore with different dosages of CaF2 |
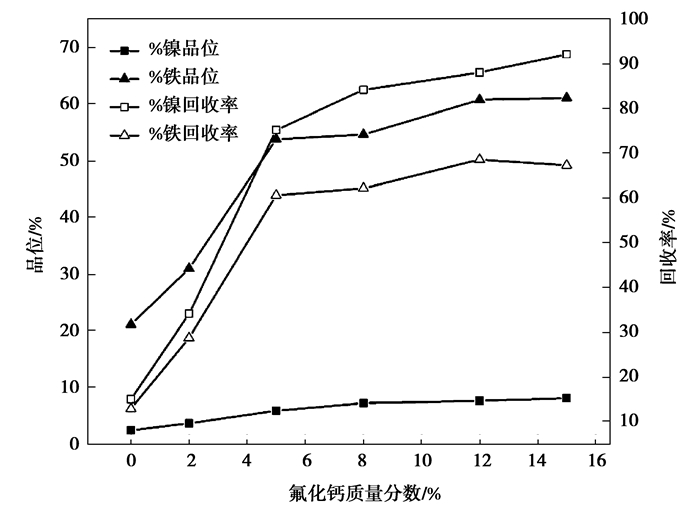
CaF2添加量对镍铁粉中镍、铁品位及金属元素回收率的影响如图 7所示。由图 7可见,未添加CaF2的试样,磁选出的镍铁粉中镍、铁品位及金属回收率非常低,镍含量仅为2.29%,镍的回收率只有14.83%。当添加CaF2之后,随CaF2加入量提高,磁选产物的镍、铁品位及金属回收率迅速增加。当CaF2达到8%时,镍铁粉中镍和铁的品位分别达到7.10%和54.56%,镍和铁的回收率分别达到84.14%和62.07%。继续增加CaF2量,对磁选产物中镍的品位及回收率影响不大。
|
图 7 CaF2对磁选产物镍、铁品位及回收率的影响 Figure 7 Effects of CaF2 on the grade of nickel and iron in magnetic products and the recovery rate of metal elements |
从上述实验结果可知,添加CaF2能大幅度促进红土镍矿自还原过程中金属相的聚集长大。通过对自还原产物进行XRD分析,以及CaF2对红土镍矿熔融温度影响的研究,分析CaF2强化红土镍矿自还原过程中金属相聚集长大的作用机理。
3.3.1 加入CaF2对还原产物矿物组成的影响取CaF2为0%和8%的两个试样(内配碳比1.2),在1 250 ℃下还原15 min后对还原产物进行XRD分析,结果如图 8所示。
|
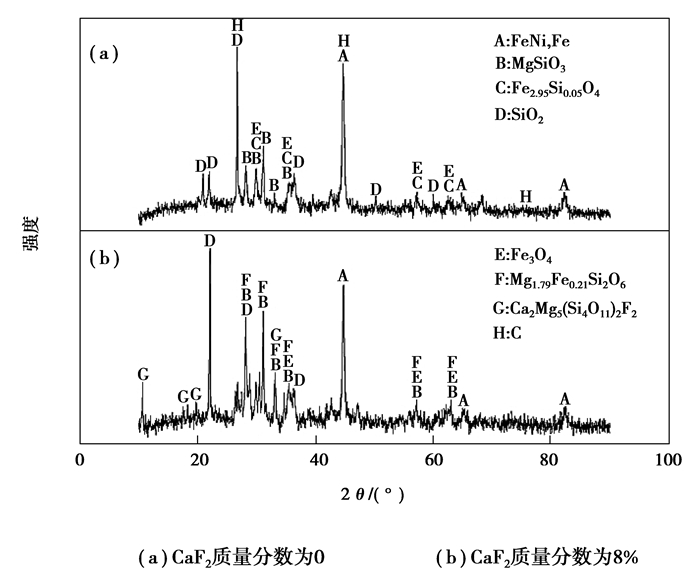
图 8 不同CaF2用量下自还原产物XRD图谱 Figure 8 XRD patterns of self-reduction products with different dosages of CaF2 |
由图 8可见,还原产物中金属镍以FeNi形式存在。未添加CaF2的试样自还原产物中,未被还原的铁以铁橄榄石(Fe2.95Si0.05O4)和磁铁矿(Fe3O4)的形式存在;添加8% CaF2后,还原产物中铁橄榄石物相消失,生成了透闪石(Ca2Mg5(Si4O11)2F2)和顽辉石(Mg1.79Fe0.21Si2O6)。这一结果表明CaF2能促进硅酸盐中氧化铁的还原。
橄榄石在硅氧骨干的构型上属于岛状结构硅酸盐,而透闪石则是双链状结构硅酸盐,顽辉石是单链状结构硅酸盐[12]。岛状结构硅酸盐的离子堆积方式比链状结构硅酸盐要更加紧密,并且硅氧骨干与金属阳离子之间的离子键力比链状结构硅酸盐要强[12],因而岛状结构硅酸盐的反应活性低于链状结构硅酸盐。CaF2能促进碳与硅酸盐的反应,在反应过程中通过形成链状结构硅酸盐来减少岛状结构硅酸盐的生成,促进了镍、铁氧化物的还原。
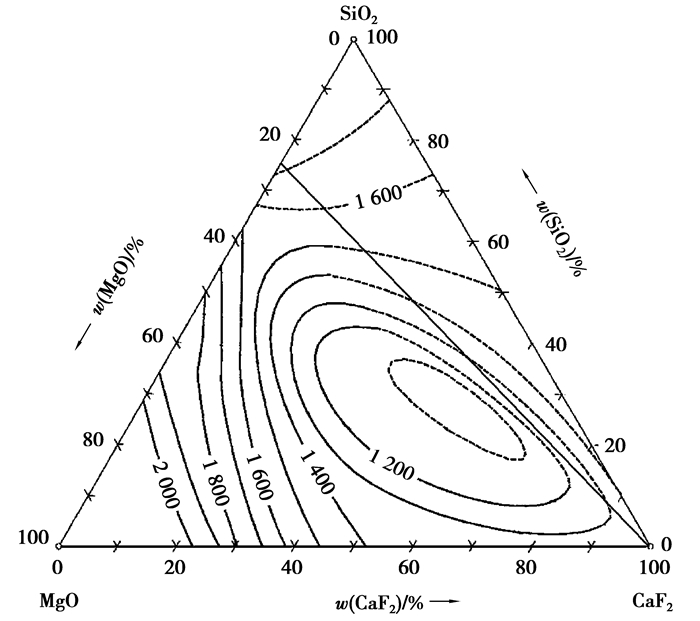
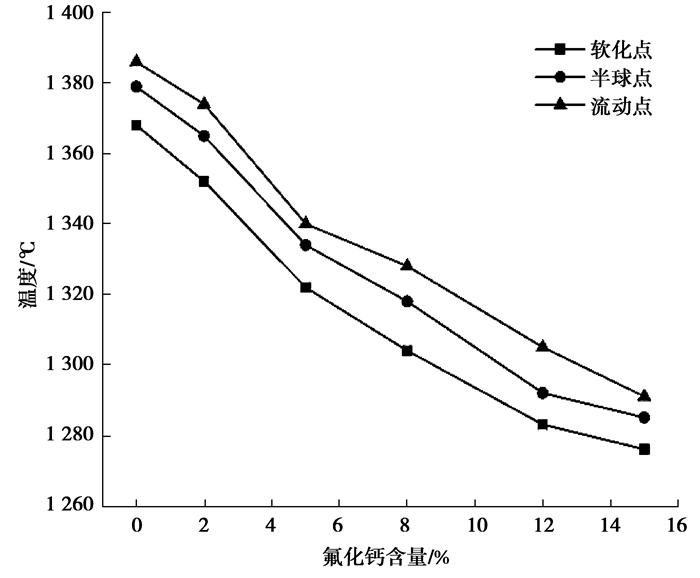
3.3.2 CaF2对红土镍矿脉石相熔融特性的影响表 1红土镍矿的主要脉石组成是SiO2和MgO,w(SiO2)/w(MgO)≈3/1,由SiO2-MgO-CaF2三元相图[13](图 9)可知,随CaF2的增加,渣系熔点是逐渐下降的。本实验中用炉渣熔点仪测定红土镍矿添加不同量CaF2后的熔融温度变化。为了模拟自还原过程中氧化铁和氧化镍被还原后实际脉石相的熔点变化,试样中仍然按内配碳比1.2配加煤粉,测试过程中通入氩气作保护气氛,测试结果见图 10。由图 10可见,随着CaF2用量的增加,红土镍矿自还原压块中脉石的软化温度、半球点温度和流动点温度均逐渐降低。
|
图 9 SiO2-MgO-CaF2三元系相图 Figure 9 Phase diagram of SiO2-MgO-CaF2 system |
|
图 10 CaF2对红土镍矿脉石熔融温度的影响 Figure 10 Effects of CaF2 on the melting temperature of laterite nickel ore gangue |
F-和O2-具有基本相同的离子半径[14-15],F-进入由Si-O四面体形成的硅酸盐网络结构中能降低Si-O键能,使Si-O键更容易断裂[16],从而降低硅酸盐的熔点。事实上,由图 8可知,加入CaF2后,脉石相中生成了低熔点的透闪石(Ca2Mg5(Si4O11)2F2)。从图 10可知,当加入8%CaF2后,脉石的软化点温度仍然高于自还原温度1 250 ℃,但根据固态扩散理论[17],当体系熔点降低时,原子扩散系数将增大,各反应物之间的传质速率加快,将促进金属颗粒沿边界析出,使较小的颗粒能够更快地聚集到大颗粒之上,从而使金属颗粒相互连接成一个整体,这些均促进了金属颗粒的析出、聚集与长大。
4 结论1) 红土镍矿采用煤基自还原-细磨-磁选工艺制备镍铁粉,在CaF2作用下通过降低内配碳比可抑制氧化铁的还原,从而获得镍品位较高的镍铁粉,但相应牺牲镍的回收率。
2) 在1 250 ℃下自还原,当内配碳比为0.8~1.0时,红土镍矿压块自还原析出的金属相晶粒细小,且呈蠕虫状;当内配碳比达到1.2时,红土镍矿中铁、镍氧化物得到充分还原,析出的金属晶粒尺寸大,呈球状;内配碳比提高到1.4,因还原剂大量过剩,未气化的碳粉对金属相的聚集起到阻碍作用。
3) CaF2能明显强化红土镍矿自还原过程中金属相的析出、聚集和长大,促进镍铁与脉石的有效分离,大幅度提高镍铁粉中镍和铁的品位及金属元素的回收率。当内配碳比1.2时,加入8%的CaF2,自还原产物细磨磁选后可获得含镍7.1%的镍铁粉,镍的回收率达到84.14%。
| [1] | Patzelt N, Schmitz T, Grund G. Treatment of nickel ores in rotary kilns and cyclone reactors[C]//Proceedings of International Laterite Nickel Symposium. New York, 2004:527-543. |
| [2] | LV X W, Bai C G, He S P, et al. Mineral change of Philippine and Indonesia nickel lateritic ore during sintering and mineralogy of their sinter[J]. ISIJ International, 2010, 50(3): 380–385. DOI:10.2355/isijinternational.50.380 |
| [3] | LV X W, Bai C G, Qiu G B, et al. Dehydrating and sintering of Philippine nickel laterite[J]. Canadian Metallurgical Quarterly, 2011, 50(1): 20–27. DOI:10.1179/000844311X552278 |
| [4] | Li B, Wang H, Wei Y G. The reduction of nickel from low-grade nickel laterite ore using a solid-state deoxidization method[J]. Minerals Engineering, 2011, 24(14): 1556–1562. DOI:10.1016/j.mineng.2011.08.006 |
| [5] | Kursunoglu S, Kaya M. Atmospheric pressure acid leaching of Caldag lateritic nickel ore[J]. International Journal of Mineral Processing, 2016(150): 1–8. |
| [6] | Landers M, Grafe M, Gilkes R J, et al. Nickel distribution and speciation in rapidly dehydroxylated goethite in oxide-type lateritic nickel ores:XAS and TEM spectroscopic(EELS and EFTEM) investigation[J]. Australian Journal of Earth Sciences An International Geoscience Journal of the Geological Society of Australia, 2011, 58(7): 745–765. |
| [7] |
刘继军, 胡国荣, 彭忠东.
红土镍矿处理工艺的现状及发展方向[J]. 稀有金属与硬质合金, 2011, 39(3): 62–66.
LIU Jijun, HU Guorong, PENG Zhongdong. The latest and future development of laterite nickel ore processing technology[J]. Rare Metals and Cemented Carbides, 2011, 39(3): 62–66. (in Chinese) |
| [8] |
郭学益, 吴展, 李栋, 等.
红土镍矿常压盐酸浸出工艺及其动力学研究[J]. 矿冶工程, 2011, 31(4): 69–76.
GUO Xueyi, WU Zhan, LI Dong, et al. Atmospheric leaching of nickel laterite by hydrochloride acid and its kine-tics[J]. Mining and Metallurgical Engineering, 2011, 31(4): 69–76. (in Chinese) |
| [9] |
林重春, 张建良, 黄冬华, 等.
红土镍矿含碳球团深还原-磁选富集镍铁工艺[J]. 北京科技大学学报, 2011, 33(3): 270–275.
LIN Chongchun, ZHANG Jianliang, HUANG Donghua, et al. Enrichment of nickel and iron from nickel laterite ore/coal composite pellets by deep reduction and magnetic separation[J]. Journal of University of Science and Technology Beijing, 2011, 33(3): 270–275. (in Chinese) |
| [10] |
黄希祜. 钢铁冶金原理[M]. 4版. 北京: 冶金工业出版社, 2013.
HUANG Xihu. Principles of steel metallurgy[M]. 4th ed. Beijing: The Metallurgical Industry Press, 2013. (in Chinese) |
| [11] |
赵栋楠. 碱性内配碳团块高温自还原制备金属铁粒的基础研究[D]. 武汉: 武汉科技大学, 2012. ZHAO Dongnan. Fundamental research on self-reduction of basic synthetic iron ore briquettes by carbon to make iron nuggets at high temperature[D]. Wuhan:Wuhan University of Science and Technology, 2012.(in Chinese) http://cdmd.cnki.com.cn/Article/CDMD-10488-1012460671.htm |
| [12] |
孙传尧, 印万忠. 硅酸盐矿物浮选原理[M]. 北京: 科学出版社, 2001.
SUN Chuanyao, YIN Wanzhong. Flotation principles of silicate minerals[M]. Beijing: Science Press, 2001. (in Chinese) |
| [13] |
陈家祥. 炼钢常用图表数据手册[M]. 2版. 北京: 冶金工业出版社, 2010.
CHEN Jiaxiang. Handbook of common chart data for steelmaking process[M]. 2th ed. Beijing: The Metallurgical Industry Press, 2010. (in Chinese) |
| [14] | Bjorn O M, David V. Interaction between fluorine and silica in quenched melts on the joins SiO2-AlF3, and SiO2-NaF determined by raman spectroscopy[J]. Physicss & schemistry of Minerals, 1985, 12(2): 77–85. |
| [15] |
赵运才, 肖汉宁, 谭伟.
CaF2添加量对玻璃陶瓷晶化过程及材料性能的影响[J]. 中国陶瓷工业, 2002, 9(6): 33–36.
ZHAO Yuncai, XIAO Hanning, TAN Wei. Effect of different amount of CaF2 added on crystallization and properties of glass-ceramic[J]. China ceramic industry, 2002, 9(6): 33–36. (in Chinese) |
| [16] | Kim H, Sohn I. Effect of CaF2 and Li2O additives on the viscosity of CaO-SiO2-Na2O slags[J]. ISIJ International, 2011, 51(1): 1–8. DOI:10.2355/isijinternational.51.1 |
| [17] |
张代东, 吴润. 材料科学基础[M]. 北京: 北京大学出版社, 2011.
ZHANG Daidong, WU Run. Fundamentals of materials science[M]. Beijing: Peking University Press, 2011. (in Chinese) |
 2017, Vol. 40
2017, Vol. 40

