1b. 重庆大学 低碳绿色建筑国际联合研究中心, 重庆 400045;
2. 中国市政工程西南设计研究总院有限公司, 成都 610081
1b. National Centre for International Research of Low-Carbon and Green Buildings, Chongqing University, Chongqing 400045, P. R. China;
2. Southwest Municipal Engineering Design and Research Institute of China, Chengdu 610081, P. R. China
过硫酸盐活化技术近年来在有机废水处理领域应用广泛[1-2]。与以产生羟基自由基(·OH)为主要活性物种降解有机物的原理不同[3],该技术主要通过一些活化方式如热活化、过渡离子活化以及紫外光活化等使S2O82-转化为更多的高活性自由基(·SO4-)[4-5],·SO4-的标准氧化还原电位(E0=2.5~3.1 V)接近甚至超过·OH(E0=1.8~2.7 V)[6-7],理论上可持续有效地降解甚至矿化大部分有机污染物且具有较好的经济效益。通常需要测定COD来表征过硫酸盐处理有机废水的效果,但处理后的水样中不可避免的还残留些许的过硫酸盐,S2O82-含有一个过氧键(-O-O-),具有较强氧化性,当遇到氧化性更强的物质时将表现为还原性。化学需氧量(COD)从某种程度上反映的是水样中还原性物质被氧化时消耗氧化剂的量,目前,COD测定方法主要有高锰酸钾法和重铬酸钾法,由于后者重铬酸钾具有非常强的氧化性,几乎可以完全氧化水中的有机物和还原性的无机物质,成为国际上普遍采用的COD标准测定法,但在采用重铬酸钾COD测定经过硫酸盐处理的有机水样时残余的S2O82-就可能被K2Cr2O7氧化,给CODCr测定带来干扰,影响结果的准确性[5, 8]。
高级氧化技术处理有机废水时引进的某些化学试剂或与其有机物质反应后残余组分对COD的测定都可能会带来不同程度的干扰,国内学者刘生宝等[9]研究了Fenton技术中残余组分如Fe2+和H2O2对COD的干扰,发现影响值同残余组分浓度成一定线性关系,通过测定值乘以折减系数满足精度要求。国内外文献对于S2O82-处理有机废水应用有较多报导,Deng等[10]采用热活化过硫酸盐技术处理垃圾渗滤液时,考虑了S2O82-对COD测定的影响,尽量使引入的过硫酸盐反应殆尽再进行COD测定,此法效率偏低,操作有难度,且S2O82-难以完全耗尽,比较耗费能量。Kehinde等[11]研究环境条件对过硫酸盐氧化处理纺织废水的影响时对COD的测定忽略了引入S2O82-质量浓度的影响。
目前,有机废水的处理越来越倾向于采用过硫酸盐高级氧化技术,与其相关的COD测定技术的改良也一直是众多研究者的兴趣所在。笔者研究了水样中引入S2O82-质量浓度与CODCr测定值的关系,发现呈良好的线性相关性,且考察了所得线性关系在不同水样体系包括几类实际环境水体中的适用性,从而为消除S2O82-对CODCr测定的影响提供依据。
1 材料与方法 1.1 主要仪器与试剂1) 仪器:HACH DR1010分光光度计;HACH DRB 200消解器;HACH COD 10 mL消解比色管;艾科浦超纯水机;TOC测定仪HTY-DI1500;BSA124S-CW电子天平。
2) 试剂:过硫酸钾(分析纯);1, 2-苯二甲酸单钾盐(KHP,优级纯);重铬酸钾(分析纯);硫酸汞(分析纯);硫酸银(分析纯);浓硫酸(分析纯)。
1.2 测定方法本实验测定S2O82-原理同碘量滴定法类似,采用分光光度法间接测定水溶液中S2O82-离子质量浓度[12]。首先向50 mL比色管中加入0.2 g NaHCO3和4 g KI,然后加入有S2O82-的水样,然后定容利用S2O82-与I-充分混匀反应后在特定波数下测定吸光度从而间接得到S2O82-离子质量浓度。
考虑低质量浓度COD测定时仪器误差的影响可能会大于高质量浓度的COD,因此针对低、高质量浓度(分别为0~150 mg/L和0~1 500 mg/L)COD范围采用HACH 1010分别进行测定,类似于分段重铬酸钾测定COD的思想,对不同范围内的COD采用不同重铬酸钾质量浓度,低量程组选用4.903 2 g/L K2Cr2O7溶液,高量程组选用49.032 g/L K2Cr2O7溶液。两种量程的COD测定原理分别如下:
低量程组是指在(440±20) nm波长处测定溶液中残余Cr2O72-和生成的Cr3+两种铬离子总吸光度,绘制总吸光度变化值与水样CODCr值的标准曲线,从而计算出水样CODCr值。高量程组是指在(600±20) nm波长处测定水样中Cr3+的吸光度,通过Cr3+的吸光度变化值与水样CODCr值之间的正比例关系得出相应标准吸光度曲线,从而计算出水样中的CODCr值[13]。本实验分别在波长420 nm和610 nm处进行吸光度测量。
1.3 研究方法实验初始阶段将S2O82-标准溶液作为管理水样对CODCr全程序空白值进行测定,即配制梯度S2O82-质量浓度去离子水系列溶液,然后分别测定CODCr值,绘图得到的结果符合数理统计线性规律;取一定量的有机废水样,测定CODCr值,记有机废水样CODCr测定值与去离子水体系中梯度S2O82-质量浓度对应的CODCr值之和为CODCr′,继续向有机废水样中添加梯度S2O82-质量浓度后直接测定相应的化学需氧量记为CODCr″,通过比较CODCr′和CODCr″是否一致,来分析判断是否可以通过扣除水样中对应的COD值或采用折减系数来消除S2O82-对有机废水CODCr测定的影响或校正测定值。
2 结果与讨论 2.1 S2O82-质量浓度与CODCr的关系由于高质量浓度和低质量浓度的重铬酸钾的氧化性不同,导致生成物的价态也可能不同,另外HACH 1010测定分低、高2种不同的量程,因此在研究不同水样体系中S2O82-质量浓度与CODCr值的关系时也需要从2个量程组分别考察起,尽量消除由于仪器误差等不确定性因素对测定结果带来的干扰。
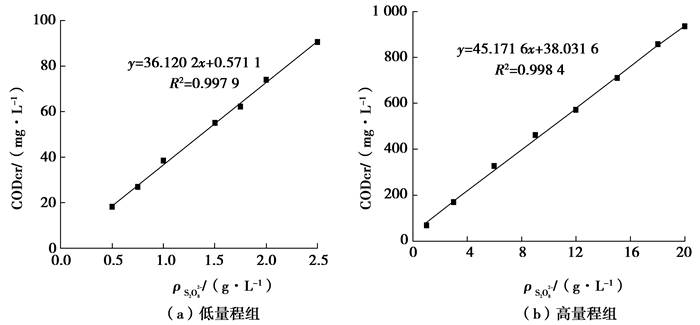
准确配制低、高2种质量浓度组(0.5~2.5 g/L)及(1.0~20.0 g/L)的过硫酸根离子溶液(以过硫酸钾为溶质,去离子水为溶剂)并测定其对应的CODCr值,实验结果如图 1所示。通过对实验数据进行统计和回归分析,发现这2种数值即S2O82-质量浓度CODCr和之间确实存在着线性关系,无论在低量程组还是高量程组中,线性关系都比较良好,线性方程分别为低量程组:y=36.120 2x+0.571 1,R2=0.997 9,高量程组:y=45.171 6x+38.031 6,R2=0.998 4,其中y代表CODCr值,x代表S2O82-质量浓度,R为相关系数。
|
图 1 去离子水体系S2O82-质量浓度与CODCr值关系 Figure 1 Relationship between S2O82- and COD in ultrapure water |
由此可以判断在采用重铬酸钾法测定COD时,K2Cr2O7与水样中S2O82-发生了某种程度上的化学反应,导致氧化剂消耗量的增加。参考Cr2O72-与H2O2在酸性条件下的反应方程式(1)[14]推测Cr2O72-与S2O82-的反应方程式可能如式(2)。
| $ {\rm{C}}{{\rm{r}}_{\rm{2}}}{\rm{O}}_7^{2{\rm{ - }}}{\rm{ + 3}}{{\rm{H}}_{\rm{2}}}{{\rm{O}}_{\rm{2}}}{\rm{ + 8}}{{\rm{H}}^{\rm{ + }}} \to {\rm{2C}}{{\rm{r}}^{{\rm{3 + }}}}{\rm{ + 7}}{{\rm{H}}_{\rm{2}}}{\rm{O + 3}}{{\rm{O}}_{\rm{2}}}{\rm{, }} $ | (1) |
| $ {\rm{C}}{{\rm{r}}_{\rm{2}}}{\rm{O}}_7^{2{\rm{ - }}}{\rm{ + 3}}{{\rm{S}}_{\rm{2}}}{\rm{O}}_8^{2{\rm{ - }}}{\rm{ + 2}}{{\rm{H}}^{\rm{ + }}} \to {\rm{2C}}{{\rm{r}}^{{\rm{3 + }}}}{\rm{ + 6SO}}_4^{2{\rm{ - }}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O + 3}}{{\rm{O}}_{\rm{2}}}{\rm{}}。$ | (2) |
根据方程式(2),理论上,1 g S2O82-对CODCr变化的贡献值为83.34 mg,但据图 1分析可得,低、高质量浓度组中1 g S2O82-引起的CODCr变化值分别为36.12 mg和45.17 mg。由此推测CODCr测定过程中,可能还存在除Cr2O72-→Cr3+外的其他反应。Meyer和Pietsch曾提出酸性条件下,Cr2O72-与H2O2反应会有H2Cr2O12生成,其不稳定又会转化为Cr2O3[15],如式(3),(4)。因此本实验中,Cr2O72-与S2O82-反应过程中可能还会有稳定性较强的氧化铬沉淀(Cr2O3)生成。
| $ {{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{r}}_{\rm{2}}}{{\rm{O}}_{\rm{7}}}{\rm{ + 5}}{{\rm{H}}_{\rm{2}}}{{\rm{O}}_{\rm{2}}} \to {{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{r}}_{\rm{2}}}{{\rm{O}}_{{\rm{12}}}}{\rm{ + 5}}{{\rm{H}}_{\rm{2}}}{\rm{O, }} $ | (3) |
| $ {{\rm{H}}_{\rm{2}}}{\rm{C}}{{\rm{r}}_{\rm{2}}}{{\rm{O}}_{{\rm{12}}}}{\rm{ + 8}}{{\rm{H}}_{\rm{2}}}{{\rm{O}}_{\rm{2}}} \to {\rm{C}}{{\rm{r}}_{\rm{2}}}{{\rm{O}}_{\rm{3}}}{\rm{ + 9}}{{\rm{H}}_{\rm{2}}}{\rm{O + 8}}{{\rm{O}}_{\rm{2}}}。$ | (4) |
已知每克邻苯二甲酸氢钾(KHP)溶于1 L水中对应COD为1 776 m/L计算,分别配制2组质量浓度梯度的COD标准溶液(30, 60, 90 mg/L;300, 500, 800 mg/L),分别加入不同剂量的S2O82-,经过150 ℃消解2 h后,冷却至常温,测定水样吸光度以确定S2O82-变化值,测定CODCr值同已知质量浓度进行比较。
结果如表 1和表 2所示。表 1显示消解后低质量浓度COD标准溶液中S2O82-的剩余质量浓度值与实际加入的S2O82-量差值仅为实际加入S2O82-的0.40% ~ 4.20%;表 2显示消解后高质量浓度COD标准溶液中S2O82-的剩余质量浓度值与实际加入的S2O82-量差值仅为实际加入S2O82-的0.71%~6.51%。说明在COD标准溶液消解前后S2O82-没有显示量的差异,而且无论KHP配制质量浓度高低,COD测定结果并未发生实质性变化,因此过硫酸盐活化技术处理的实际有机废水样残余S2O82-在消解过程中产生硫酸根自由基降解COD标准溶液的情况可以排除。
| 表 1 低量程组COD标准溶液体系中S2O82-的质量浓度变化 Table 1 The variation of COD concentration in low concentration standard S2O82- solution |
| 表 2 高量程组COD标准溶液体系中S2O82-的质量浓度变化 Table 2 The variation of COD concentration in high concentration standard S2O82- solution |
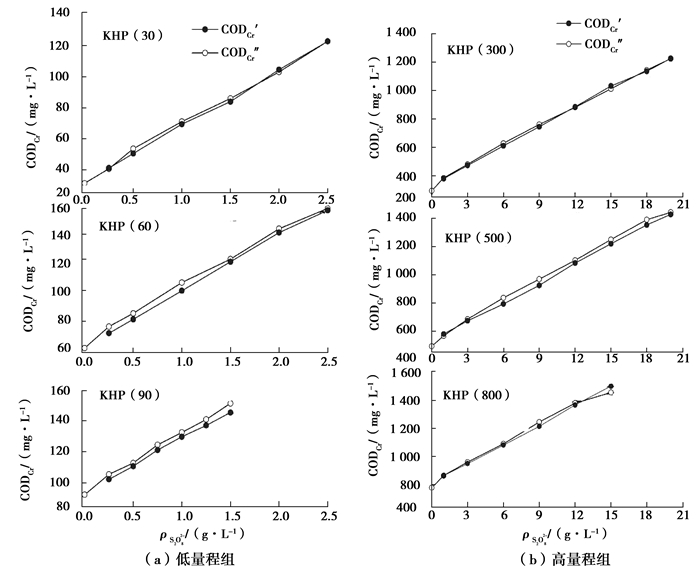
分析比较CODCr′与CODCr″结果如图 2所示。从图 2(a),图 2(b)可以看出CODCr′与CODCr″差异较小;在低质量浓度的COD标准溶液中CODCr′与CODCr″差值为0.1~6.1 mg/L,为原水有机物产生CODCr值的0.43%~9.67%;高质量浓度组中CODCr′与CODCr″差值为2~83 mg/L,为原水有机物产生CODCr值的0.07%~8.92%。说明在COD标准溶液体系中S2O82-质量浓度-CODCr线性方程能较好的反映实际的COD差异。
|
图 2 COD标准溶液体系中CODCr′与CODCr″的比较 Figure 2 Comparison of CODCr′ and CODCr″ in standard COD solution system |
实际废水体系成分复杂,在不具备过硫酸盐活化技术条件下,其中某些物质可能也具备催化S2O82-反应或分解的能力。为了分析对实际环境废水体系CODCr测定的影响,重复上述考察COD标准溶液体系中线性关系适用性的实验步骤,以分析消除S2O82-对于水体有机物CODCr测定值的干扰是否适用于实际废水体系。
考察垃圾渗滤液反渗透后(RO)出水,向其中添加适量S2O82-然后进行测定。由表 3计算得知,2 h后S2O82-的剩余质量浓度与实际加入S2O82-的量最大差值仅为实际加入的0.52%~8.45%,S2O82-含量在实际水样体系中没有发生明显的变化,说明在上述废水体系中S2O82-处于比较稳定的状态。
| 表 3 实际废水体系中S2O82-的质量浓度变化 Table 3 The variation of S2O82 in environmental water solution 2 h later |
继而对机械厂乳化液的混凝处理出水和垃圾渗滤液MBR出水分别研究,实验结果如表 4所示。据表 4可知,反应2 h后实际废水体系中S2O82-的测定值相对于实际加入S2O82-量几乎没有变化,变化波动范围仅0.07%~4.92%,说明S2O82-在水样中基本没有发生反应。
| 表 4 实际废水体系S2O82-的质量浓度变化 Table 4 The variation of S2O82 in environmental water solution 2 h later |
过硫酸盐具有强氧化性,但在一般常规条件下还不能发挥很好的氧化效力,只有在一定条件下或配合先进活化技术使发生S2O82-→·SO4-时才可以达到去除有机物的目的。实际水样成分尽管复杂,但总体在常规条件下不影响S2O82-。
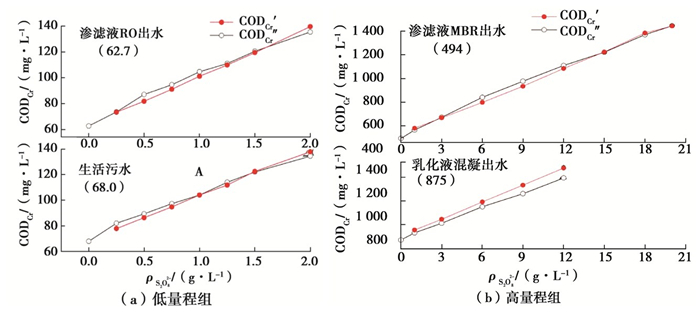
所选实际废水体系分别代表 2种COD质量浓度组,垃圾渗滤液反渗透出水COD值较低,代表低质量浓度组,而机械加工厂乳化液的混凝处理出水和垃圾渗滤液MBR出水COD值一般较高,代表高质量浓度组。计算CODCr′与CODCr″比较结果分别如图 3所示。在低质量浓度组的实际废水体系中CODCr′与CODCr″差值为0.1~5.2 mg/L,为原水CODCr的0.11%~8.92%;高质量浓度组中CODCr′与CODCr″差值为1~45 mg/L,为原水CODCr的0.36%~9.56%。说明S2O82-质量浓度-CODCr线性方程依然适用于在实际废水体系中消除S2O82-对CODCr测定的干扰。
|
图 3 实际废水体系中CODCr′与CODCr″的比较 Figure 3 Comparison of CODCr′ and CODCr″ in environmental water solution |
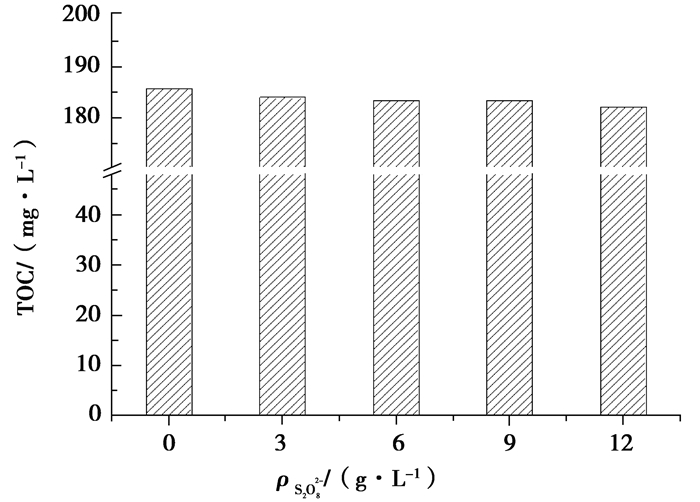
实验中探讨了S2O82-是否会对TOC测定造成干扰的实验,即通过用邻苯二甲酸氢钾配置一定质量浓度的TOC溶液,然后在其中投加不同质量浓度的S2O82-,使用TOC测定仪测定TOC值,实验结果见图 4。由图可以看出,随着S2O82-质量浓度的提高,测定得到的TOC值较空白水样TOC值偏差越来越大,但不同质量浓度S2O82-下的TOC测定值与TOC准确值最大相差也才接近1.9%,几乎可以忽略。由此可得,在测定体系中TOC时,过量的过硫酸盐对TOC的测定影响相对COD的测定是几乎可以忽略的。因此在采用过硫酸盐高级氧化技术处理有机废水时,鉴于废水水质,在水样有机物质含量不高时,COD测定误差较TOC大,建议采用TOC代替COD来表征水质处理效果。
|
图 4 S2O82-对TOC测定的干扰 Figure 4 The disturbance of S2O82- to the determination of TOC |
着重就过硫酸盐活化技术处理有机废水后水样中残余过硫酸根离子对COD测定影响进行研究,发现和提出类似标准曲线校正的扣除法消除S2O82-干扰,并进行方法适用性的检验,从COD低量程和高量程2种情况对COD标准溶液体系和实际水体进行研究。结果表明:
1) 在去离子水体系中,引入的S2O82-质量浓度与CODCr测定值之间具备较好的线性相关性,在低(CODCr=0~150 mg/L)、高(CODCr=0~1 500 mg/L)2种质量浓度CODCr测定组中,线性关系方程分别为y=36.120 2x+0.571 1(R2=0.997 9;x,g/L;y,CODCr mg/L),y=45.171 6x+38.031 6(R2=0.998 4)。
2) 上述线性方程可用于COD标准溶液体系和实际环境水体CODCr测定时消除S2O82-的干扰。
3) 针对有机质含量不高的水样,采用测定TOC代替COD受到环境及技术因素影响较小,更能准确反映处理效果。
| [1] |
高焕方, 龙飞, 曹园城, 等.
新型过硫酸盐活化技术降解有机污染物的研究进展[J]. 环境工程学报, 2015, 12(9): 5658–5664.
GAO Huanfang, LONG Fei, CAO Yuancheng, et al. Advances in degradation of organic pollutants by novel persulfate activated technology[J]. Chinese Journal of Environmental Engineering, 2015, 12(9): 5658–5664. (in Chinese) |
| [2] |
马京帅, 吕文英, 刘国光, 等.
热活化过硫酸盐降解水中的普萘洛尔[J]. 环境化学, 2017, 2(36): 1–8.
MA Jingshuai, LYU Wenying, LIU Guoguang, et al. Degradation of propranolol in aqueous solution by heat-activated persulfate[J]. Environmental Chemistry, 2017, 2(36): 1–8. (in Chinese) |
| [3] |
王伟, 初本莉, 王嘉承.
过硫酸盐法和芬顿法降解有机物的对比研究[J]. 广州化工, 2013, 22(44): 4–7.
WANG Wei, CHU Benli, WANG Jiacheng. The comparative study of degradation of organic pollutants between persulfate method and Fenton method[J]. Guangzhou Chemical Industry, 2013, 22(44): 4–7. (in Chinese) |
| [4] | House D A. Kinetics and mechanism of oxidations by peroxydisulfate[J]. Chemical Reviews, 1962, 62(3): 185–203. DOI:10.1021/cr60217a001 |
| [5] | Ghaly M Y, Farah J Y, Fathy A M. Enhancement of decolorization rate and COD removal from dyes containing wastewater by the addition of hydrogen peroxide under solar photocatalytic oxidation[J]. Desalination, 2007, 217(1/2/3): 74–84. |
| [6] | Buxton G V, Greenstock C L, Helman W P, et al. Critical review of rate constants for reactions of hydrated electrons, hydrogen atoms and hydroxyl radicals in aqueous solution[J]. Journal of Physical and Chemical Reference Data, 1988, 17(2): 513–886. DOI:10.1063/1.555805 |
| [7] | Neta P, Huie R E, Ross A B. Rate constants for reactions of inorganic radicals in aqueous-solution[J]. Journal of Physical & Chemical Reference Data, 1988, 17(3): 1027–1284. |
| [8] |
郭玉文, 袁东.
对CODCr测定干扰因素及其消除方法的探讨[J]. 环境工程, 2007, 25(6): 73–75.
GUO Yuwen, YUAN Dong. Discussion on the interference factors and its eliminating methods in the determination of CODCr[J]. Environmental Engineering, 2007, 25(6): 73–75. (in Chinese) |
| [9] |
刘生宝, 刘芬, 蓝明菊.
Fenton技术中残余组分对COD测定的干扰和消除研究[J]. 当代化工, 2016, 45(6): 1152–1155.
LIU Shengbao, LIU Fen, LAN Mingju. Interference and elimination of residual components on the standard COD test in Fenton technology[J]. Contemporary Chemical Industry, 2016, 45(6): 1152–1155. (in Chinese) |
| [10] | Deng Y, Ezyske C M. Sulfate radical-advanced oxidation process (SR-AOP) for simultaneous removal of refractory organic contaminants and ammonia in landfill leachate[J]. Water Research, 2011, 45(18): 6189–6194. DOI:10.1016/j.watres.2011.09.015 |
| [11] | Kehinde FO, Abdul Aziz H. Influence of operating conditions on the persulfate oxidation of textile waste water at ambient temperature[J]. Applied Mechanics & Materials, 2015, 802(34): 454–459. |
| [12] | Liang C, Huang C F, Mohanty N, et al. A rapid spectrophotometric determination of persulfate anion in ISCO[J]. Chemosphere, 2008, 73(9): 1540–1543. DOI:10.1016/j.chemosphere.2008.08.043 |
| [13] |
谭庆欢.
配制COD试剂替代美国哈希COD试剂[J]. 现代物业, 2012(5): 153–155.
TAN Qinghuan. Preparation of COD agent instead HACH-COD reagent[J]. Modern Property Management, 2012(5): 153–155. (in Chinese) |
| [14] | Snell F D, Hilton C L, Ettre L S. Encyclopedia of industrial chemical analysis[J]. Organophosphorus Compounds, 1966, 4(1): 17–19. |
| [15] | Partington E J R. Gmelins Handbuch der anorganischen Chemie[J]. The Jphys.chem, 1934(2): 307–307. |
 2017, Vol. 40
2017, Vol. 40

