2. 河南理工大学 安全科学与工程学院, 河南 焦作 454003
2. School of Safety Science & Engineering, Henan Polytechnic University, Jiaozuo 454003, Henan, P. R. China
煤自燃是一个极其复杂的物理化学过程,在一定的条件下伴随着煤氧物理化学吸附、热量释放、煤温升高、最终达到燃点导致发火的过程。同时煤作为具有复杂物理化学结构的有机岩体,其官能团的种类、氧化活性决定煤氧化活化能的大小,进而影响煤氧化反应的速率。近些年来,国内外研究学者针对煤自燃氧化特性及表观活化能进行了大量的研究,取得了一定的成果。李林等[1]提出了煤自燃活化理论,认为温度越高,煤自燃活化需要的活化能越小,煤就越容易被活化。秦波涛等[2]以活化能为观点提出在煤炭的自燃过程中,随着煤体温度的升高,活化能逐步降低。王兰云等[3]基于静态耗氧实验结果所得的活化能变化规律显示,随着温度升高,煤氧复合的活化能逐渐减小,较高温度时出现负值。陆伟等[4]在研究中提出煤自燃逐步自活化反应理论,得出了煤自燃过程活化能随温度的升高逐步上升。屈丽娜[5]在煤自燃阶段特征及其临界点变化规律的研究中得到煤在氧化反应过程中,其活化能经历了由负值向到正值的变化过程。邓军等[6]运用15 t大型实验平台研究煤自燃和厌氧冷却过程,分析了煤自燃过程中温度、耗氧速率和生成气体比例的变化。谢振华等[7]通过程序升温实验,测定了不同粒径煤样在不同温度下产生CO、CO2等气体的浓度,并指出了指标气体的选择。朱红青等[8]基于煤绝热氧化自热升温过程的基本假设,并结合Arrhenius方程对该过程的反应特征进行分析,得到了不同变质程度煤自燃发火难易程度差异的氧化动力学原因。Fei等[9]采用MTE技术研究分析了维多利亚褐煤和巴基斯坦褐煤等低阶煤及其系列干燥合成物的自燃氧化特性。Avila等[10]运用油镜和图像分析技术分析研究了来自世界各地25种煤样的纹理特征,得出煤的岩相特征可作为评价其自燃潜在性的一种方法。Nimaje等[11]采集49个煤样,通过工业分析、元素分析、交叉点温度、岩相分析、燃点温度、Olpinski指数、热重实验等确定煤的自燃特性,得到元素分析数据与Olpinski指数有着显著地相关性。Dai等[12]运用MFBRA探讨不同煤种和混合煤样在热解过程中气体释放特征和生成动力学,结果显示在相同条件下随着煤的挥发性增加,气体初始释放温度和热解活化能降低,混煤的活化能不等于单煤活化能加权平均值。Yangali等[13]在西弗吉尼亚煤岩热重实验研究分析中得到煤岩自燃氧化过程中的每个温度阶段,其活化能呈现出不同的规律。Taraba等[14]采集了300个不同种类和不同自然含水量的煤样,并结合25年实验经验,运用PFC技术方法评价煤的自燃性。
以上研究主要基于不同矿区或者相同矿区不同煤层煤样自燃过程中氧化特性及活化能变化开展的,对于不同自燃倾向性煤低温氧化阶段活化能变化规律以及氧化特征方面的研究与归纳鲜有报道。结合煤的自燃倾向性研究煤自燃过程中氧化特性及活化能变化,得到不同自燃性煤低温氧化规律,把煤低温氧化特性影响因素与煤的自燃倾向性联系起来,对制定统一的煤矿防灭火技术和措施具有重要意义。基于此,选取铜川下石节煤矿、大同国投塔山矿和晋城王台铺煤矿的煤样为样本,通过交叉点温度法确定三种煤样的自燃倾向性,在此基础上通过煤的自燃氧化实验,分析不同自燃性煤氧化过程中的氧化特性及活化能的变化规律。
1 理论分析模型煤的物理化学结构影响煤的自燃氧化过程,煤中有大量的官能团和活性结构与氧气反应生成CO、CO2等气体,反应[15]如下:
| $\text{Coal+}{{\text{O}}_{\text{2}}}\to \mathsf{m}\text{CO+gC}{{\text{O}}_{\text{2}}}\text{+}其他产物$ | (1) |
根据阿伦尼乌斯方程,任意温度T时煤氧之间的反应速率为
| $V(T)={{V}_{\text{CO}}}(T)/m=AC_{\text{O}2}^{n}\text{exp}\left( -E/RT \right)$ | (2) |
假设:1) 反应前后煤样质量变化很小,忽略不计。2) 干空气朝煤样罐的轴向流动且流量稳定。3) 煤样罐内温度均匀。
基于以上假设,在煤样罐轴向dx处煤样的CO生成速率为
| $S{\rm{d}}x{V_{{\rm{CO}}}}(T) = Q{\rm{d}}c{\rm{,}}$ | (3) |
将式(2) 带入式(3) ,得
| $S{\rm{d}}xAmC_{{\rm{O}}2}^n{\rm{exp}}\left( { - E/RT} \right) = Q{\rm{d}}c,$ | (4) |
将式(4) 积分可得
| $\int _{0}^{L}SAmC_{\text{O}2}^{n}\text{exp}\left( -E/RT \right)\text{d}\mathsf{x}=\int _{0}^{C}Q\text{d}c,$ | (5) |
可以得到
| $\text{ln}c=-\frac{E}{R}\frac{1}{T}+\text{ln}\frac{SLAmC_{\text{O}2}^{n}}{Q}$ | (6) |
式中:S为煤样罐的截面积,m2;A为指前因子;T为煤的热力学温度,K;E为活化能,J/mol;R为摩尔气体常数;VCO(T)为CO的生成速率,m3/(m3·s);Q为气流速率,m3/s;c为煤氧化过程中生成CO的体积分数;L为煤样罐的长度,m;CO2为反应气体中氧气的含量,mol/m3;n为反应级数。由式(6) 可知lnc与1/T呈线性关系,通过拟合的直线斜率可求出煤氧化不同反应阶段的表观活化能。
2 实验过程 2.1 煤样的选取与制备选取铜川下石节煤矿、大同国投塔山矿、晋城王台铺煤矿的煤样,按照《GB/T1922—2003》和《GB474—2008煤样制备方法》进行煤样的采取、制备,煤样采取和制备后用密封袋密封好,防止氧化。实验前,选取大块三种煤样中煤芯部分,用粉碎机粉碎并筛选出粒径为0.18~0.45 mm的煤样为测试煤样,放在密封瓶中待用。
2.2 煤自燃倾向性判定根据《煤自燃倾向性的氧化动力学测试方法》[16]测定煤自燃倾向性的方法进行实验。按照实验要求和方法,可求出各煤样自燃倾向性判定指数I[17]。对照判定标准,得出3种煤样的自燃倾向性,如表 1所示。
| 表 1 3种煤样自燃倾向性 Table 1 Spontaneous combustion tendencies of 3 coal samples |
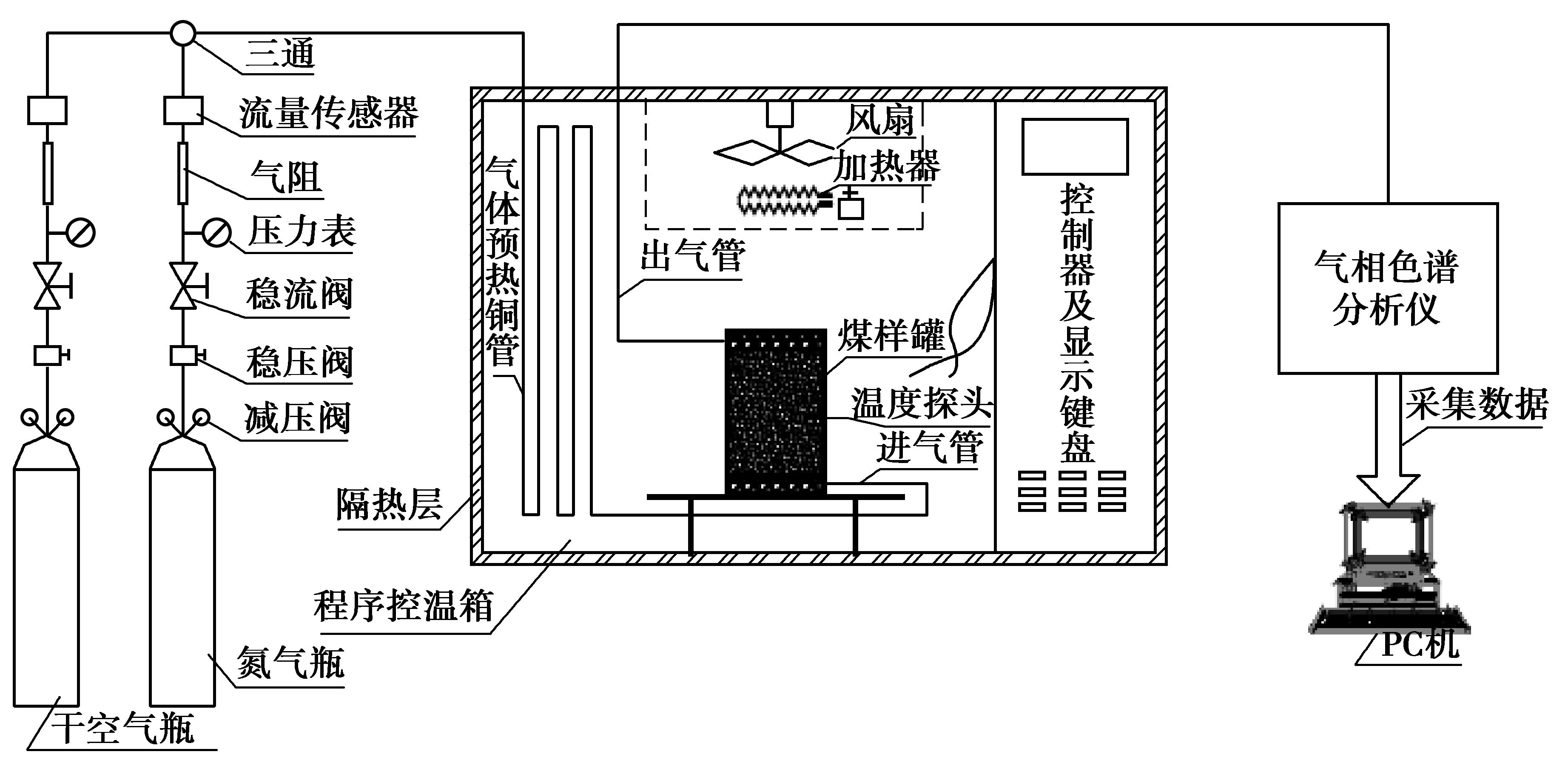
煤程序升温氧化实验装置采用煤氧化升温模拟系统(见图 1)。该系统由预热气路系统、传热煤样罐、程序控温箱、气体采集和分析系统、多路数据采集系统组成。测试时煤样罐放在可程序升温的恒温箱中,恒定干燥的空气从煤样罐的底部流入,在气体出口处对浓度进行收集处理。实验开始前,将50 g粒径为0.18~0.45 mm测试煤样置于煤样罐中,设置干空气流量60 mL/min,控温箱以0.8 ℃/min的升温速率对煤样罐进行程序升温,利用气体分析仪采集数据,在温度35~260 ℃间尽可能多的检测煤样罐出口的CO和O2体积分数。
|
图 1 煤氧化模拟实验系统 Figure 1 System of simulating spontaneous combustion of coal |
通过实验室煤氧化模拟试验仪(STA449C热分析仪),对3种煤样进行热重-差示扫描量热(TG-DSC)实验分析研究。实验测试前,将20 mg粒径为40~80目测试煤样放入坩埚中,干空气流量为50 mL/min,保护气流量25 mL/min,在温度30~300 ℃阶段内,以5 ℃/min升温速率对煤样进行加热,可得3种煤样氧化过程中DSC曲线。
3 实验结果与分析 3.1 CO产生量规律及氧化特征温度通过气体分析仪检测出口生成气体成分和体积分数,可得3种煤样升温过程中CO体积分数变化规律,如图 2所示。同时根据式(6) 对不同自燃倾向性煤样在不同温度下CO气体产生量进行计算拟合,得出了不同温度段lnc与1/T之间的函数关系式,如图 3所示。
|
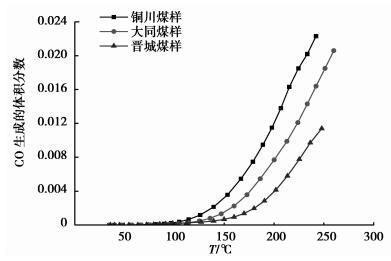
图 2 3种煤样升温过程中CO体积分数变化规律 Figure 2 Relationship between CO concentration and temperature of 3 coal samples |
|
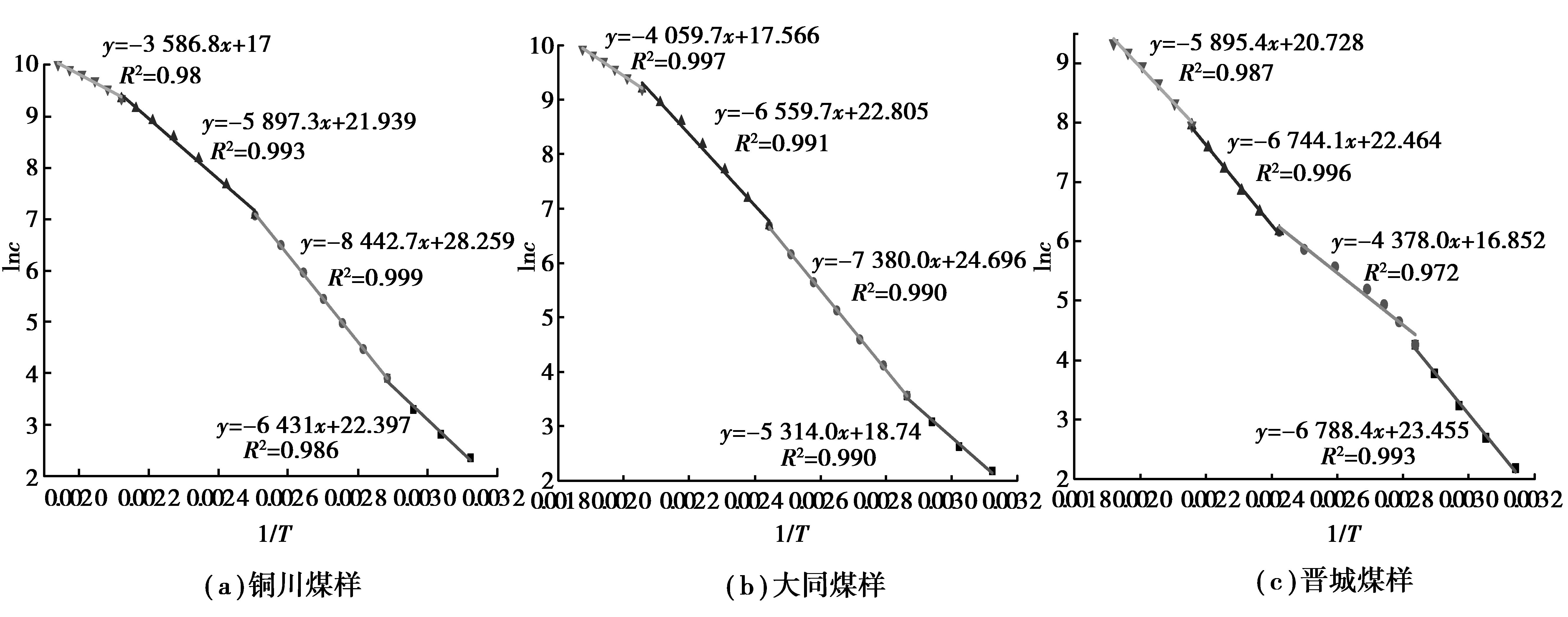
图 3 3种煤样lnc与温度1/T的关系 Figure 3 The relationship between lnc and temperature 1/T of 3 coal samples |
由图 2可以看出,在升温过程中,3种煤样的CO体积分数随温度的升高近似呈指数型增加,但其变化规律显著不同。从室温到100 ℃左右,3种煤样生成CO量少且增加缓慢。之后随着温度的升高,特别当煤温达到120 ℃后,3种煤样反应生成CO量快速增加,说明煤样氧化反应加快,但3种煤样氧化过程中CO生成量确有显著差别,分别为铜川>大同>晋城煤样。同时从图中可以看出,3种煤样CO急剧增大的温度拐点分别为100,120,160 ℃,可见随着煤自燃倾向性减弱,该拐点温度越高。
从图 3中可见,整个程序升温过程中,3种煤样CO体积分数的变化随温度的升高存在明显的阶段性。通过对铜川、大同、晋城煤样不同氧化阶段lnc与1/T线性拟合,得出各氧化阶段线性函数之间的交点,即3种煤样CO体积分数发生变化的氧化特征温度点,如表 2所示。3种煤样从室温开始,随着温度的升高,反应生成CO量分别按照一定的速率增大,其中晋城煤样CO增速最大。当煤温达到各自第1个温度拐点即临界温度时,CO体积分数发生突变,其中铜川和大同煤样CO增速增大,表明其氧化反应速率加快,且铜川煤样快于大同煤样。此阶段晋城煤样CO增速变缓,与下图 5(a)此温度段的出口氧气体积分数略微升高相吻合,表明其氧化反应速率相比前两种煤样较慢。当达到第2个温度拐点即干裂温度时,CO体积分数再次发生突变,之后前2种煤样CO增速开始减缓,表明煤已进入高温阶段,煤分子中各有机结构均发生不同程度地干馏、断裂和裂解,并与氧发生反应生成烷烃、烯烃类气体。晋城煤样CO增速却开始快速增大,煤分子中各官能团与氧气发生剧烈反应,氧化反应速率不断增强。当到达第3个温度拐点即活性温度时,CO体积分数再次发生突变,3种煤样CO增速快速减小。其中铜川和大同煤样CO增速最快发生于临界温度到干裂温度阶段,而晋城煤样则为干裂温度到活性温度阶段;同时3种煤样到达各自活性温度后,CO增速呈现出降低的趋势。
| 表 2 3种煤样氧化变化的拐点温度 Table 2 The inflection temperatures of 3 coals oxidation change |
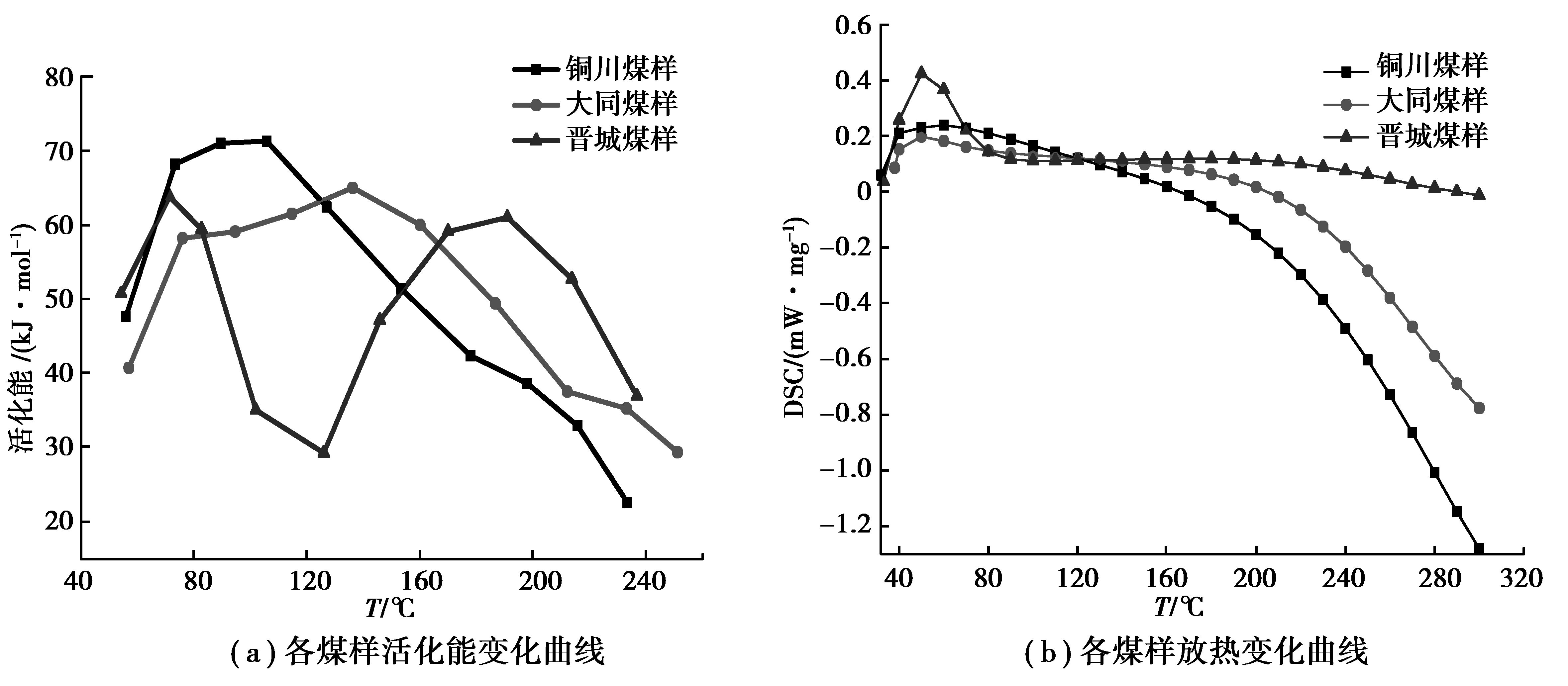
升温氧化过程中,3种不同自燃性煤表观活化能变化规律存在显著差异,如图 4(a)所示。易自燃和自燃煤样表观活化能变化规律相同,随着温度的升高,活化能经历先增大后减少的过程,但在各个温度阶段,活化能大小却有明显的不同,其中2种煤样活化能最大点温度段分别为90~110 ℃、120~140 ℃。不易自燃煤样随着温度的升高,活化能先减少后增大再减少,活化能最大2个温度段分别为60~80 ℃和180~200 ℃,同时在100~140 ℃阶段内,活化能达到整个氧化实验最低点。同时从图中可以看出,3种煤样的温度达到活性温度后,活化能迅速减少,需要外界提供的能量减少,氧化反应更加容易进行,温度对其氧化反应速率的影响已减弱。同时为了考察3种煤样自燃氧化过程中的放热特征,确定煤表观活化能变化规律,通过热重-差示扫描量热实验得到3种煤样的放热量曲线,如图 4(b)所示。刚开始氧化反应时,3种煤样均处于吸热状态,其中晋城煤样吸热量最大,其次为铜川和大同煤样,表现为初期氧化表观活化能较大。随着温度的升高,氧化放热的增强,晋城煤样吸热量快速降低,活化能减少,而铜川和大同煤样相对较缓慢,两种煤样表观活化能增大。之后铜川和大同煤样吸热量快速减少,活化能逐渐降低,直至转化为放热,其中两种煤样放热量变化曲线和活化能变化曲线的交叉点温度有着高度一致性。而晋城煤样在130 ~210 ℃左右氧化放热加强的同时,煤样的吸热量却缓慢增大,活化能增大,之后随着氧化反应放热量的增多,从外界吸收的热量缓慢减少,活化能逐渐降低。从图中可以看出,3种煤样初始放热温度分别为170,200,280 ℃左右,可见随着自燃倾向性增强,其温度逐渐降低,其中铜川和大同煤样的温度到达活性温度时,2种煤样已开始放热。
|
图 4 3种煤样活化能和放热量随温度变化规律 Figure 4 The change law of activation energy and heat of 3 coal samples during heating process |
3 种煤样低温氧化过程中各阶段表观活化能的不同,表明煤中活化物质和官能团的活性不同[18],即官能团氧化反应的难易程度不同,同时也表明同一官能团在不同自燃性煤样中发生氧化的温度有所不同。这主要因为煤的主体结构的不同,进而通过主体结构影响官能团的氧化性。不同煤体中不同官能团需要不同的能量才能被激活参与氧化反应,需要吸收的热量越多,活化能表现越大,同时氧化反应放出热量使煤体温度升高。当煤体温度升高到一定程度时,煤中的活性物质与官能团更容易被活化,需要外界能量就越小,当氧化反应放出的能量可以激活煤自身的活性结构参与反应的时候,活化能快速降低,煤开始进入自发氧化阶段。根据图 3所计算出的特征温度和活化能可把3种煤样的低温氧化过程分为四个阶段,具体温度段和活化能大小如表 3所示。通过表 3可以看出,3种煤样的温度达到活性温度即195,204,216 ℃后,活化能快速减少。同时根据DSC曲线图 4(b),各煤样到达各自活性温度后,放热量逐渐增大,氧化反应更加容易,其中铜川和大同煤样开始进入自发氧化阶段。
| 表 3 3种煤样氧化阶段的划分 Table 3 The division of oxidation stage of three coal samples |
根据上述实验过程和方法,可获得3种不同自燃倾向性煤在35~260 ℃间出口O2体积分数以及各温度的耗氧量,如图 5(a)所示。同时根据计算模型中的假设,可推导出煤的耗氧速率VO2(T)[19]计算公式如下:
| ${{V}_{\text{O}2}}(T)=(Q{{C}_{in}}/\left( SL \right))\text{ln}({{C}_{in}}/{{C}_{out}}),$ | (7) |
式中:VO2(T)为温度为T时煤的耗氧速率,mol/(cm3·s);Cin为进口处氧气体积分数,Cin=20.96%;Cout为出口氧气体积分数,%;将检测出的Cout和其他参数带入式(7) 中,计算出各个温度下3种煤样的耗氧速率,如图 5(b)所示。
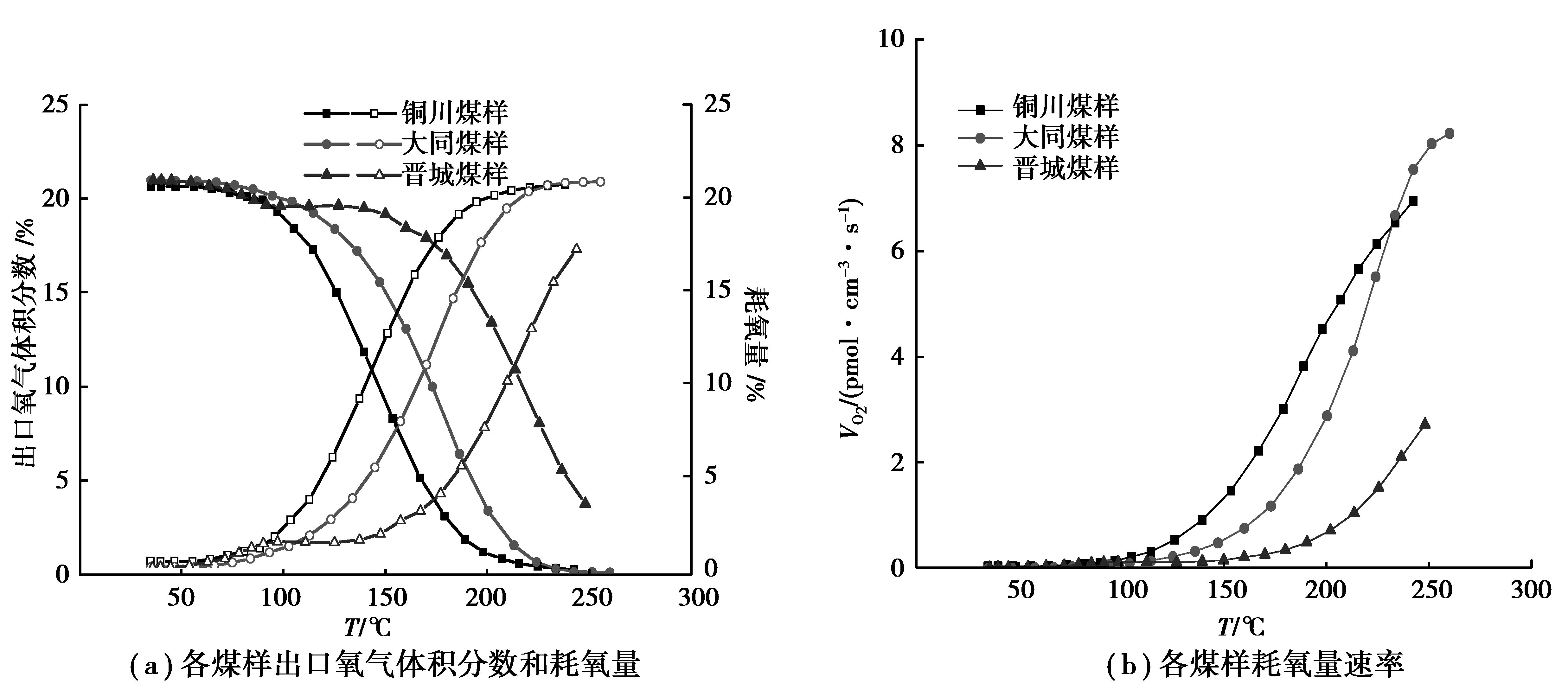
通过图 5(a)可见,不同自燃性煤出口氧气体积分数与耗氧量随温度的升高存在显著的差异。表面氧化阶段,3种煤样耗氧量小且增长缓慢,之后随着温度的升高,氧化反应加强,易自燃和自燃的铜川与大同煤样出口氧气体积分数随温度升高近似呈负指数减少,耗氧量呈指数增加,且在氧化自热和加速氧化阶段,铜川煤样耗氧量明显快于大同煤样,但在深度氧化阶段,两种煤样的耗氧量出现交叉。不易自燃晋城煤样耗氧量先是增加,在氧化自热阶段,耗氧量出现缓慢减少,说明此阶段晋城煤样的氧化反应速率没有前两种煤样快,之后随着温度升高,耗氧量快速增加。同时结合图 2和图 5(b)可知,不同煤样在实验过程中出现同样的CO生成量与耗氧速率急剧增加的温度拐点,针对3种煤样分别为100,120,160 ℃,当煤温超过温度拐点,氧化反应加快,耗氧速率和CO生成量增长极快。
|
图 5 3种煤样升温过程中耗氧量和耗氧速率 Figure 5 Oxygen consumption rate and oxygen consumption of 3 coal samples |
通过对3种不同自燃性煤进行自燃氧化实验,求解活化能和特征温度,并分析了不同自燃性煤低温氧化特性和活化能变化规律,可得出以下结论:
1) CO体积分数随着煤温升高而增大,其变化存在明显的阶段性和差异性,且阶段交点温度为煤氧化进程的特征温度点。易自燃(铜川)与自燃煤样(大同)在临界温度到干裂温度阶段CO增速最快,而不易自燃煤样(晋城)则发生于干裂温度到活性温度阶段,可见随着煤自燃倾向性减弱,CO最快增速温度从低温向高温移动。
2) 不同自燃性煤低温氧化阶段活化能变化规律存在显著差异。易自燃(铜川)与自燃煤(大同),随着煤温升高活化能先增大后减少,但其大小在各氧化阶段不同,不易自燃煤(晋城)活化能变化较复杂,经历先减少后增大再减少过程。其中各不同自燃性煤分别在90~110 ℃、120~140 ℃(氧化自热期)和180~200 ℃(加速氧化期),活化能达到最大,之后当其煤温到达活性温度后,活化能快速减少。同时结合热分析实验确定了煤活化能变化规律。
3) 低温氧化阶段,煤的耗氧量和耗氧速率随着自燃倾向性增强而增大。同时CO生成量与耗氧速率急剧上升的温度拐点相同,且不同自燃性煤的温度拐点不同,拐点温度越高,表明煤的初期氧化能力越弱。
| [1] |
李林, BB Beamish, 姜德义.
煤自然活化反应理论[J]. 煤炭学报, 2009, 34(4): 505–508.
LI Lin, B B Beamish, JIANG Deyi. Self-activation theory of spontaneous combustion of coal[J]. Journal of China Coal Society, 2009, 34(4): 505–508. (in Chinese) |
| [2] |
秦波涛, 王德明, 李增华, 等.
以活化能的观点研究煤炭自燃机理[J]. 中国安全科学学报, 2005, 15(1): 11–13.
QIN Botao, WANG Deming, LI Zenghua. Study on the mechanism of coal spontaneous combustion with activated energy view[J]. China Safety Science Journal, 2005, 15(1): 11–13. (in Chinese) |
| [3] |
王兰云, 蒋曙光, 邵昊, 等.
煤自燃过程中自氧化加速温度研究[J]. 煤炭学报, 2011, 36(6): 989–992.
WANG Lanyun, JIANG Shuguang, SHAO Hao. Self-accelerating oxidation temperature during spontaneous combustion of coal[J]. Journal of China Coal Society, 2011, 36(6): 989–992. (in Chinese) |
| [4] |
陆伟, 胡千庭, 仲晓星.
煤自燃逐步自活化反应理论[J]. 中国矿业大学学报, 2007, 36(1): 111–115.
LU Wei, HU Qianting, ZHONG Xiaoxing. Gradual self-activation reaction theory of spontaneous combustion of coal[J]. Journal of China University of Mining and Technology, 2007, 36(1): 111–115. (in Chinese) |
| [5] |
屈丽娜. 煤自燃阶段特征及其临界点变化规律的研究[D]. 北京:中国矿业大学, 2013. QU Lina. The study on the characteristics of coal stage and the critical point variation of the spontaneous combustion[D]. Beijing:China University of Mining and Technology, 2013. (in Chinese) |
| [6] | Deng J, Xiao Y, Li Q W. Experimental studies of spontaneous combustion and anaerobic cooling of coal[J]. Fuel, 2015, 157: 261–269. DOI:10.1016/j.fuel.2015.04.063 |
| [7] |
谢振华, 金龙哲, 宋存义.
程序升温条件下煤炭自燃特性[J]. 北京科技大学报, 2003, 25(1): 12–14.
XIE Zhenhua, JIN Longzhe, SONG Cunyi. Coal spontaneous combustion characteristics at programmed temperatures[J]. Journal of University of Science and Technology Beijing, 2003, 25(1): 12–14. (in Chinese) |
| [8] |
朱红青, 王海燕, 宋泽阳.
煤绝热氧化动力学特征参数与变质程度的关系[J]. 煤炭学报, 2014, 39(3): 498–503.
ZHU Hongqing, WANG Haiyan, SONG Zeyang. The relationship between oxidation kinetics characteristic parameters of coaladiabatic progress and metamorphic degree[J]. Journal of China Coal Society, 2014, 39(3): 498–503. (in Chinese) |
| [9] | Fei Y, Aziz A A, Nasir S, et al. The spontaneous combustion behavior of some low rank coals and a range of dried products[J]. Fuel, 2008, 88(9): 1650–1655. |
| [10] | Avila C, Wu T, Lester E. Petrographic characterization of coals as a tool to detect spontaneous combustion potential[J]. Fuel, 2014, 125: 173–182. DOI:10.1016/j.fuel.2014.01.042 |
| [11] | Nimaje D S, Tripathy D P. Characterization of some Indian coals to assess their liability to spontaneous combustion[J]. Fuel, 2016, 163: 139–147. DOI:10.1016/j.fuel.2015.09.041 |
| [12] | Dai C S, Ma S J, Liu X P, et al. Study on the pyrolysis kinetics of blended coal in the fluidized-bed reactor[J]. Procedia Engineering, 2015, 102: 1736–1741. DOI:10.1016/j.proeng.2015.01.309 |
| [13] | Yangali P, Celaya A M, Goldfarb J L. Co-pyrolysis reaction rates and activation energies of West Virginia coal and cherry pit blends[J]. Journal of Analytical and Applied Pyrolysis, 2014, 108: 203–211. DOI:10.1016/j.jaap.2014.04.015 |
| [14] | Taraba B, Pavelek Z. Investigation of the spontaneous combustion susceptibility of coal using the pulse flow calorimetric method:25 years of experience[J]. Fuel, 2014, 125: 101–105. DOI:10.1016/j.fuel.2014.02.024 |
| [15] |
仲晓星, 王德明, 尹晓丹.
基于程序升温的煤自燃临界温度测试方法[J]. 煤炭学报, 2010, 35(suppl)): 128–131.
ZHONG Xiaoxing, WANG Deming, YIN Xiaodan. Test method of critical temperature of coal spontaneous combustion based on the temperature programmed experiment[J]. Journal of China Coal Society, 2010, 35(suppl)): 128–131. (in Chinese) |
| [16] |
国家安全生产监督管理总局. 煤自燃倾向性的氧化动力学测试方法非书资料:AQ/T1068-2008[S]. 北京:煤炭工业出版社, 2009. State Administration of Work Safety. Oxidation kinetics testing method for the propensity of coal to spontaneous combustion AQ/T1068-2008[S]. Beijing:China Coal Industry Publishing House, 2009.(in Chinese) |
| [17] |
王德明. 矿井火灾学[M]. 徐州: 中国矿业大学出版社, 2008.
WANG Deming. Mine fire[M]. Xuzhou: China University of Mining and Technology Press, 2008. (in Chinese) |
| [18] |
李林.煤自燃活化机理及自燃过程实验研究[D]. 重庆:重庆大学, 2008. LI Lin. Self-activation theory and process of spontaneous combustion of coal[D].Chongqing:Chongqing University, 2008. (in Chinese) |
| [19] |
文虎, 徐精彩, 葛玲梅, 等.
煤自燃性测试技术及数值分析[J]. 北京科技大学学报, 2001, 23(6): 499–501.
WEN Hu, XU Jingcai, GE Lingmei, et al. Technique of measurement and test of coal spontaneous combustion characteristic and Numerical analysis[J]. Journal of University of Science and Technology, 2001, 23(6): 499–501. (in Chinese) |
| [20] | Goldfarb J L, Ceylan S. Second-generation sustainability:application of the distributed activation energy model to the pyrolysis of locally sourced biomass-coal blends for use in co-firing scenarios[J]. Fuel, 2015, 160: 297–308. DOI:10.1016/j.fuel.2015.07.071 |
| [21] |
贾海林, 余明高, 徐永亮.
矿井气体CO成因类型及机理辨识分析[J]. 煤炭学报, 2013, 38(10): 1812–1818.
JIA Hailin, YU Minggao, XU Yongliang. Analysis on the genetic type and mechanism identification of carbon monoxide in the coal mine[J]. Journal of China Coal Society, 2013, 38(10): 1812–1818. (in Chinese) |
| [22] |
褚廷湘, 杨胜强, 孙燕, 等.
煤的低温氧化实验研究及红外光谱分析[J]. 中国安全科学学报, 2008, 18(1): 171–176.
CHU Tingxiang, YANG Shengqiang, SUN Yan, et al. Experiment study on low temperature oxidization of coal and it's infrared spectrum analysis[J]. China Safety Science Journal, 2008, 18(1): 171–176. (in Chinese) |
 2017, Vol. 40
2017, Vol. 40

