由于煤、石油、天然气等传统能源逐步枯竭,同时燃烧带来了严重的环境污染和温室效应,传统能源的清洁高效利用和新能源的研究开发变得急迫而重要。中国的主要能源来自煤的燃烧,煤直接燃烧会带来严重的环境危害,而且煤的利用效率也没有发挥到最大。如果将煤气化,得到的合成气的主要成分为H2和CO,还有不同量的稀释气体,如N2、CO2和H2O等[1],煤中的N和S气化之后合成氨可在燃烧之前对S进行回收[2],这样煤气化技术就将煤的直接燃烧转化为清洁可燃物为H2和CO组成的合成气的燃烧。生物质能具有分布广、可再生的优点[3],生物质气化减少了直接燃烧造成的污染,被认为是继煤、石油、天然气之后的第4大能源。生物质气化产物由H2、CO、CO2、CH4、N2等组成的合成气,而不同的气化方式各气体组分的含量不同,但主要的可燃成分为H2和CO。无论是煤或生物质,由于煤种和生物质种类及气化方式的不同,气体组分复杂,且含有大量的稀释气(N2和CO2等),热值很低,为4~13 MJ/m3,远低于甲烷的36 MJ/m3,其稳定燃烧难度较大。而且,合成气中含有大量的氢,具有更快的燃烧速度、更大的化学反应速率和更高的火焰温度[4],因此,了解合成气的燃烧特性,对于煤的高效清洁利用及生物质能的发展起着重要的作用。
合成气燃烧技术主要分为稀释旋流扩散燃烧以及预混燃烧这2种方式。相较于扩散燃烧而言,贫燃料预混燃烧过程具有更高的能源利用效率以及更低的污染物排放的特点[5]。但是,预混燃烧过程比扩散燃烧更容易出现脱火或者回火,制约了其在工程上的广泛运用。火焰传播速度,作为评判脱火与回火极限的重要指标,是火焰燃烧特性中不可忽略的重要因素。因此,对火焰传播速度的测量是合成气利用过程必不可少的步骤。本生灯法,是最简单、最成熟的稳定预混燃烧方法,它在合成气燃烧火焰的研究中具有独特优点。但精确测量火焰传播速度,还存在一定的难度。
文中利用多种生物质气化合成气,在当量比(化学当量空燃比/实际燃烧空燃比)0.6~1.2进行预混燃烧,采用PLIF技术(平面激光诱导荧光显示技术),利用获取的OH基浓度分布图,精确提取火焰前锋面,结合面积法对合成气燃烧速度进行研究。采用CHEMKIN软件模拟,对燃烧过程的化学反应机理进行了探讨。
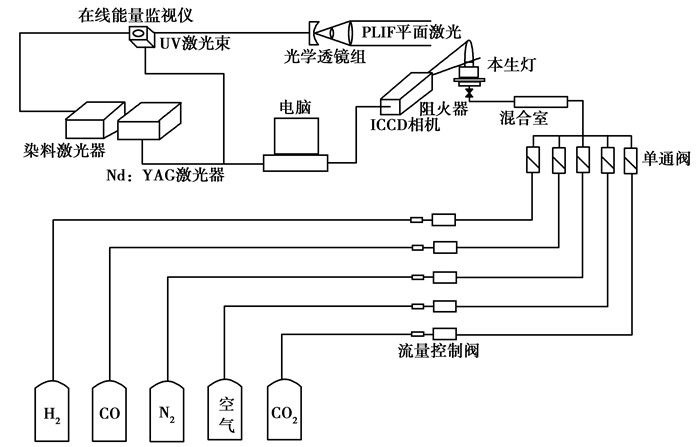
1 实验系统及研究方法 1.1 PLIF系统实验采用PLIF来测量合成气燃烧过程中的OH分布,实验系统如图 1所示。
|
图 1 实验系统原理图 Figure 1 The schematic of experimental system |
实验所用的PLIF设备全部由德国Davis公司提供,YAG激光器激发的激光初始波长为1 064 nm,经1/2玻片和THG倍频晶体,叠加之后输出波长为355 nm的泵浦激光,脉冲频率为10 Hz,单个脉冲功率为270 mJ以上。染料激光器为德国Sirah公司制造,2个染料泵使用一定浓度的coumarin153-乙醇稀释液作为染料介质,YAG激光器出来的激光在染料激光器中经过光栅精细调谐、染色后再经过倍频晶体倍频为波长283.55 nm的激光,经柱面镜转化为平面激光后,穿过燃烧器中心。燃烧火焰中的OH基接收激光能量后,发生跃迁处于不稳定状态,会自动跌落为基态,此过程会发射出特定波长的荧光,通过安装有OH基过滤镜片的ICCD相机接收荧光信号。ICCD相机通过数据线和电脑相连,采用Davis软件处理后可以直接测量到燃烧过程中火焰的OH基浓度二维分布。
1.2 燃烧器及气体管路由于H2、CO都属于易燃易爆气体,为保证预混燃烧过程安全,在燃烧器入口安装阻火器和单向阀。阻火器可有效防止管路回火爆炸,单向阀确保高温气体不会回流到混合室。燃烧器为简单改装过的预混本生灯,燃烧器的出口为内径为5 mm,高度为260 mm的不锈钢管。为保证层流燃烧,燃烧器出口雷诺数恒定为1 000。
研究中,合成气初始成分根据生物质气化相关文献[6-12]进行确定。为了清楚地了解燃烧过程中各个气体成分之间的相互影响,将合成气中的CH4按照C、H元素和O元素结合变成稳定产物CO2和H2O的比例加入到合成气H2和CO中。实验所用生物质合成气组分见表 1。
| 表 1 合成气成分(体积百分数) Table 1 compositions of syngas (volume percentage) |
层流火焰速度是指沿火焰面法线方向上平面火焰锋面向未燃气体的传播速度。本生灯计算火焰传播速度是目前计算火焰速度较为简单而且应用较多的一种方法。计算本生灯火焰速度的方法有角度法和面积法,角度法计算较简单但是准确度不高,为了获取更加精确的计算结果,文中采用面积法进行分析。
面积法计算火焰速度可近似于一维反应区火焰速度,火焰速度可由式(1) 计算[13]:
| $ S_b^0 = \frac{Q}{{{A_b}}}, $ | (1) |
式中:Q表示未燃预混气体的体积流量;Ab表示火焰前锋面的面积。
由于火焰前锋面面积难以求取,成为研究过程的难点。而近年来PLIF技术的发展,为精确求取火焰前锋面面积提供了可能性。利用PLIF系统拍摄的OH基浓度分布图,结合Davis软件将前锋面处OH基浓度梯度最高的点确定为前锋面位置,并利用origin软件对这些点坐标进行拟合,将前锋面曲线用多项式表示出来:
| $ f\left( x \right) = \sum\limits_{i = 0}^n {{a_i}{x^i}}, $ | (2) |
式中,x坐标为燃烧器出口轴线方向。再根据旋转曲面的表面积计算公式对前锋面曲线积分可以计算出火焰前锋面的表面积,计算公式为
| $ {A_b} = \int_0^t {2{\rm{\pi }} \cdot f\left( x \right) \cdot \sqrt {1 + {{\left[{f'\left( x \right)} \right]}^2}} {\rm{d}}x} 。 $ | (3) |
将式(1)~式(3) 联立,利用面积法精确计算出层流本生火焰的传播速度Sb0。
1.4 CHEMKIN模拟设置CHEMKIN软件已经广泛应用到甲烷、合成气等气体燃烧的数值模拟[14-16],实验证明,CHEMKIN软件对气体燃烧过程中的温度场、速度场、组分计算以及化学动力学分析具有较高的准确性。利用CHEMKIN软件中的预混燃烧模型,对实验工况进行模拟。实验在常温、常压的情况下进行,模拟过程中气体的初始温度为298 K,压力为0.101 3 MPa,采用自动建立温度文件方式。
2 实验结果及分析 2.1 合成气火焰OH分布图 2为1-8组合成气在当量比为1.0时燃烧的火焰实物图及OH浓度分布图,实物图通过固定位置和焦距的数码相机拍摄获得。

|
图 2 当量比为1.0时,1-8组合成气燃烧火焰OH浓度分布及实际火焰图 Figure 2 The images of OH distribution and flames of the syngas at the equivalence ratio of 1.0 |
当量比为1.0时OH基浓度不高,是因为在理论燃-空比的情况下反应区域增大使得OH基在燃尽区内反应时生成的热量和放出的热量保持在一个相对比较平衡的状态,因此,燃尽区比较大。图 2(a)为1-3组合成气,而且H2比例逐渐增大、CO比例增大、CO2量减小。随着H2含量的增加,火焰的内焰高度逐渐降低,由于H2扩散作用的影响,外焰OH基浓度也在增大。火焰结构随着CO含量的增加而变小。图 2(b)为4-5组合成气,其H2比例变化不大,但CO比例减小,CO2量增大。随着CO含量的减少,合成气内焰高度有所增加,但并没有H2含量变化对内焰高度影响那么明显。图 2(c)为6-8组中合成气,成分增加了N2,而且H2比例增加、CO比例增加、CO2比例减小、N2比例减小。N2的加入,使得合成气火焰中OH基浓度明显降低,火焰宽度随着N2含量的减少而增加。其主要原因为,N2加入虽不参与反应,但会降低合成气热值,并带走大量的热量,使得火焰温度降低,降低了OH基的生成速率。
2.2 燃烧速度分析文中通过实验计算和CHEMKIN模拟研究了合成气1-8的火焰传播速度。
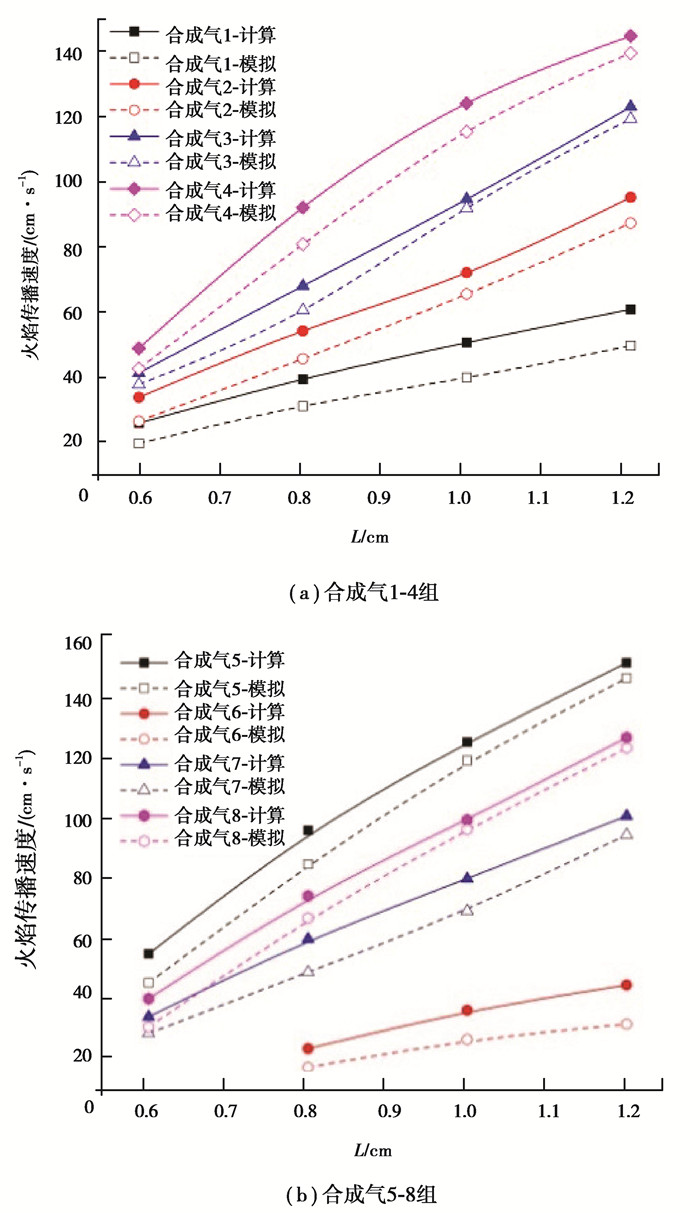
从图 3可以看出,合成气模拟的结果和实验计算的结果吻合度较好,由于本生灯管口加热的影响,实验计算的结果总是略大于模拟的结果。这是因为,本生灯出口温度升高会直接导致未燃合成气流经此管段时被加热,使得燃料更快达到着火温度,实际燃烧过程的火焰传播速度增加,但模拟过程设置的气流初始温度为常温。可以看出合成气在燃烧过程中火焰传播速度是随当量比的增加而增加的,合成气5(50%H2-33%CO-17%CO2)和合成气4(45%H2-45%CO-10%CO2)的火焰传播速度始终要大于其它合成气的传播速度。这2组气体中H2和CO的比例都较高,但是相比于合成气3(34%H2-62%CO-4%CO2),合成气5和4的CO比例远低于合成气3,CO2的比例高于3,但是火焰传播速度却远大于3,这说明合成气中H2的体积分数对火焰的传播速度影响较大。合成气1(20%H2-37%CO-43%CO2)和合成气6(20%H2-12%CO-21%CO2-47%N2)中的H2浓度都为20%,合成气6的火焰传播速度小于合成气1,主要是由于合成气6中不可燃气体比例较大,影响了火焰的传播速度。
|
图 3 合成气预混燃烧火焰传播速度计算与模拟结果对比图 Figure 3 The burning velocity of syngas-air mixture measured by experiments and simulations |
各合成气在当量比为0.6时火焰传播速度差别不大,但是当量比增大,各合成气燃烧火焰传播速度差距变大,这也解释了在当量比较小的情况下OH基浓度在内封面比较集中的原因,而当量比增大,火焰传播速度增大,在外焰处OH基浓度较大。因此,合成气火焰传播速度随当量比的增大而增大,而且增大的幅度随H2比例增大而增加。
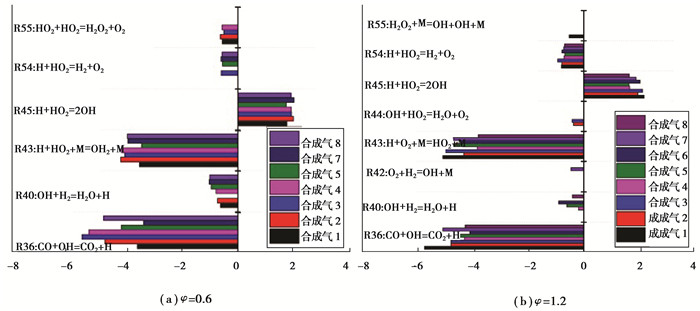
2.3 CHEMKIN模拟结果及化学动力学分析从图 4(a)可以看出在当量比为0.6时对合成气燃烧OH级生成影响比较大的反应主要有R36、R40、R43和R45,其中除R45:H+HO2=2OH是生成OH基,敏感性系数为正以外,其余反应的敏感性系数皆为负数,而且反应R36:CO+OH=CO2+H有CO的直接参与,因此对合成气3的影响最大,而反应R45对各合成气的敏感性系数非常接近。当量比增加到1.2时R45的敏感性系数进一步增大,但是R36的敏感性系数在数值上减小,因此造成OH基浓度的增加在当量比为1.2时达到最大。
|
图 4 合成气燃烧生成OH基敏感性分析 Figure 4 The sensitivity analysis on the formation of OH radicals |
根据敏感性分析可知,对合成气燃烧过程中OH基生成具有较大影响的是R36: CO+OH=CO2+H、R43:H+O2+M=HO2+M和R45:H+HO2=2OH这3个基元反应。CO对合成气燃烧过程中OH生成具有重要影响,主要由于CO的加入促进了基元反应R36:CO+OH=CO2+H的发生,R45:H+HO2=2OH随当量比的增加敏感性系数增大,因此合成气的OH基浓度在当量比为1.2时浓度达到最大;R43:H+O2+M=HO2+M虽然在反应过程中没有OH直接参与,但是反应的中间产物对OH基生成有较大影响。
3 结论经过对多种生物质气化合成气燃烧特性的测量,为合成气的工业运用奠定了一定基础。研究结果表明,合成气中H2含量的增加,会使火焰内焰高度降低。但H2成分一定时,CO含量的变化,对火焰内焰高度影响不大。而N2的加入会直接降低火焰温度,从而降低OH基的生成速率。合成气火焰传播速度随当量比的增大而增大,而且增大的幅度随合成气中H2比例的增大而增加。燃烧过程决定OH基生成的主要步骤是R36: CO+OH=CO2+H、R43:H+O2+M=HO2+M和R45:H+HO2=2OH这3步。
| [1] |
王辅臣, 于广锁, 龚欣, 等.
大型煤气化技术的研究与发展[J]. 化工进展, 2009, 28(2): 173–180.
WANG Fuchen, YU Guangsuo, GONG Xin, et al. Research and development of large-scale coal gasification technology[J]. Chemical Industry and Engineering Progress, 2009, 28(2): 173–180. (in Chinese) |
| [2] | 高聚忠. 煤气化技术的应用与发展[J]. 洁净煤技术, 2013, 19(1): 65–71. |
| [3] |
赵连臣, 李晓伟, 王责路, 等.
生物质气化的应用与研究[J]. 可再生能源, 2008, 26(6): 55–58.
ZHAO Lianchen, LI Xiaowei, WANG Zelu, et al. The research and utilization on biomass gasification[J]. Renewable Energy Resources, 2008, 26(6): 55–58. (in Chinese) |
| [4] |
郭培卿, 臧述升, 葛冰.
合成气燃烧数值模拟与验证[J]. 计算机与应用化学, 2014, 31(1): 1–4.
GUO Peiqing, ZANG Shusheng, GE Bing. Numerical simulation and validation of syngas combustion[J]. Computers and Applied Chemistry, 2014, 31(1): 1–4. (in Chinese) |
| [5] | Fu J, Tang C, Jin W, et al. Study on laminar flame speed and flame structure of syngas with varied compositions using OH-PLIF and spectrograph[J]. International Journal of Hydrogen Energy, 2013, 38(3): 1636–1643. DOI:10.1016/j.ijhydene.2012.11.023 |
| [6] |
陈冠益, 高文学, 颜蓓蓓, 等.
生物质气化技术研究现状与发展[J]. 煤气与热力, 2006, 26(7): 20–26.
CHEN Guanyi, GAO Wenxue, YAN Beibei, et al. Present research status and development of biomass gasification technologies[J]. Gas and Heat, 2006, 26(7): 20–26. (in Chinese) |
| [7] |
张亚宁, 李炳熙, 张波, 等.
生物质氧气气化和水蒸汽气化的能量分析及火用分析[J]. 华北电力大学学报(自然科学版), 2012, 39(1): 64–69.
ZHANG Yaning, LI Bingxi, ZHANG Bo, et al. Energy and exergy analysis of biomass gasification with oxygen or steam[J]. Journal of North China Electric Power University(Natural Science Edition), 2012, 39(1): 64–69. (in Chinese) |
| [8] | Gao N, Li A, Quan C, et al. Hydrogen-rich gas production from biomass steam gasification in an updraft fixed-bed gasifier combined with a porous ceramic reformer[J]. International journal of hydrogen energy, 2008, 33(20): 5430–5438. DOI:10.1016/j.ijhydene.2008.07.033 |
| [9] |
应浩, 涂军令, 江俊飞, 等.
木屑高温水蒸气气化制备合成气研究[J]. 太阳能学报, 2014, 35(3): 379–383.
YING Hao, TU Junling, JIANG Junfei, et al. Production of synthesis gas by high temperature steam gasification of sawdust[J]. Acta Energiae sloris Sinica, 2014, 35(3): 379–383. (in Chinese) |
| [10] | Tinaut F V, Melgar A, Perez J F, et al. Effect of biomass particle size and air superficial velocity on the gasification process in a downdraft fixed bed gasifier. An experimental and modelling study[J]. Fuel Processing Technology, 2008, 89(11): 1076–1089. DOI:10.1016/j.fuproc.2008.04.010 |
| [11] |
付鹏, 向军, 张安超, 等.
生物质空气-水蒸气催化气化制氢技术[J]. 化工时刊, 2006, 20(11): 55–58.
FU Peng, XIANG Jun, ZHANG Anchao, et al. Catalytic gasification of biomass with air-steam to produce hydrogen[J]. Chemical Industry Times, 2006, 20(11): 55–58. DOI:10.3969/j.issn.1002-154X.2006.11.019 (in Chinese) |
| [12] | Zhou J, Chen Q, Zhao H, et al. Biomass-oxygen gasification in a high-temperature entrained-flow gasifier[J]. Biotechnology advances, 2009, 27(5): 606–611. DOI:10.1016/j.biotechadv.2009.04.011 |
| [13] | Bouvet N, Chauveau C, G kalp I, et al. Characterization of syngas laminar flames using the Bunsen burner configuration[J]. International Journal of Hydrogen Energy, 2011, 36(1): 992–1005. DOI:10.1016/j.ijhydene.2010.08.147 |
| [14] | Natarajan J, Lieuwen T, Seitzman J. Laminar flame speeds of H2/CO mixtures:Effect of CO2 dilution, preheat temperature, and pressure[J]. Combustion and Flame, 2007, 151(1/2): 104–119. |
| [15] | Ouimette P, Seers P. Numerical comparison of premixed laminar flame velocity of methane and wood syngas[J]. Fuel, 2009, 88(3): 528–533. DOI:10.1016/j.fuel.2008.10.008 |
| [16] | Ai Y, Zhou Z, Chen Z, et al. Laminar flame speed and Markstein length of syngas at normal and elevated pressures and temperatures[J]. Fuel, 2014, 137(6): 339–345. |
 2017, Vol. 40
2017, Vol. 40

