b. 重庆大学 低碳绿色建筑国际联合研究中心, 重庆 400045
b. National Centre for International Research of Low-carbon and Green Buildings, Chongqing University, Chongqing 400045, P. R. China
铬广泛的应用于电镀、皮革鞣制加工和金属表面处理等行业[1-3]。铬的主要存在形式为Cr (Ⅲ)和Cr (Ⅵ)。Cr (Ⅵ)具有极大的危害性,其毒性是Cr(Ⅲ)的500倍[2],不仅会对环境造成严重的污染,还会对人体产生致癌作用,所以解决水体铬污染问题刻不容缓[1-3]。目前,去除水体Cr (Ⅵ)的技术主要有化学沉淀法、离子交换法、光催化还原、膜分离法、吸附法等。其中,吸附法因其净化效果好、可再生、无二次污染等优点,成为水体重金属治理最具前景的技术之一[3-4]。
中国是茶叶的发源地,茶产量居世界第一位,但是茶加工过程产生的大量茶废弃物并未得到充分利用[5]。茶梗,是指茶叶的叶梗,特指从成品茶中挑拣出来的叶梗,最常见的是铁观音茶梗[6]。铁观音茶梗是茶叶废弃物的重要组成部分,含有丰富的茶多酚、茶皂素、咖啡碱、嘌呤碱和氨基酸等成分[7],这些物质能够和重金属离子发生氧化还原、吸附和络合作用,从而实现水体重金属的净化与去除[8-10]。目前,国内外有许多学者研究了原茶[7, 11-12]、废弃茶叶渣[13-17]、改性茶渣[18-22]对水中重金属的去除,但是直接用铁观音茶梗还原吸附去除水中Cr (Ⅵ)离子的相关内容未见报道。笔者致力于为水体中重金属Cr (Ⅵ)的去除提供一种新思路,同时期望实现大量废弃茶梗的资源化再利用,达到以废治废、变废为宝的目的。
1 材料与方法 1.1 主要仪器与试剂752N紫外可见分光光度计;SHZ-82A气浴恒温振荡器;ML-800高速多功能粉碎机;JF1004电子天平;1ESCALAB250Xi X射线光电子能谱仪;Mira3 LMH场发射扫描电镜;5DXC FTIR红外分光光度计;ASAP 2020M+C物理化学吸附分析仪;LA-p H10 pH计;01A-1E电热鼓风干燥箱等。
重铬酸钾(K2Cr2O7)、二苯碳酰二肼(C13H14N4O)、浓硫酸(H2SO4)、磷酸(H3PO4)、丙酮(CH3COCH3)、氢氧化钠(NaOH)、盐酸(HCl)、甲醛(CH2O)和硫化钠(Na2S)等,以上试剂均为分析纯。本实验用水为去离子水。此外还有活性炭、铁观音茶梗(原产地福建安溪)和普洱茶茶梗(原产地云南)。
1.2 Cr(Ⅵ)模拟废水的配制用去离子水溶解2.829 g K2Cr2O7后,于1 000 mL容量瓶中定容得到质量浓度为1 000 mg/L的Cr(Ⅵ)标准贮备液。后续实验中所需不同质量浓度的Cr(Ⅵ)溶液,均采用该贮备液定量稀释得到。
1.3 吸附剂的制备铁观音茶梗:将铁观音茶梗原材料在105 ℃下烘干6 h至恒重。再将烘干的茶梗用粉碎机粉碎成较小的粒径,分别过60,80,100,120目的筛子,然后将不同粒度的茶梗粉末分别置于封口袋内,储存于冰箱中备用。除特别说明是普洱茶梗外,本文中的茶梗均指铁观音茶梗。
普洱茶茶梗制备:将普洱茶茶梗原材料在105 ℃下烘干6 h至恒重,再将烘干的茶梗用粉碎机粉碎成较小的粒径,然后取80~100目筛子之间的粉末,置于封口袋内,储存于冰箱中备用。
甲醛改性茶梗:取铁观音茶梗粉末2 g,加入40 mL的0.1 mol/L的H2SO4,再加入10 mL的甲醛溶液,于60 ℃的气浴振荡器振荡2 h,使其充分接触,然后抽滤,经多次水洗至中性,移至105 ℃烘箱下干燥6 h,置于封口袋内,储存于冰箱中备用。
硫化钠改性茶梗:取铁观音茶梗粉末2 g,加入50 mL的1 mol/L Na2S溶液,于60 ℃的气浴振荡器振荡2 h,使其充分接触,然后抽滤,经多次水洗至中性,移至105 ℃烘箱下干燥6 h,置于封口袋内,储存于冰箱中备用。
氢氧化钠改性茶梗:取铁观音茶梗粉末2 g,加入50 mL的1 mol/L的NaOH溶液,于60 ℃的气浴振荡器振荡2 h,使其充分接触,然后抽滤,经多次水洗至中性,移至105 ℃烘箱下干燥6 h,置于封口袋内,储存于冰箱中备用。
1.4 分析方法实验采用《水和废水监测分析方法》(第四版)中的二苯碳酰二肼法,即用紫外分光光度法测定Cr(Ⅵ)的吸光度,进而绘制Cr(Ⅵ)的标准曲线,然后通过标准曲线上吸光度对应的质量浓度值得到所测Cr(Ⅵ)质量浓度值。其原理为:在酸性溶液中,Cr(Ⅵ)与C13H14N4O反应生成紫红色化合物,可于波长540 nm处进行吸光度测定。
去除率计算公式:
| $ p = ({C_{\rm{e}}} - {C_{\rm{o}}})/{C_{\rm{e}}} \times 100\% 。$ | (1) |
吸附容量计算公式:
| $ {q_{\rm{e}}} = ({C_{\rm{e}}} - {C_{\rm{o}}}) \times V/m, $ | (2) |
式中:p为去除率;qe为平衡吸附容量,mg/g;V为重金属离子溶液的体积,L;m为吸附剂的投加量,g;Ce为吸附后达到平衡时的质量浓度,mg/L;Co为吸附前重金属离子的质量浓度,mg/L。
动力学采用准一级动力学模型和准二级动力学模型进行拟合。
准一级动力学模型方程:
| $ \lg ({q_{\rm{e}}} - {q_{\rm{t}}}) = 4{q_{\rm{e}}} - \frac{{{k_1}}}{{2.303}}t。$ | (3) |
准二级动力学模型方程:
| $ \frac{t}{{{q_t}}} = \frac{1}{{{k_2}q_{\rm{e}}^2}} + \frac{t}{{{q_{\rm{e}}}}}, $ | (4) |
式中:qe为吸附后达到平衡时的吸附容量,mg/g;qt为t时刻吸附剂的吸附容量,mg/g;k1为准一级动力学模型吸附速率常数,min-1;k2为准二级动力学模型吸附速率常数,min-1。
等温线采用Langmiur和Freundlich等温吸附模型进行拟合。
Langmiur等温吸附模型:
| $ \frac{{{C_{\rm{e}}}}}{{{q_{\rm{e}}}}} = \frac{{{C_{\rm{e}}}}}{{{q_{\rm{m}}}}} + \frac{1}{{{q_{\rm{m}}}b}}。$ | (5) |
Freundlich等温吸附模型:
| $ \ln {q_{\rm{e}}} = \frac{1}{n}\ln {C_{\rm{e}}} + \ln {K_{\rm{f}}}, $ | (6) |
式中:b、Kf均为吸附系数,mg/g;n为非均相因子,是受温度影响的常数;Ce为吸附后达到平衡时的质量浓度,mg/L;qe为吸附后达到平衡时的吸附容量,mg/g;qm为吸附剂表面所有位点均参与反应的吸附量, 即饱和吸附容量,mg/g。
2 结果与讨论 2.1 单因素对茶梗还原吸附Cr(Ⅵ)的影响 2.1.1 茶梗水溶液颜色对实验的影响茶梗水溶液具有浅颜色,讨论该颜色是否会对分光光度法产生影响十分必要[23]。分别称取0.3,0.5,1.0,1.5,2.0 g的茶梗粉末于250 mL锥形瓶中,加入50 mL去离子水,于转速为150 r/min、温度为30 ℃的气浴恒温振荡器中振荡2 h,然后抽滤,取1 mL滤液按照二苯碳酰二肼法测定其吸光度,如表 1所示。
| 表 1 茶梗水溶液颜色对分光光度法的影响 Table 1 The influence of the tea stalk color on the spectrophotometry |
由表 1可知,茶梗粉末量不超过2 g时,茶梗水溶液的吸光度值很小,最大仅为0.003。即认为本实验中茶梗水溶液颜色对分光光度法测定Cr(Ⅵ)质量浓度的影响基本可忽略不计。
2.1.2 茶梗粒径对还原吸附Cr(Ⅵ)的影响取50 mL初始质量浓度为50 mg/L的Cr(Ⅵ)溶液于250 mL的具塞玻璃锥形瓶中,用pH计测得此时pH≈5,分别投加粒径为≤60目,60~80目,80~100目,100~120目,≥120目的茶梗粉末0.50 g。将所有锥形瓶置于气浴恒温振荡器中,温度控制在30 ℃,转速定于150 r/min,振荡2 h后各取1 mL滤液测定Cr(Ⅵ)的剩余浓度并计算去除率和吸附容量,结果如图 1所示。
|
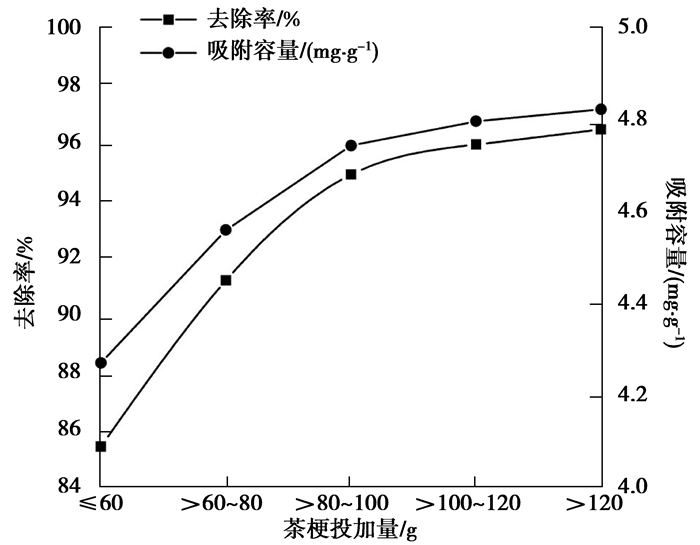
图 1 茶梗粒径对Cr(Ⅵ)去除率的影响 Figure 1 The influence of the tea stalk diameter to removal rate of Cr(Ⅵ) |
图 1表明,茶梗粒径对还原吸附水中Cr(Ⅵ)有明显的影响:茶梗粉末过筛的目数越大,即茶梗粉碎的越细小,茶梗的粒径越小,表面积越大,重金属离子与吸附位点相互作用的机会越大[24],则茶梗对Cr(Ⅵ)的去除率和吸附容量都越高。但茶梗粒径过大,易堵塞滤纸,后续固液分离困难,故本研究中采用过80~100目筛子的茶梗粉末,此时去除率仍达94.91%。
2.1.3 茶梗投加量对还原吸附Cr(Ⅵ)的影响取50 mL初始质量浓度为50 mg/L的Cr(Ⅵ)溶液于250 mL的具塞玻璃锥形瓶中,用pH计测得此时pH≈5,再分别投加0.1,0.2,0.3,0.4,0.5,0.6,0.7,0.8,0.9,1.0,1.2 g的吸附剂。然后将所有锥形瓶置于气浴恒温振荡器中,温度控制在30 ℃,转速定于150 r/min,振荡2 h后各取1 mL滤液测定Cr(Ⅵ)的剩余质量浓度并计算去除率和吸附容量,结果如图 2所示。
|
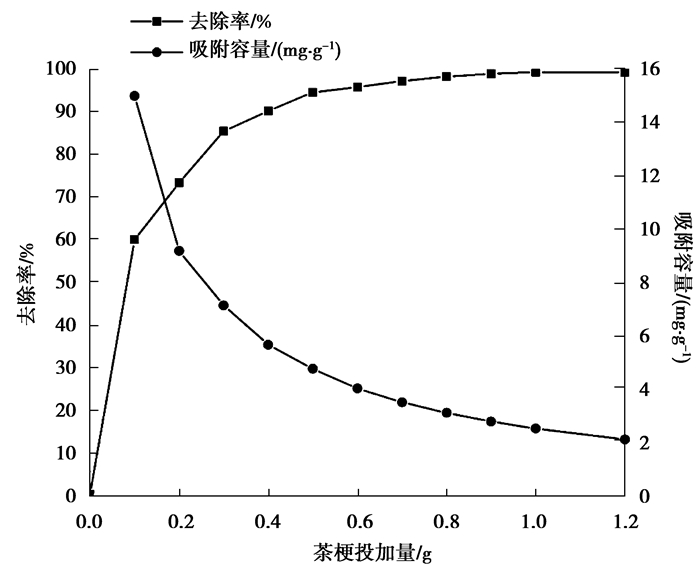
图 2 茶梗投加量对Cr(Ⅵ)去除率的影响 Figure 2 The influence of the tea stalk mass to removal rate of Cr(Ⅵ) |
图 2表明,Cr(Ⅵ)去除率随茶梗投加量的增大而增大,但吸附容量随茶梗投加量的增大而减小。这是因为随着吸附剂投加量的增加,吸附位点的数量也有所增加,吸附剂结合位点的可获得性增大,所以Cr(Ⅵ)去除率增大。然而吸附容量减小是因为高投加量时重金属浓度相对较低,吸附位点处于非饱和状态未被充分利用[24]。吸附剂用量小于0.5 g时,去除率增加速度较快,吸附剂用量大于0.5 g后,去除率增加缓慢,投加0.5 g茶梗粉末时,Cr(Ⅵ)去除率可达94.56%,故本实验最佳吸附剂用量取0.5 g。
2.1.4 初始pH对茶梗还原吸附Cr(Ⅵ)的影响取50 mL初始质量浓度为50 mg/L的Cr(Ⅵ)溶液于250 mL具塞玻璃锥形瓶中,用0.1 mol/L和1 mol/L的HCl或NaOH调节溶液pH值分别为2.13,3.05,4.37,5.23,6.45,7.11,8.21,9.08,10.29,11.03,12.11,13.01后,各自加入0.50 g吸附剂,然后将所有锥形瓶置于气浴恒温振荡器中,温度控制在30 ℃,转速定于150 r/min,振荡2 h后抽滤取1 mL滤液测定Cr(Ⅵ)的剩余质量浓度并计算去除率和吸附容量,结果如图 3所示。
|
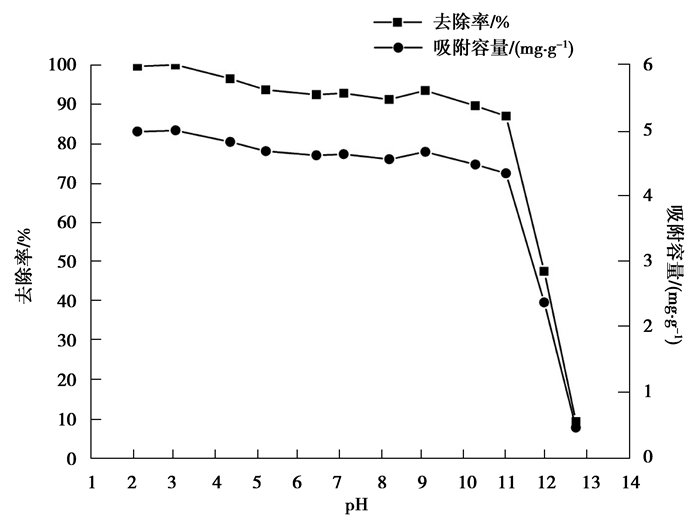
图 3 初始pH值对Cr(Ⅵ)去除率的影响 Figure 3 The influence of initial pH to removal rate of Cr(Ⅵ) |
图 3表明,溶液初始pH对茶梗还原吸附水中Cr(Ⅵ)有明显的影响:随着溶液初始pH值的增大,Cr(Ⅵ)的去除率和吸附容量均呈下降趋势。当pH≤11时,去除率和吸附容量下降缓慢;当pH>11时,去除率和吸附容量急剧下降。未经酸碱调节的Cr(Ⅵ)溶液原始pH约为5.23,此时的去除率仍可达到90%以上,所以本实验中其他单因素影响实验均采用此pH值。酸性和中性条件下,Cr(Ⅵ)在溶液中主要以Cr2O72-的形式存在,Cr2O72-具有氧化性,推测此时Cr(Ⅵ)去除率较高是因为茶多酚与Cr2O72-发生氧化还原反应[4, 10, 25],降低了溶液中Cr(Ⅵ)的质量浓度。
2.1.5 竞争离子对茶梗还原吸附Cr(Ⅵ)的影响本文中采用水体中常见的碱土离子Ca(Ⅱ)和工业废水重金属离子Ni(Ⅱ)分别作为竞争离子,研究共存离子的竞争吸附实验。取一定体积初始质量浓度不同的Cr(Ⅵ)溶液和一定体积初始质量浓度50 mg/L的Ni(Ⅱ)溶液混合于250 mL具塞玻璃锥形瓶中,并保证混合液总体积为50 mL且Cr(Ⅵ)质量浓度为50 mg/L,投加0.5 g的吸附剂。然后将所有锥形瓶置于气浴恒温振荡器中,温度控制在30℃,转速定于150 r/min,振荡2 h后各取1 mL滤液测定Cr(Ⅵ)的剩余质量浓度并计算去除率和吸附容量,结果如图 4所示。
|
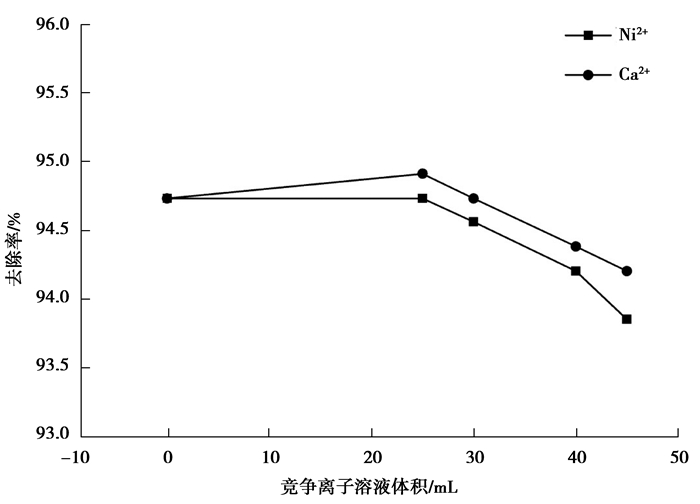
图 4 竞争离子不同溶度对Cr(Ⅵ)去除率的影响 Figure 4 The influence of different concentrations of competition ions to removal rate of Cr(Ⅵ) |
图 4表明,共存离子Ca(Ⅱ)离子和Ni(Ⅱ)离子对Cr(Ⅵ)去除率的影响不显著。当干扰离子体积达到45 mL(总体积50 mL)时,Cr(Ⅵ)去除率仅下降了0.88%。这说明茶梗几乎不能吸附Ca(Ⅱ)离子和Ni(Ⅱ)离子或者该吸附反应进行的十分缓慢,并进一步验证了茶梗对Cr(Ⅵ)有较高的去除率除了吸附作用外,氧化还原反应也起到了非常重要的作用。
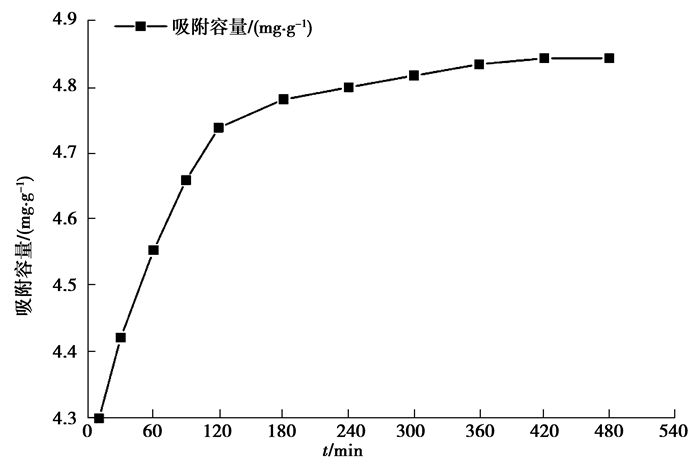
2.2 吸附动力学和吸附热力学的研究 2.2.1 吸附动力学取50 mL初始质量浓度为50 mg/L的Cr(Ⅵ)溶液于250 mL的具塞玻璃锥形瓶中,用pH计测得此时pH≈5,分别投加0.5 g的吸附剂。然后将所有锥形瓶置于气浴恒温振荡器中,温度控制在30 ℃,转速定于150 r/min,分别振荡10,30,60,90,120,180,240,300,360,420,480 min后各取1 mL滤液测定Cr(Ⅵ)的剩余质量浓度并且计算平衡质量浓度。用平衡吸附容量qe(mg/g)对吸附时间t作图,可得图 5所示动力学曲线。
|
图 5 动力学曲线 Figure 5 Kinetics curve |
由图 5可知,吸附初始阶段(0~120 min)Cr(Ⅵ)的吸附容量增加较快,去除率也较大,然后逐渐趋于平稳,180 min后基本达到吸附平衡。当吸附达到平衡后,溶液中Cr(Ⅵ)平衡质量浓度稳定在1.58 mg/L,吸附容量为4.842 mg/g,去除率达到94.84%。为进一步深入研究茶梗对Cr(Ⅵ)的吸附动力学过程,分别对实验数据进行了准一级动力学和准二级动力学拟合,拟合结果见图 6、图 7和表 2。
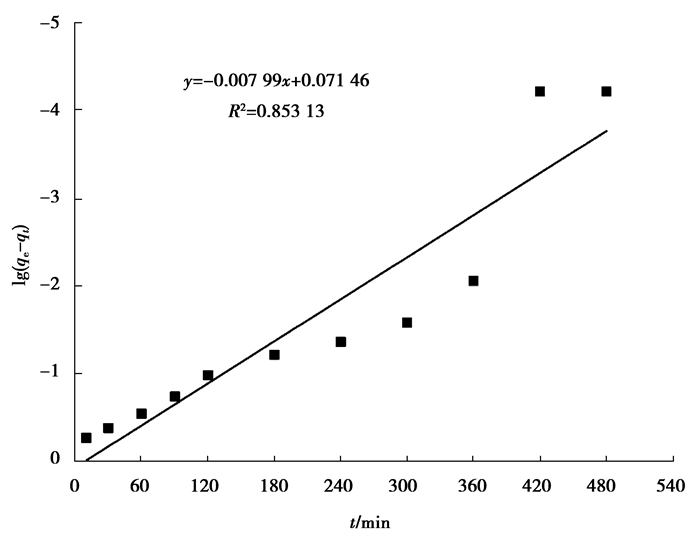
|
图 6 准一级动力学方程曲线 Figure 6 Pseudo-first-order model curve |
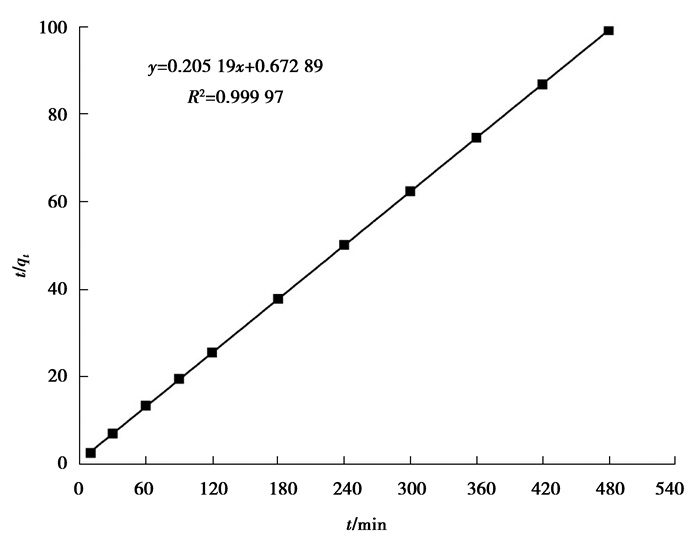
|
图 7 准二级动力学方程曲线 Figure 7 Pseudo-second-order model curve |
| 表 2 动力学模型拟合参数 Table 2 Fitting parameters of kinetic model |
从表 2可以看出,准二级动力学模型拟合效果更好,拟合系数高达0.999 97。且平衡吸附量计算值与实际测量值基本吻合。准二级动力学模型是建立在电子得失的化学吸附基础上的,说明茶梗对Cr(Ⅵ)化学吸附起主导作用[13]。
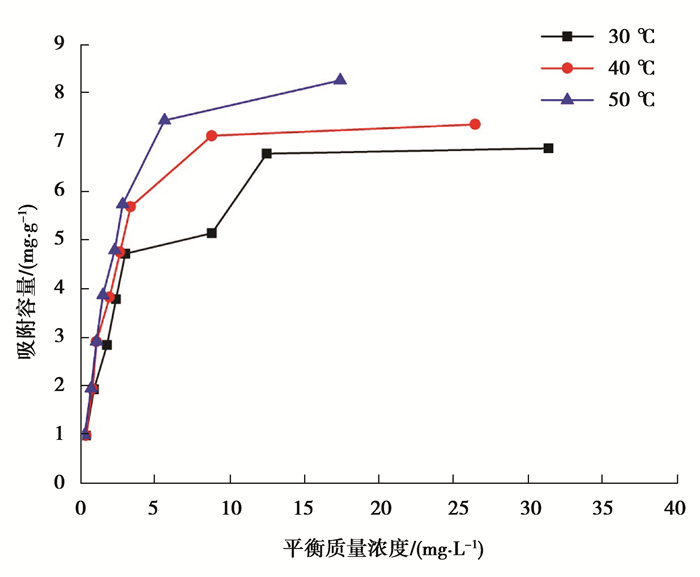
2.2.2 吸附等温线取50 mL初始质量浓度分别为10,20,30,40,50,60,80,100 mg/L的Cr(Ⅵ)溶液于250 mL的具塞玻璃锥形瓶中,用pH计测得此时pH≈5,分别投加0.5 g的吸附剂。然后将所有锥形瓶置于气浴恒温振荡器中,温度分别控制在20,30,40 ℃,转速定于150 r/min,振荡2 h后各取1 mL滤液测定Cr(Ⅵ)的剩余质量浓度并计算吸附容量,然后根据实验数据绘制平衡吸附容量与平衡质量浓度之间的关系曲线,结果如图 8所示。
|
图 8 多种温度下吸附容量与平衡质量浓度之间的关系 Figure 8 The relationship between equilibrium concentration and adsorption capacity at various temperatures |
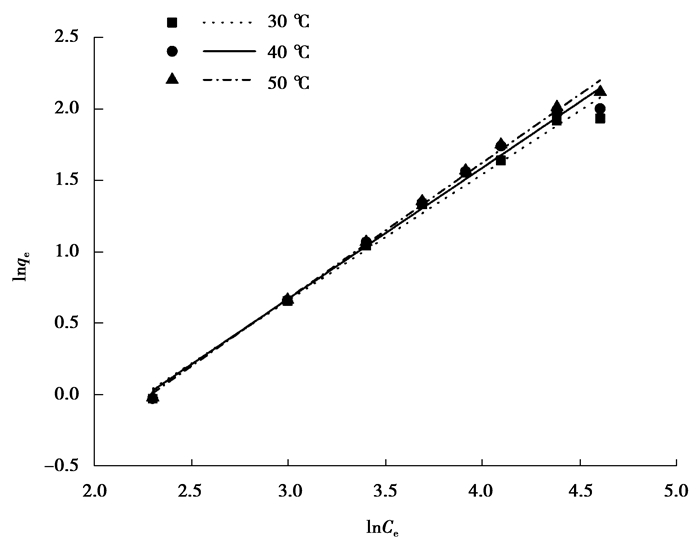
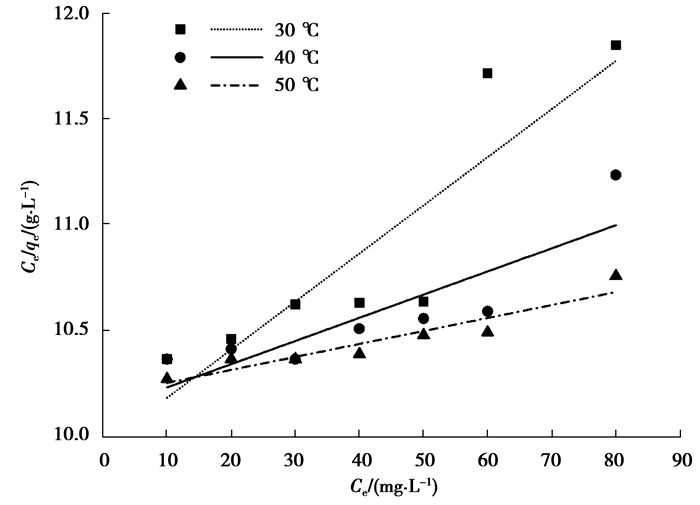
由图 8可知,茶梗对Cr(Ⅵ)的吸附容量随吸附温度的升高而增大。这说明升高反应温度可以促进反应的进行。在30 ℃的条件下,当初始质量浓度未达到80 mg/L时,茶梗的吸附容量保持稳步上升,当质量浓度超过80 mg/L后,吸附容量达到饱和无法进一步增大。为进一步深入研究茶梗对Cr(Ⅵ)的吸附动力学过程,分别对实验数据进行Langmiur和Freundlich等温吸附模型拟合,拟合结果见图 9、图 10和表 3。
|
图 9 多种温度下Freundlich模型的拟合直线 Figure 9 Fitted line of Freundlich model at various temperatures |
|
图 10 多种温度下Langmiur模型的拟合直线 Figure 10 Fitted line of Langmiur model at various temperatures |
| 表 3 等温线模型拟合参数 Table 3 Fitting parameters of Isotherm models |
由表 3可知,在3组不同实验温度下,Freundlich等温模型拟合效果都明显优于Langmiur等温模型,拟合系数R2最好可达0.996 40。此外,由Freundlich计算得到的n值大于1,说明茶梗对Cr(Ⅵ)的还原吸附比较容易进行。
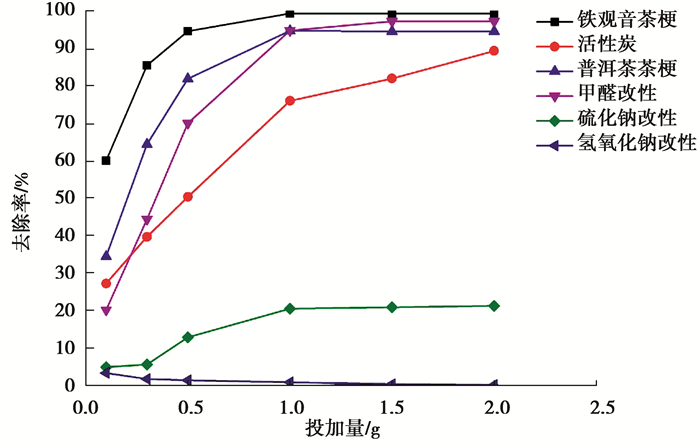
2.3 不同茶梗吸附剂对比试验结果取50 mL初始质量浓度为50 mg/L的Cr(Ⅵ)溶液于250 mL的具塞玻璃锥形瓶中,分别投加0.1,0.3,0.5,1.0,1.5,2.0 g不同吸附剂(铁观音茶梗,普洱茶茶梗、活性炭和3种改性茶梗),然后将所有锥形瓶置于气浴恒温振荡器中,温度控制在30 ℃,转速定于150 r/min,振荡2 h后各取1 mL滤液测定Cr(Ⅵ)的剩余质量浓度并计算去除率和吸附容量,结果如图 11所示。
|
图 11 投加不同吸附剂的对比实验 Figure 11 Contrast experiment with different adsorbents |
由图 11可知,当吸附剂投加量小于1 g时,去除率大致为:铁观音茶梗>普洱茶茶梗>甲醛改性茶梗>活性炭>硫化钠改性茶梗>氢氧化钠改性茶梗;当吸附剂投加量大于1 g且小于2 g时,去除率大致为:铁观音茶梗>甲醛改性茶梗>普洱茶茶梗>活性炭>硫化钠改性茶梗>氢氧化钠改性茶梗。可见茶梗对Cr(Ⅵ)的去除率在一定条件下优于活性炭,对去除水体重金属具有潜在探索价值,有待进一步深入研究。
2.4 表征结果 2.4.1 扫描电镜表征实验采用Mira3 LMH场发射扫描电镜对吸附前后的茶梗进行电镜扫描。将吸附前后茶梗粉末干燥后,用导电双面胶固定在样品台上,然后进行喷金处理30 s,用扫描电子显微镜观察样品形状和表面特征,结果见图 12。

|
图 12 茶梗吸附Cr(Ⅵ)前后的扫描电镜图 Figure 12 The morphology of the surface of tea stalk under scanning electron microscope before(a) and after(b) adosorption Cr(Ⅵ) |
由图 12观察可知,对比吸附反应前的茶梗,吸附反应后的茶梗表面发生了较大的变化。茶梗表面覆盖有一层可溶性物质,推测吸附反应后,这些可溶性物质大部分被溶解[13]。其中茶梗中的茶多酚等成分易溶解于水中,且茶多酚具有强还原性,能和重金属离子发生络合作用和静电作用[7]。由此推测,反应前后茶梗表面发生的变化是茶梗与Cr(Ⅵ)发生氧化还原反应后且吸附在茶梗表面造成的。
2.4.2 比表面积和孔径分布实验采用ASAP 2020M+C物理化学吸附分析仪对吸附前茶梗的比表面积和孔径分布进行了测定。通过N2的吸附等温线和脱附等温线计算得出BET表面积、Langmuir表面积、外表面积;通过t-plot法计算得出微孔体积和总孔体积;最后通过BJH吸脱附等温线计算得出平均孔径,结果见表 4。
| 表 4 茶梗的比表面积和孔径分布 Table 4 The ratio surface area and pore size distribution of tea stalks |
从表 4数据结果可知,茶梗的比表面积很小,BET比表面积只有0.240 9 m2/g,外表面积只有0.242 4 m2/g。从孔体积上来看,总孔体积为0.001 0 cm3/g,其中微孔体积只有0.000 2cm3/g,说明微孔所占的比重不大,主要是以中孔和大孔为主。茶梗平均孔径为16.434 5 nm,这也证实孔径主要为中孔和大孔。这些特点说明茶梗比较容易吸附直径较大的分子[14],同时也说明Cr(Ⅵ)有如此高的去除率,除了吸附作用外,氧化还原也起了很大的作用。
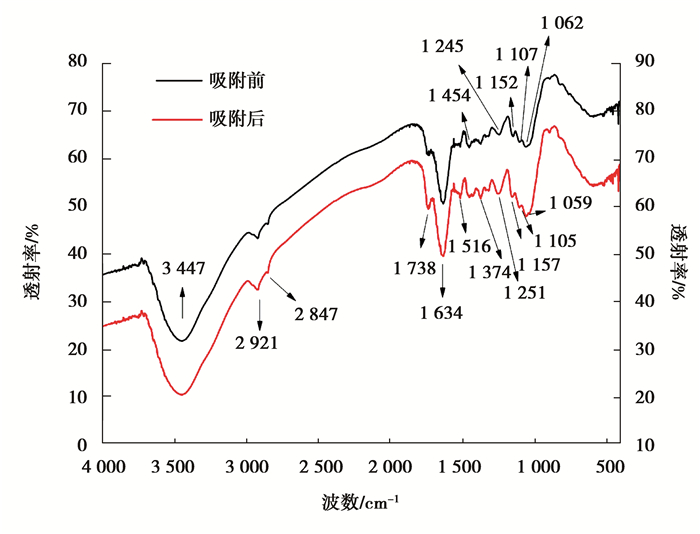
2.4.3 傅里叶红外光谱表征通过对比茶梗吸附Cr(Ⅵ)前后的FTIR光谱,可以有效的表征茶梗表面官能团的变化,为探索吸附机理提供依据。实验采用5DXC FTIR红外分光光度计进行检测。首先对茶梗粉末进行KBr压片处理,经恒温干燥箱烘干2 h的茶梗粉末与KBr按1:200的比例混合后,置于恒温干燥箱内烘干30 min,使水分全部去除,进行压片。然后在400~4 000 cm-1之间对其进行检测,实验结果见图 13。
|
图 13 茶梗吸附Cr(Ⅵ)前后的红外光谱图 Figure 13 FTIR spectra of tea stalk before and after adsorption Cr(Ⅵ) |
从图 13可以看出茶梗在不同波长处有大量的吸收峰,这表明茶梗的表面性质复杂,含有各种各样的官能团。吸附前茶梗主要含有以下一些官能团和化学键:1)含O-H(伸缩振动)的酚类化合物羟基(吸收峰出现在红外光谱图中3 447 cm-1附近);含O-H(伸缩振动)的醇类化合物羟基(吸收峰出现在红外光谱图中3 447 cm-1和1 454 cm-1附近);含-OH(伸缩振动)的羧酸类化合物羟基、含C-H(伸缩振动)的烷烃、烯烃(吸收峰出现在红外光谱图中2 921 cm-1、2 847 cm-1附近);2)含N-H(伸缩振动)的胺类化合物氨基和亚氨基(吸收峰出现在红外光谱图中3 447 cm-1和1 245 cm-1附近);3)含C-H(伸缩振动)的醛基(吸收峰出现在红外光谱图中2 847 cm-1附近);4)含C=O(伸缩振动)的的饱和脂肪醛、酯和羧酸类化合物羰基(吸收峰出现在红外光谱图中1 738 cm-1附近);5)含C=O(伸缩振动)的酰胺类化合物羰基(吸收峰出现在红外光谱图中1 634 cm-1附近);6)含-CH2(面外摇摆振动)的羧酸、C-F(伸缩振动)的卤代烃、含C-O(伸缩振动)的酯基、醚键、含C-N(伸缩振动)的酰胺、含C=H(面内弯曲振动)的烯炔烃类(吸收峰出现在红外光谱图中1 245 cm-1、1 251 cm-1附近);7)含C-O(伸缩振动)的醇、酸酐(吸收峰出现在红外光谱图中1 062 cm-1、1 107 cm-1、1 152 cm-1附近)[7, 13, 14, 23]。
对比吸附前的茶梗的红外光谱图,吸附后的茶梗的红外光谱图主要发生以下变化:1)在3 447,2 921,1 738 cm-1、1 634 cm-1处的吸收峰略微加强;2)在1 516 cm-1和1 374 cm-1处新出现较强的吸收峰;3)吸附前在1 245,1 152,1 107,1 062 cm-1处的吸收峰,吸附后分别移动到了1 251,1 157,1 105,1 059 cm-1处。因此,认为参与茶梗去除水中Cr(Ⅵ)的活性基团是含羟基、氨基和酰基的醇类、酰胺类等物质。
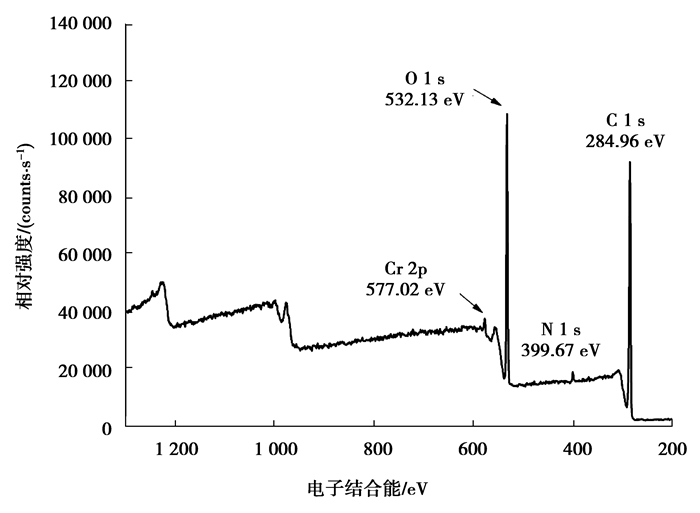
2.4.4 XPS表征X射线光电子能谱是一种非常重要的表面成分分析方法,不仅能够给出材料表面的化学组成及含量,而且可以分析出化学价态、化学键等信息[23]。通过XPS宽扫描全谱图的电子结合能可以定性鉴别化学元素的和进行半定量分析;从XPS高分辨扫描窄谱图可以得到电子轨道信息,进而鉴别元素的化学价态,对进行Cr(Ⅵ)吸附实验后的茶梗进行XPS表征,结果见图 14、图 15和表 5。
|
图 14 茶梗吸附Cr(Ⅵ)后的XPS全谱图 Figure 14 XPS spectra of tea stalk after adsotption Cr(Ⅵ) |
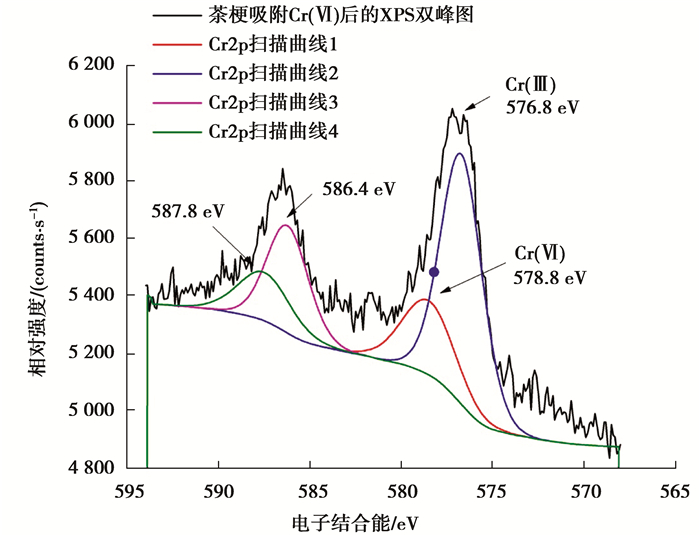
|
图 15 茶梗吸附Cr(Ⅵ)后的XPS双峰拟合图 Figure 15 XPS narrow spectra of tea stalk after adsotption Cr(Ⅵ) |
| 表 5 茶梗吸附Cr(Ⅵ)后的主要元素分布 Table 5 Distribution of the main elements of tea stalk after adsorption Cr(Ⅵ) |
XPS宽扫描全谱图能检测出样品中含有的全部或极大多数元素。由图 14可知,进行Cr(Ⅵ)吸附实验后的茶梗中含有C,N,O,Cr等元素(XPS无法测出H元素),且Cr的含量为0.63%。因为吸附前茶梗本身并不含有Cr元素,说明此时一定量的Cr离子被吸附到了茶梗表面。由图 14的双峰拟合图可知,Cr2p的两个波峰出现在576.8 eV和586.4 eV,说明吸附在茶梗上面的铬主要是Cr (Ⅲ),而578.8 eV和587.8 eV处的峰拟合效果并不理想,说明吸附反应后的茶梗表面几乎不存在Cr(Ⅵ)或存在极少量的Cr(Ⅵ)。可见茶梗对水中Cr(Ⅵ)的去除不是简单的吸附过程,氧化还原在此过程中起到了十分重要的作用[10, 23, 25]。
3 结论1) 通过一系列静态试验表明:茶梗投加量小于2 g时,茶梗水溶液虽然有少许浅颜色,但是对本实验的干扰基本可忽略不计。茶梗对Cr(Ⅵ)的去除率随茶梗粒径和茶梗投加量的增大而增大,取过80~100目筛子的茶梗0.5 g时,Cr(Ⅵ)去除率已经可达到90 %以上。pH会影响Cr(Ⅵ)在溶液中的存在形式,在酸性和中性条件下,茶梗和Cr(Ⅵ)更易发生还原吸附反应。共存离子Ca(Ⅱ)和Ni(Ⅱ)对Cr(Ⅵ)几乎不存在竞争吸附,茶梗对Cr(Ⅵ)的去除不仅是简单的吸附作用,还存在氧化还原反应。
2) Freundlich吸附等温方程能够较好的描述茶梗对Cr(Ⅵ)的去除过程,拟合系数最好可达0.996 40。茶梗对Cr(Ⅵ)的动力学拟合表明准二级动力学模型拟合效果更好,拟合系数高达0.999 97,表明茶梗对Cr(Ⅵ)的去除过程中化学吸附占主导作用。
3) 铁观音茶梗和普洱茶茶梗对Cr(Ⅵ)均有较高的去除率,一定条件下去除效果甚至优于活性炭,这为寻找成本低廉、吸附效果好的吸附剂提供一种新思路。甲醛改性的铁观音茶梗对Cr(Ⅵ)的还原吸附也有较好的效果,而Na2S和NaOH改性的铁观音茶梗对Cr(Ⅵ)去除效果较差。
4) SEM图表明吸附反应前后的茶梗表面发生较大的变化。BET表征显示茶梗比表面积、外表面积和孔体积均不大,并且微孔所占比例很小,大部分孔洞为中孔和大孔。FTIR图谱分析可知,含羟基、氨基和酰基的醇类、酰胺类等活性基团可能是参与茶梗还原吸附Cr(Ⅵ)的重要官能团。XPS表征证明有一定量的铬离子可以被吸附到茶梗表面,且吸附到茶梗表面的铬离子以Cr(Ⅲ)为主。
| [1] |
Malkoc E, Nuhoglu Y. Potential of tea factory waste for chromium (Ⅵ) removal from aqueous solutions:Thermodynamic and kinetic studies[J]. Separation & Purification Technology, 2007, 54(3): 291-298. |
| [2] |
Fahim N F, Barsoum B N, Eid A E, et al. Removal of chromium (Ⅲ) from tannery wastewater using activated carbon from sugar industrial waste[J]. Journal of Hazardous Materials, 2006, 136(2): 303-309. DOI:10.1016/j.jhazmat.2005.12.014 |
| [3] |
Mohan D, Singh K P, Singh V K. Trivalent chromium removal from wastewater using low cost activated carbon derived from agricultural waste material and activated carbon fabric cloth[J]. Journal of Hazardous Materials, 2006, 135(1/2/3): 280-295. |
| [4] |
万顺利, 徐圣友, 张庆瑞, 等. 废弃茶叶渣净化水体中重金属的研究进展[J]. 水处理技术, 2013, 39(8): 5-9. WAN Shunli, XU Shengyou, ZHANG Qingrui, et al. Removal of heavy metal from wastewater by tea waste:A review[J]. Technology of Water Treatment, 2013, 39(8): 5-9. (in Chinese) DOI:10.3969/j.issn.1000-3770.2013.08.002 |
| [5] |
张维麟, 李依蔓. 茶叶渣对废水中Cr6+和MnO4-的吸附效果研究[J]. 湖南农机, 2013, 40(3): 220-223. ZHANG Weilin, LI Yiman. The tea dregs of wastewater Cr6+ and MnO4- adsorption effect[J]. Hunan Agricultural Machinery, 2013, 40(3): 220-223. (in Chinese) |
| [6] |
冯秋月. 探讨茶梗开发应用的途径[J]. 福建茶叶, 2010, 32(12): 35-36. FENG Qiuyue. Discuss on the development and application of tea stems[J]. Tea in Fujian, 2010, 32(12): 35-36. (in Chinese) DOI:10.3969/j.issn.1005-2291.2010.12.009 |
| [7] |
周菁菁. 茶叶对废水中铅锌镉离子的吸附性能研究[D]. 长沙: 湖南大学, 2013. ZHOU Jingjing. Adsorption of lead, zinc, and cadmium ions from aqueous solution by teawaste adsorbents[D]. Changsha: Hunan University, 2013. (in Chinese) |
| [8] |
田芝娟, 苏剑生. 茶多酚与金属离子的相互作用及其生物学效应[J]. 中华临床医师杂志:电子版, 2008, 2(5): 599-602. TIAN Zhijuan, SU Jiansheng. Interactions between tea polyphenol and metal ions and its biological effects[J]. Chinese Journal of Clinicians:Electronic Version, 2008, 2(5): 599-602. (in Chinese) |
| [9] |
Bajpai S K, Jain A. Removal of copper (Ⅱ) from aqueous solution using spent tea leaves (STL) as a potential sorbent[J]. Water Sa, 2010, 36(3): 221-228. |
| [10] |
Park D, Lim S R, Yun Y S, et al. Reliable evidences that the removal mechanism of hexavalent chromium by natural biomaterials is adsorption-coupled reduction[J]. Chemosphere, 2007, 70(2): 298-305. DOI:10.1016/j.chemosphere.2007.06.007 |
| [11] |
Prabhakaran S K, Vijayaraghavan K, Balasubramanian R. Removal of Cr (Ⅵ) ions by spent tea and coffee dusts:Reduction to Cr (Ⅲ) and biosorption[J]. Industrial & Engineering Chemistry Research, 2009, 48(4): 2113-2117. |
| [12] |
Zuorro A, Lavecchia R. Adsorption of Pb (Ⅱ) on spent leaves of green and black tea[J]. American Journal of Applied Sciences, 2010, 7(2): 153-159. DOI:10.3844/ajassp.2010.153.159 |
| [13] |
敖晓奎. 速溶茶渣对废水中重金属离子的吸附行为和机理研究[D]. 长沙: 湖南农业大学, 2008. AO Xiaokui. Studies on the behavior and mechanism of adsorption of instant tea dregs on heavy metal ion in wastewater[D]. Changsha: Hunan Agricultural University, 2008. (in Chinese) |
| [14] |
张同钦. 废弃茶叶对重金属的吸附性能及重金属毒性评价研究[D]. 哈尔滨: 哈尔滨工业大学, 2011. ZHANG Tongqin. Research on adsorbability of waste tea for heavy metals and toxicity assessment for heavy metals[J]. Harbin: Harbin Institute of Technology, 2011. (in Chinese) |
| [15] |
Wasewar K L, Atif M, Prasad B, et al. Adsorption of zinc using tea factory waste:Kinetics, equilibrium and thermodynamics[J]. Clean:Soil, Air, Water, 2008, 36(3): 320-329. DOI:10.1002/(ISSN)1863-0650 |
| [16] |
Dizadji N, Anaraki N A. Adsorption of chromium and copper in aqueous solutions using tea residue[J]. International Journal of Environmental Science & Technology, 2011, 8(3): 631-638. |
| [17] |
Mahvi A H, Naghipour D, Vaezi F, et al. Teawaste as an adsorbent for heavy metal removal from industrial wastewaters[J]. American Journal of Applied Sciences, 2005, 2(1): 372-375. DOI:10.3844/ajassp.2005.372.375 |
| [18] |
崔晓宁. 预处理茶渣对废水重金属离子吸附特性和吸附机理研究[D]. 武汉: 华中农业大学, 2011. CUI Xiaoning. Studies on adsorption characteristics and mechanism of heavy metal ions from wastewater onto pretreated tea residue[J]. Wuhan: Huazhong Agricultural University, 2011. |
| [19] |
万顺利, 马钊钊, 薛瑶, 刘国斌, 何海, 吴芳芳, 谢华俊. 氧化锰改性的茶叶渣吸附水体中Pb (Ⅱ)[J]. 环境化学, 2014, 33(12): 2198-2205. WAN Shunli, MA Zhaozhao, XUE Yao, et al. Study on sorption characteristic of tea waste modified by hydrated manganese oxide toward Pb (Ⅱ) in water[J]. Environmental Chemistry, 2014, 33(12): 2198-2205. (in Chinese) DOI:10.7524/j.issn.0254-6108.2014.12.020 |
| [20] |
尤伟, 李华兰. 改性绿茶对Pb2+的吸附性能研究[J]. 四川师范大学学报:自然科学版, 2014, 37(2): 239-242. YOU Wei, LI Hualan. Study on adsorption ability of Pb2+ by modified green tea[J]. Journal of Sichuan Normal University:Natural Science, 2014, 37(2): 239-242. (in Chinese) |
| [21] |
Mondal M K. Removal of Pb (Ⅱ) ions from aqueous solution using activated tea waste:Adsorption on a fixed-bed column[J]. Journal of Environmental Management, 2009, 90(11): 3266-3271. DOI:10.1016/j.jenvman.2009.05.025 |
| [22] |
Yoshita A, Lu J L, Ye J H, et al. Sorption of lead from aqueous solutions by spent tea leaf[J]. African Journal of Biotechnology, 2009, 8(10): 2212-2217. |
| [23] |
郭昌建. 茶叶对重金属的吸附性能研究[D]. 大连: 大连理工大学, 2010. GUO Changjian. Reduction and adsorption of heavy metal ions from aqueous solution by green tea[D]. Dalian: Dalian University of Technology, 2010. (in Chinese) |
| [24] |
于明革, 陈英旭. 茶废弃物对溶液中重金属的生物吸附研究进展[J]. 应用生态学报, 2010, 21(2): 505-513. YU Mingge, CHEN Yingxu. Biosorption of heavy metals from solution by tea waste:A review[J]. Chinese Journal of Applied Ecology, 2010, 21(2): 505-513. (in Chinese) |
| [25] |
Park D, Park J M, Yun Y S. Mechanisms of the removal of hexavalent chromium by biomaterials or biomaterial-based activated carbons[J]. Journal of Hazardous Materials, 2006, 137(2): 1254-1257. DOI:10.1016/j.jhazmat.2006.04.007 |
| [26] |
Argun M E, Dursun S, Ozdemir C, et al. Heavy metal adsorption by modified oak sawdust:Thermodynamics and kinetics[J]. Journal of Hazardous Materials, 2007, 141(1): 77. DOI:10.1016/j.jhazmat.2006.06.095 |
 2018, Vol. 41
2018, Vol. 41


