为了实现镁热法生产海绵钛中的镁氯循环,很多海绵钛生产企业配套了镁电解技术。我国的镁电解技术基本涵盖了世界各种镁电解槽型技术,有无隔板电解槽、流水线电解槽、多极槽[1-3]。多极槽因其良好的经济指标占据了国内大部分市场[4-10]。流水线电解槽将多台无隔板电解槽和精炼槽以及镁-电解质分离槽通过电解质循环通道联合起来,实现集中加料和抽镁,极大地缩减了劳动强度,使其在镁电解工艺中具有竞争力和吸引力[11-12]。
流水线镁电解的杂质净化技术是该技术的特色技术,其设置了专门用于净化的精炼槽,可消化吸收低质量原料氯化镁。由于该技术属国内首次引进,鲜有镁电解过程中杂质Fe的净化可供参考的相关文献报道,某海绵钛生产企业流水线镁电解的工业生产中,杂质Fe净化效果极差,严重影响镁电解经济技术指标。而笔者利用气冷阴极研究了杂质Fe对镁相貌的影响,采用电化学工作站测试了杂质Fe的电化学行为,运用熔盐物性测定仪测定了适合杂质沉降的温度,根据电化学行为的研究结果和熔盐综合测定仪的测试结果提出了杂质Fe净化方法,将该净化方法应用于工业试验取得了良好的净化效果,镁电解经济技术指标得以提高,进一步凸显了流水线镁电解技术在海绵钛行业的技术优势。
1 杂质Fe净化原理在镁电解的电解质基本成分中,MgCl2的分解电压最低,因此,Na+、K+不放电,阴极涉及的反应见式(1),电极电势由能斯特方程确定[13],见式(2)。经计算,在温度为700 ℃及质量分数为16%时的电极电势为-2.802 V。
| $ {{\rm{M}}{{\rm{g}}^{2 + }} + 2{\rm{e}} \to {\rm{Mg, }}} $ | (1) |
| $ {{E_{{\rm{Mg}}/{\rm{M}}{{\rm{g}}^{2 + }}}} = E_{{\rm{Mg}}/{\rm{M}}{{\rm{g}}^{2 + }}}^\theta + \frac{{RT}}{{nF}}\ln \frac{{{\alpha _{{\rm{M}}{{\rm{g}}^{2 + }}}}}}{{{\alpha _{{\rm{Mg}}}}}}。} $ | (2) |
式中:EMg/Mg2+为绝对温度T及某一质量分数时的电极电势,V;EMg/Mg2+θ为标准电极电势,EMg/Mg2+θ=-2.59 V[14];R为常数,R=8.314 3 J/(K·mol);T为绝对温度,T=973 K;n为化合价,n=2;F为法拉第数,F=96 500 C;αMg2+为镁离子的活度,αMg2+=5×10-3[14];αMg为镁的活度,αMg=1。
杂质Fe在电解质中可以以FeCl2和FeCl3两种形态存在,FeCl3在高温下极易分解,在电解质中存在式(3)的平衡。FeCl2和FeCl3的比值与Cl2的分压有关,当Cl2的分压为1.01×105 Pa(阳极区)时,阳极区主要以FeCl3的形式存在,当Cl2的分压为0(阴极区)时,FeCl3几乎完全分解[14]。
| $ 2 \mathrm{FeCl}_{2}+\mathrm{Cl}_{2} \leftrightarrow 2 \mathrm{FeCl}_{3}。$ | (3) |
在流水线镁电解工艺中,杂质主要在精炼槽除去,为了提升精炼槽的除杂能力,在电解槽内安装了直流电极,杂质Fe在电解槽内可发生电化学反应,在阳极处,氯离子被氯气氧化,并发生氢氧化物和氧化物的氯化反应。在阴极处,杂质Fe的电位比Mg要正,首先被还原沉积在阴极上,反应过程见式(4),电极电势由能斯特方程确定,见式(5)。经计算,铁离子在温度为700 ℃及质量分数为0.03%时的电极电势为-1.99 V,阴极反应的产物沉淀在底部并进入淤泥。
| $ {{\rm{F}}{{\rm{e}}^{2 + }} + 2{{\rm{e}}^ - } \leftrightarrow {\rm{Fe, }}} $ | (4) |
| $ {{E_{{\rm{Fe}}/{\rm{F}}{{\rm{e}}^{2 + }}}} = E_{{\rm{Fe}}/{\rm{F}}{{\rm{e}}^{2 + }}}^\theta + \frac{{RT}}{{nF}}\ln \frac{{{\alpha _{{\rm{F}}{{\rm{e}}^{2 + }}}}}}{{{\alpha _{{\rm{Fe}}}}}}。} $ | (5) |
式中:EFe/Fe2+为绝对温度T及某一质量分数时的电极电势,V;EFe/Fe2+θ为标准电极电势,EFe/Fe2+θ=-1.163 V[14];R为常数,R=8.314 3 J/(K·mol);T为绝对温度,T=973 K;n为化合价,n=2;F为法拉第数,F=965 00 C;αFe2+为铁离子的活度,αFe2+=1.1×10-9[14];αFe为铁的活度,αFe=1。
在杂质离子降低的同时,在阴极产生细粒金属镁,金属镁可同FeCl2发生化学反应,反应式见式(6),在镁滴表面释放的杂质将变重并沉淀至淤泥[14]。
| $ \mathrm{FeCl}_{2}+\mathrm{Mg} \rightarrow \mathrm{Fe}+\mathrm{MgCl}_{2}。$ | (6) |
试验所用的电解质均来自某海绵钛厂流水线镁电解槽,成分见表 1。
| 表 1 电解质成分 Table 1 Electrolyte components |
试验利用电化学工作站研究杂质Fe的电化学行为,型号:CHI860D;厂家:北京华科普天科技有限责任公司。
试验利用装有气冷阴极[15]的电解装置研究镁的析出形貌,装置示意图见图 1。
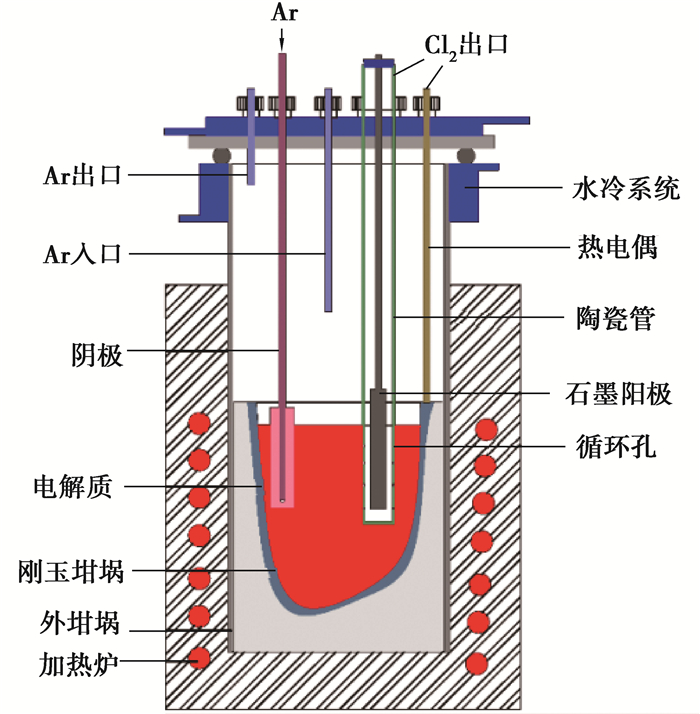
|
图 1 装有气冷阴极的电解装置示意图 Fig. 1 Diagram of electrolytic device with a gas-cooled cathode |
试验利用电子天平称重,称量范围:0~6 000 g;称量精度:0.001 g。
试验利用熔盐综合物性测试仪测试熔盐的密度,测试温度:RT~1 400 ℃;温控精度:0~10 ℃/min,±1 ℃;重锤材料:铂金;测试精度:<±1%。
试验利用高温熔盐黏度测试仪测试熔盐的黏度,测试温度:RT~1 000 ℃;温控精度:0~50 ℃/min,±1 ℃;测试范围:1.6×10-3~500 Pa·s;测试精度:2.5%;测试气氛:惰性气氛。
试验利用自制电解装置进行熔盐的净化试验,装置示意图见图 2。
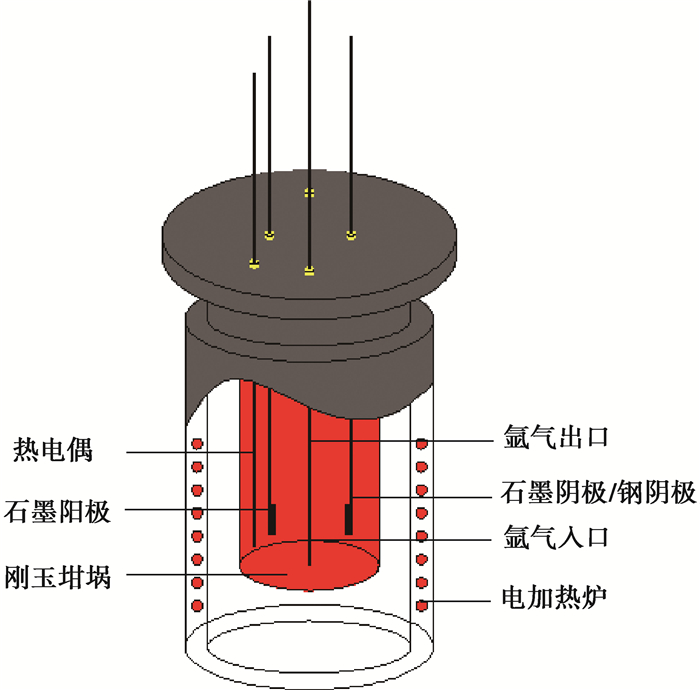
|
图 2 电解装置示意图 Fig. 2 Diagram of electrolytic device |
试验前,将所用的电解质在150 ℃的条件下烘干12 h。按试验要求分别称取各组元,研磨混匀后放入刚玉坩埚,在加热炉中在300 ℃下脱水4 h后升温至700 ℃,恒温1 h使样品充分熔化后开始试验,升温速率为10 ℃/min。采用电化学工作站研究铁离子在阴极沉积的电化学行为。采用气冷阴极研究不同杂质Fe含量对阴极镁滴形貌特征的影响。采用高温熔盐综合物性测定仪测试电解质的密度,采用高温熔盐黏度测试仪测试熔盐的黏度。采用自制电解装置进行Fe的净化研究。
试验过程中的净化率按式(7)计算。
| $ \omega = \frac{{{C_{\rm{前}}} - {C_{\rm{后}}}}}{{{C_{\rm{前}}}}} \times 100\% , $ | (7) |
式中:ω为净化率,%;C前为净化试验前的质量浓度,%;C后为净化试验后的质量浓度,%。
3 结果与讨论 3.1 杂质Fe对镁电解过程的影响在700 ℃分别以ϕ1 mm的石墨棒为工作电极(WE),ϕ2 mm的石墨棒为对电极(CE),Ag/AgCl(其中NaCl-KCl-4.5%AgCl,NaCl与KCl等摩尔比)为参比电极(RE),测试42%NaCl-42%KCl-16%MgCl2体系(其中Tfe质量分数为0.03%)循环伏安曲线结果见图 3。由图 3可见,在扫描范围内出现了两对峰,分别为1.05 V时2Cl-
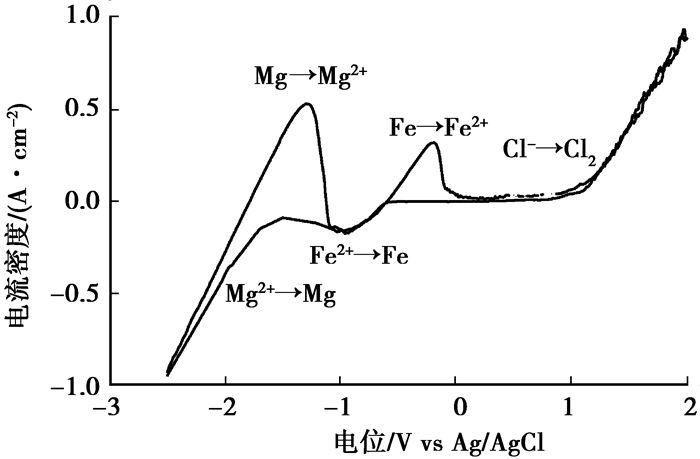
|
图 3 含Fe电解质体系的循环伏安曲线 Fig. 3 The CV of iron-containing electrolyte |
同时,在钢阴极表面生成的海绵铁也会对镁的析出产生影响。在700 ℃的40%NaCl-40%KCl-15%MgCl2-5%CaCl2电解质体系中,添加质量分数为1%的FeCl2在电流密度0.3 A/cm2下电解0.5 h,观察阴极镁滴的形貌特征,结果见图 4。由图 4可见,在未添加FeCl2的电解质体系获得镁滴颗粒大,且相对均匀;体系中添加FeCl2后,镁滴颗粒不规则,形貌特征较差,不利于镁的汇集长大,易造成镁损失。另外,含FeCl2的电解质对钢阴极的润湿性好,也会造成镁的汇集不好。电解质中的FeCl2和镁可直接发生式(3)的反应,同样会造成镁损失。

|
图 4 铁对镁形貌的影响 Fig. 4 The impact of Fe on the morphology of magnesium |
电极反应过程通常包含一系列影响溶液中溶解的氧化物O转化为还原态形式R的步骤,具体电极反应途径见图 5。由图 5可知,电极反应速率由如下过程的速率决定:1)物质传递;2)电极表面上的电子转移;3)电子转移步骤的前置或后续的化学反应;4)其他的表面反应。
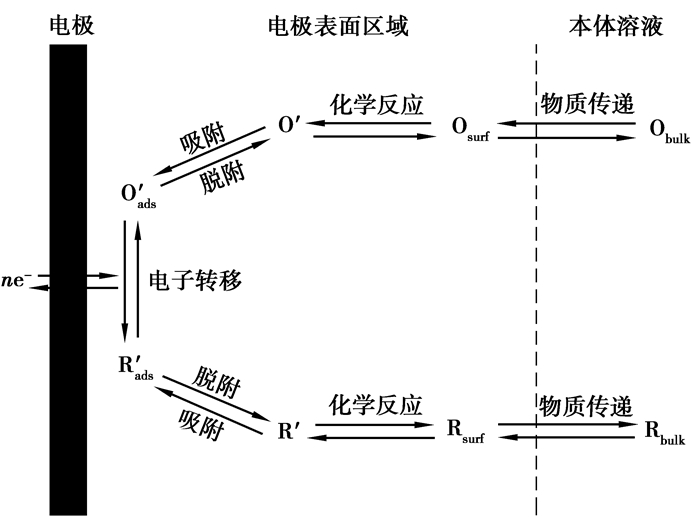
|
图 5 一般电极反应的途径 Fig. 5 The way of general electrode reaction |
在上述反应过程中,物质的传递主要受物质的电势梯度、浓度梯度或密度梯度的影响,电极表面上的电极转移主要受电势和电流密度的影响,电子转移步骤的前置或后续的化学反应和其他的表面反应主要受电极本身和本体溶液的影响[13]。在流水线镁电解过程中,杂质Fe在电极上的反应过程包含Fe离子向电极的物质传递、电极表面上的电子转移、电子转移步骤的后续的化学反应和产物Fe向熔盐本体的物质传递,主要受熔盐的浓度梯度、电势、电流密度和电极材质的影响。故研究了杂质Fe在不同电流密度、不同槽电压和不同电极材质下的净化率。
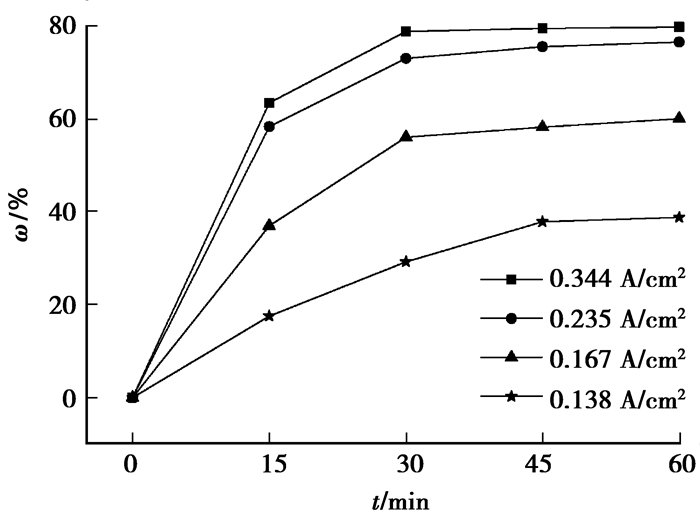
杂质Fe在不同电流密度下的净化率见图 6。电极材质为石墨,槽电压为3.5 V,电解质温度为725 ℃,无电解质扰动。由图 6可知,随着电流密度的增大,净化率增强,当电流密度增大到一定程度时,随着电流密度的增大,净化率几乎不变。电流密度对净化率的影响为电流密度的大小直接决定电极的反应速率,电极的反应速率随着电流密度的增大而增强,当增加到一定程度时,电极上的反应受物质传递速率的限制,无法进一步提高。
|
图 6 杂质Fe在不同电流密度下的净化率 Fig. 6 Purification rate of impurity Fe at different current densities |
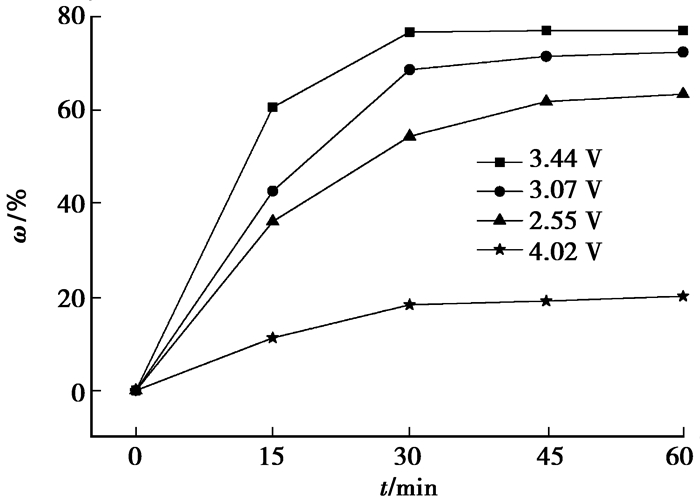
杂质Fe在不同槽电压下的净化率见图 7。电极材质为石墨,电流密度为0.35 A/cm2(选取较优电流密度,下同),电解质温度为725 ℃,无电解质扰动。由图 7可知,随着槽电压的升高,杂质Fe的净化率增强。当槽电压增加到一定程度时,净化率急剧下降。电解槽电压对除杂能力的影响为流水线镁电解在三元系MgCl2-KCl-NaCl中进行,在较低的电压(低于MgCl2的分解电压)下,电解质中的FeCl2在电极上分解,而MgCl2则不进行分解或分解很少,净化率随着电流密度的增大而增强。当槽电压高于MgCl2的分解电压时,MgCl2在电极上分解,而FeCl2分解很少,此时杂质Fe的净化主要靠阴极生成的细镁粒和FeCl2发生式(3)的化学反应。
|
图 7 杂质Fe在不同槽电压下的净化率 Fig. 7 Purification rate of impurity Fe at different cell voltages |
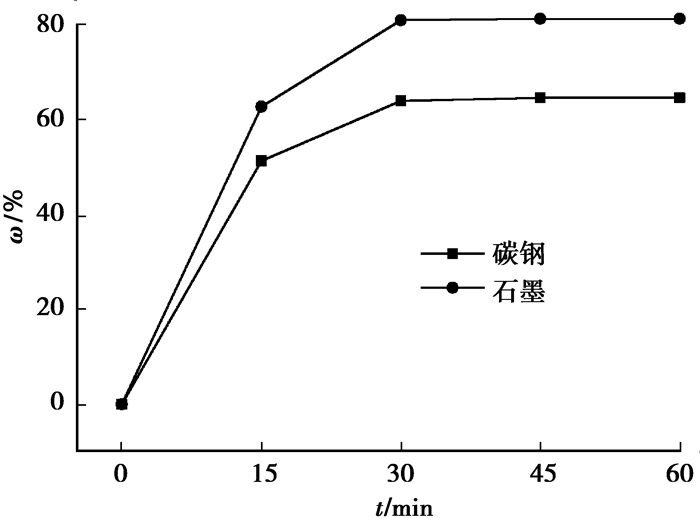
杂质Fe在不同电极材质下的净化率见图 8。槽电压为3.5 V,电流密度为0.35 A/cm2,电解质温度为725 ℃,无电解质扰动。由图 8可知,电极采用石墨电极的净化率优于采用碳钢。电极材质对除杂能力的影响为由于液镁在碳钢电极上的润湿性优于石墨电极,石墨电极上产生的镁粒较细,在石墨电极上不光可以发生杂质的电化学反应,还有大量细粒镁与杂质Fe发生式(3)的化学反应。
|
图 8 杂质Fe在不同材质下的净化率 Fig. 8 Purification rate of impurity Fe in different materials |
由图 6~8可知,随着反应时间的增加,净化率增强,当时间超过30 min后,净化率基本不随时间变化。反应时间对净化率的影响为随着电解的不断进行电解质中的杂质的浓度逐渐降低,当降低到一定程度时,受到物质传递速率的影响,杂质在电极上的反应发生极为缓慢。
3.2.2 杂质Fe在电解质中的沉降颗粒在静止流体的自由沉降过程中受到重力、浮力和曳力3个作用力的影响[16],根据牛顿第二定律可得式(8)。
| $ {F_{\rm{g}}} - {F_{\rm{b}}} - {F_{\rm{d}}} = m\frac{{{d_{\rm{u}}}}}{{{d_{\rm{t}}}}}, $ | (8) |
式中:Fg为重力,
颗粒沉降速度起先不断增加,逐渐趋向于一个渐近值,这个值即为颗粒的沉降速度。对于球形小颗粒,沉降的加速阶段很短,加速度段经历的距离也很小,可近似认为颗粒始终以沉降速度下降,且该沉降过程处于斯托克斯定律区,由式(8)可推导出小颗粒的沉降速度见式(9)。
| $ u_{\mathrm{t}}=\frac{g d_{\mathrm{p}}^{2}\left(\rho_{\mathrm{p}}-\rho\right)}{18 \mu}, $ | (9) |
式中:ut为沉降速度,m/s;g为重力加速度,m/s2;dp为颗粒直径,m;ρp为颗粒密度,kg/m3;ρ为流体密度,kg/m3;μ为流体黏度,Pa·s。
由式(9)可知,颗粒的沉降速度与流体的密度、流体的黏度、颗粒直径和颗粒的密度相关。在流水线镁电解过程中,所考虑的杂质以及流体的成分基本都是定值,流体的密度和黏度受温度的影响较大,颗粒的沉降速度与电解质的温度有关。故研究了杂质Fe在不同温度下的净化率。
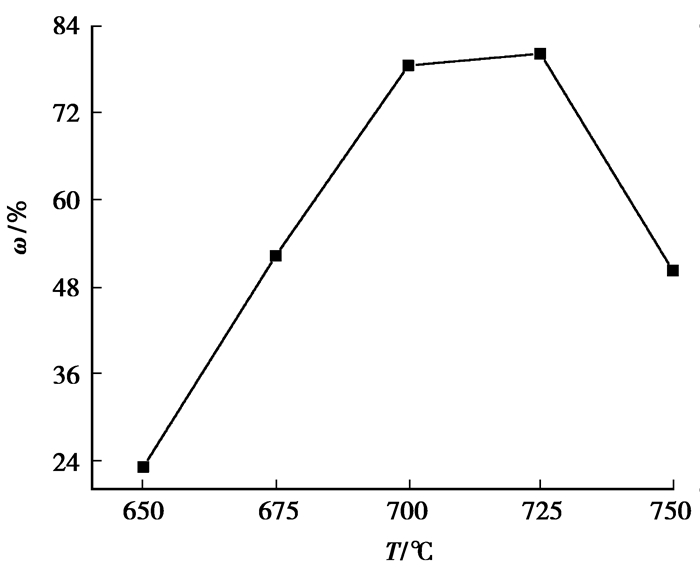
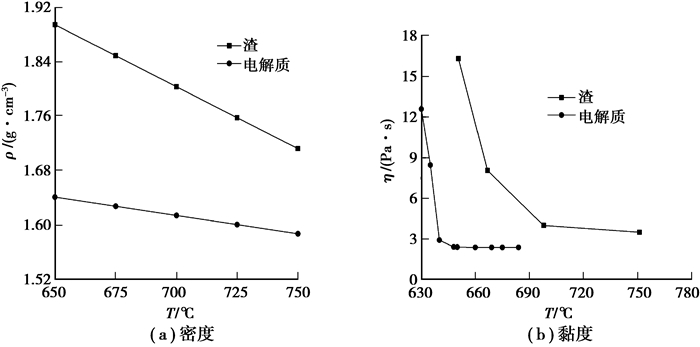
杂质Fe在不同温度下的净化率见图 9。电极材质为石墨,槽电压为3.5 V,电流密度为0.35 A/cm2,无电解质扰动。由图 9可知,随着温度的升高,净化率先增强后减弱,在温度为725 ℃时,净化率出现最佳值。温度对净化率的影响为温度影响电解质和渣的密度和黏度。不同温度下电解质和渣的密度和黏度见图 10。由图 10可知,随着温度的升高,电解质和渣的密度均降低,但渣的密度降低的速度高于电解质,不利于渣和电解质的分离。随着温度的升高,电解质和渣的粘度均降低,尤其是渣的黏度降幅很大,利于渣和电解质的分离。
|
图 9 杂质Fe在不同温度下的净化率 Fig. 9 Purification rate of impurity Fe at different temperatures |
|
图 10 不同温度下渣和电解质密度和黏度 Fig. 10 Density and viscosity of slag and electrolyte at different temperatures |
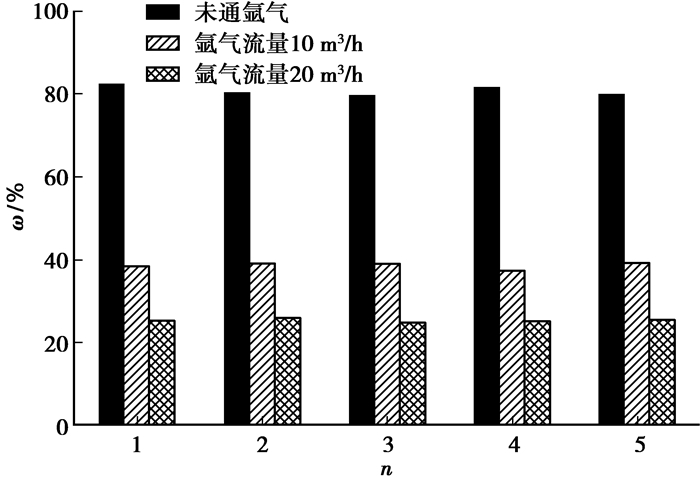
在流水线镁电解过程中,精炼槽还受到除渣、加料等操作对电解质产生扰动,故研究了杂质Fe在不同电解质扰动强度下的净化率。杂质Fe在不同电解质扰动强度下的净化率见图 11,用氩气来模拟电解槽的除杂和加料等操作对电解质的扰动,通过控制不同流量的氩气来改变电解质扰动,电极材质为石墨,槽电压为3.5 V,电流密度为0.35 A/cm2,电解质温度为725 ℃。由图 11可知,随着扰动强度的加剧,净化率急剧减弱。电解质的循环量对净化率的影响表现为电解质的扰动过大时,将槽内原有的平稳的层流变为紊流,导致电解质中的Fe杂质沉降困难。
|
图 11 杂质Fe不同扰动方式下的净化率 Fig. 11 Purification rate of impurity Fe under different disturbance modes |
采取上述措施,在实验室开展了验证试验,试验净化和工业净化的效果的对比见表 2,试验净化电极材质为石墨,槽电压为3.5 V,电流密度为0.35 A/cm2,电解质净化时间30 min,电解质温度725 ℃,无电解质扰动。由表 2可知,工业净化前后电解质中的Fe几乎无变化,含量远高于工业需求;试验净化后电解质中的Fe得到明显降低,完全满足工业要求。
| 表 2 电解质中Fe经工业净化和试验净化的效果对比 Table 2 Comparison of the effects of industrial and experimental purification of Fe in electrolyte |
基于以上杂质Fe净化率的主要因素的实验室研究,在工业生产中,通过在槽内安装石墨直流电极,控制石墨电极电压在6~8 V,提高头槽液位至1 780 mm来提高电流密度,保证原料在槽内净化时间不少于30 min可提高杂质Fe在电极上的反应能力;通过控制精炼槽的温度为725 ℃±5 ℃,减少操作对电解质的扰动,如控制适当的原料加入速度和电解质循环量,除渣方式以人工除渣和气动抓斗为主,电解质中的杂质Fe由0.028 9%降至0.009 1%,净化效果明显提升。
4 结论1) 杂质Fe对流水线镁电解过程的影响主要为:Fe离子优先于Mg离子析出造成用于镁离子还原的电流减少;在钢阴极表面生成的海绵铁使阴极钝化;含FeCl2的电解质对阴极的湿润性较好使阴极析出的镁呈鱼子状造成镁损失;Fe离子和析出的镁直接反应造成镁损失。
2) 影响杂质Fe净化的主要因素为电流密度、电解槽电压、电极材质、反应时间、电解质温度和电解质扰动。杂质Fe的净化率随着槽电压的升高(低于MgCl2分解电压)、电流密度的增加、反应时间的延长而增加;杂质在石墨电极的净化率优于碳钢电极;在电解质温度为725 ℃时,杂质Fe的净化率最佳。
3) 在工业生产中,通过在槽内安装石墨直流电极,控制石墨电极电压在6~8 V,提高头槽液位至1 780 mm来提高电流密度,保证原料在槽内净化时间不少于30 min可提高杂质Fe在电极上的反应能力;通过控制精炼槽的温度为725 ℃±5 ℃,减少操作对电解质的扰动,可提高杂质Fe在电解槽的沉降。开展工业试验后电解质中的杂质Fe由0.028 9%降至0.009 1%,净化率明显提升。
| [1] |
阎守义. 试谈我国海绵钛生产工艺的优化途径[J]. 轻金属, 2016(6): 35-39. YAN Shouyi. Discussion on optimization approach of titanium sponge production process in China[J]. Light Metals, 2016(6): 35-39. (in Chinese) |
| [2] |
李开华. 镁热法生产海绵钛技术发展现状[J]. 材料导报, 2011(2): 225-228, 244. LI Kaihua. Discussion on technical development status for sponge titanium production by magnesium reduction process[J]. Materials Review, 2011(2): 225-228, 244. (in Chinese) |
| [3] |
姜宝伟, 蔡增新, 翁启钢. 海绵钛生产工艺中几种镁电解槽技术的对比分析[J]. 轻金属, 2014(9): 65-67. JIANG Baowei, CAI Zengxin, WENG Qigang. Comparative analysis of several magnesium reduction cell technologies in titanium sponge production[J]. Light Metals, 2014(9): 65-67. (in Chinese) |
| [4] |
Okabe T H. Mass of electricity and technology: titanium metal and its production process[J]. The Journal of the Institute of Electrical Engineers of Japan, 2006, 126(12): 801-805. DOI:10.1541/ieejjournal.126.801 |
| [5] |
Sun Z, Liu C L, Lu G M, et al. Effects of operational and structural parameters on cell voltage of industrial magnesium electrolysis cells[J]. Frontiers of Chemical Science and Engineering, 2015, 9(4): 522-531. DOI:10.1007/s11705-015-1539-x |
| [6] |
Liu C L, Sun Z, Lu G M, et al. 3D and 2D experimental views on the flow field of gas-evolving electrode cold model for electrolysis magnesium[J]. Flow Measurement and Instrumentation, 2015, 45: 415-420. DOI:10.1016/j.flowmeasinst.2015.07.011 |
| [7] |
Duhaime P, Mercille P, Pineau M. Electrolytic process technologies for the production of primary magnesium[J]. Mineral Processing and Extractive Metallurgy, 2002, 111(2): 53-55. |
| [8] |
Chen Z Y, Wang L J, Chou K C, et al. Comparison of different calculation methods of the new generation geometric model in predicting the density of NaCl-MgCl2-CaCl2 systems[J]. Journal of Solution Chemistry, 2014, 43(3): 577-584. DOI:10.1007/s10953-014-0147-6 |
| [9] |
Choi M S, Lee C K, Lee G G, et al. Technology of molten salt electrolysis of magnesium chloride[J]. Materials Science Forum, 2010, 654/655/656: 799-802. |
| [10] |
姜宝伟, 朱卫平, 郭晓光. 镁电解多极槽技术与生产实践[J]. 轻金属, 2015(11): 50-54. JIANG Baowei, ZHU Weiping, GUO Xiaoguang. Production practice and analysis of multipolar magnesium cell technology[J]. Light Metals, 2015(11): 50-54. (in Chinese) |
| [11] |
朱福兴, 马尚润, 郑权, 等. 提高流水线镁电解电流效率的研究[J]. 有色金属(冶炼部分), 2015(2): 12-16. ZHU Fuxing, MA Shangrun, ZHENG Quan, et al. Study of improving current efficiency of pipeline magnesium electrolysis[J]. Nonferrous Metals(Extractive Metallurgy), 2015(2): 12-16. (in Chinese) DOI:10.3969/j.issn.1007-7545.2015.02.004 |
| [12] |
马尚润, 朱福兴, 穆天柱, 等. 影响流水线镁电解槽电流效率的主要因素[J]. 轻金属, 2016(11): 47-51. MA Shangrun, ZHU Fuxing, MU Tianzhu, et al. The main factors of influence of magnesium reduction cells of the production line on current efficiency[J]. Light Metals, 2016(11): 47-51. (in Chinese) |
| [13] |
巴德, 福克纳.电化学方法: 原理和应用[M].邵元华, 朱果逸, 董献堆, 等, 译.北京: 化学工业出版社, 2005: 1-31. Bard A J, Faulkner L R. Electrochemical method: principle and application[M]. SHAO Yuanhua, ZHU Guoyi, DONG Xiandui, et al, trans. Beijing: Chemical Industry Press, 2005: 1-31. (in Chinese) |
| [14] |
张永健. 镁电解生产工艺学[M]. 长沙: 中南大学出版社, 2006: 326-346. ZHANG Yongjian. Electrolytic metallurgy of magnesium[M]. Changsha: Central South University Press, 2006: 326-346. (in Chinese) |
| [15] |
马尚润, 郑权, 朱福兴, 等.气冷阴极、熔盐电解装置及电解方法: 201510081679.6[P]. 2017-03-22. MA Shangrun, ZHENG Quan, ZHU Fuxing, et al. Air cooled cathode, molten salt electrolysis device and electrolysis method: 201510081679.6[P]. 2017-03-22. (in Chinese) |
| [16] |
陈敏恒, 丛德滋, 方图南, 等. 化工原理[M]. 4版. 北京: 化学工业出版社, 2015. CHEN Minheng, CONG Dezi, FANG Tunan, et al. Principle of chemical industry[M]. 4th ed. Beijing: Chemical Industry Press, 2015. (in Chinese) |
 2019, Vol. 42
2019, Vol. 42


