零价铁作为绿色且经济的水环境处理技术之一,对水环境中有机氯化物[1-2]、重金属(铬、铅、砷)[3-5]、有机染料及农药[6-7]等处理效果良好而备受青睐。纳米零价铁(NZVI)具有比零价铁更高的比表面积和还原活性,是近年来国内外研究热点。但常规的气相制备法、液相制备法所制备的NZVI粒径小、磁性强,在环境中不稳定、易团聚和钝化,使其反应活性和迁移率降低[8-9],对污染物的去除存在一定的局限性。因此,近年来研究者将NZVI负载到活性炭上,以解决颗粒团聚问题[10-11];通过金属修饰以解决颗粒稳定性问题[12],采用电化学沉积法解决NZVI颗粒均匀负载的问题[13]。常用载体主要包括活性炭(AC)、膨润土、树脂、沸石[8, 14-16],常用的修饰金属有镍(Ni)、铅(Pd)和铜(Cu)[17-18]。
AC具有发达的孔隙结构,比表面积大、吸附性强,无毒、价廉且环境友好,对重金属和有机物具有较强的吸附能力,是作为载体的优良选择[16],可增强NZVI的分散性,有效降低零价铁的团聚[5, 15]。镍(Ni)是一种成本低且耐腐蚀性良好的磁性材料,广泛用于废水处理,可与Fe构成原电池,改变的零价铁的电子特性[12, 19],减缓零价铁的钝化,是修饰金属的不二选择[20-21]。研究证明,Ni作修饰金属,可提高零价铁的稳定性,且对持久性污染物降解也更加高效[22-24]。但目前鲜有将金属修饰和固相负载两种改良方法相结合,通过电沉积法制备NZVI的研究报道。
笔者选取合适药剂,自制电沉积液,以活性炭(AC)为固体负载,以Ni为修饰金属,通过两种改良方法的结合,取长补短,改善NZVI易团聚、易钝化的缺点;并通过电沉积法实现NZVI颗粒的制备,具有高效、易操作的特点。以Cr(Ⅵ)去除率为指标,通过试验优化制备NZVI的沉积液配比和电沉积条件,并进行Ni/Fe双金属颗粒性能试验研究,有利于完善制备方法,为后续NZVI的制备和应用研究提供基础。
1 实验材料与方法 1.1 主要仪器与材料主要仪器包括恒温水浴锅(HH-4,KA3005D),直流电源(JEOLJSM-7800F),场发射扫描电子显微镜(FESEM,JEOL JSM-7800F,牛津仪器科技有限公司),X射线衍射仪(XRD,D8 Quest,美国布鲁克·道尔顿公司),比表面积与孔隙度分析仪(BET QuadraSorb SI,美国康塔仪器有限公司)。
主要材料包括粉末活性炭(200目),石墨,聚四氟乙烯,泡沫镍,纯铁片,七水合硫酸亚铁(FeSO4·7H2O),六水合硫酸镍(NiSO4·6H2O),一水合硫酸锰(MnSO4·H2O)等。所用试剂均为分析纯。
1.2 活性炭负载型Ni/Fe双金属颗粒的制备 1.2.1 电极片的制备电沉积装置两端的电极片分别为纯铁片和活性炭电极片,纯铁片仅需弱酸浸泡,去除表面钝化层洗净,烘干即可。而活性炭为非导电性物质,需进行导电性处理,具体如下。
将200目的活性炭粉末、作黏结剂的聚四氟乙烯乳液(PTFE,质量分数40%)和作导电剂的石墨按8:1:1的质量比混合均匀,再加适量乙醇搅伴均匀,置于球磨机上反复碾压,获得0.35~0.45 mm厚的活性炭片。再按活性炭层、泡沫镍导电层、活性炭层的顺序经双辊轧机碾压后,获得0.9~1.1 mm厚的导电活性炭电极片,剪成30 mm×20 mm矩形片,沸水域清洗后烘干以备用。
1.2.2 沉积液的配制为了使镍、铁离子通过电沉积负载到活性炭电极片上,本试验采用一定质量浓度的硫酸镍、硫酸亚铁配制沉积液,同时以硼酸作缓冲试剂,硫酸锰作添加剂,每次准确称取等量的试剂,用超纯水溶解,100 mL容量瓶定容,配制沉积液。沉积液均为现配现用。
1.2.3 Ni/Fe-AC BPs的制备电沉积装置如图 1所示,阴、阳级电极片分别为活性炭和纯铁片,间隔30 mm对称放置,固定在直径为8 cm的带盖玻璃器皿上。按1.2.2节所述配制的100 mL电沉积液倒入电沉积装置,通过紫铜电极夹连接直流电源,构成电沉积装置。

|
①紫铜电极夹;②纯铁片20 mm× 30 mm×1 mm;③活性炭电极片20 mm×30 mm×1 mm;④沉积液;⑤直流电源 图 1 试验电沉积装置示意图 Fig. 1 Schematic diagram of experimental electrodeposition device |
将电沉积装置置于恒温水浴锅中,以控制电沉积温度。通过控制直流电流大小和电沉积时间,制得不同条件下的Ni/Fe-AC BPs。
1.2.4 Ni/Fe-AC BPs制备的优化零价铁对Cr(Ⅵ)具有良好的催化还原性,Cr(Ⅵ)去除率可作为Ni/Fe-AC BPs性能评价指标,优化其制备条件。将制备好的Ni/Fe-AC BPs用超纯水冲洗30 s后迅速加入盛有100 mL质量浓度为40 mg/L六价铬溶液的锥形瓶中,在室温条件下进行催化还原试验。采用二苯碳酰二肼分光光度法测试催化还原后Cr(Ⅵ)的浓度,计算Cr(Ⅵ)去除率。
1.2.5 Ni/Fe-AC BPs性能试验研究为了探究AC、Fe-AC和Ni/Fe-AC BPs对六价铬去除效果的异同,证明所采用的改良制备法的优势,进行了相同反应条件下AC、Fe-AC和Ni/Fe-AC BPs对六价铬去除效果的对比试验研究。
1.3 表征方法最优条件下制备的Ni/Fe-AC BPs进行了以下表征:在高真空度(6×10-4 Pa)条件下,采用14.80 kV加速电压通过扫描电子显微镜(FESEM)进行表面形貌分析,同时开启EDS测Ni/Fe-AC BPs的元素种类,进行元素含量的半定量分析;以Cu靶为X射线源,在40 kV电压、100 mA电流条件下对Ni/Fe-AC BPs进行X射线衍射晶型分析;以氮气吸附BET测比表面积和孔隙度。
2 结果与讨论 2.1 Ni/Fe-AC BPs制备的优化相关文献[25-26]表明,Ni/Fe-AC BPs制备的主要影响因素为沉积液配比和电沉积条件,其中电沉积条件以电沉积时间、电流密度、反应温度为主,预试验结果与其一致。本试验以Ni/Fe-AC BPs对Cr(Ⅵ)的去除率为评价指标,对Ni/Fe-AC BPs制备条件行进行优化。
2.1.1 沉积液配比的确定16组沉积液组合预试验表明,沉积液对制备Ni/Fe-AC BPs的影响主要为其组分配比:FeSO4·7H2O质量浓度(因素A)、NiSO4·6H2O与FeSO4·7H2O质量比(因素B)、硼酸质量浓度(因素C)、MnSO4·H2O质量浓度(因素D)。因此,试验以A、B、C、D为沉积液配比影响因素设计正交试验,并以Cr(Ⅵ)去除率为指标,对制备双金属颗粒的沉积液进行优化。
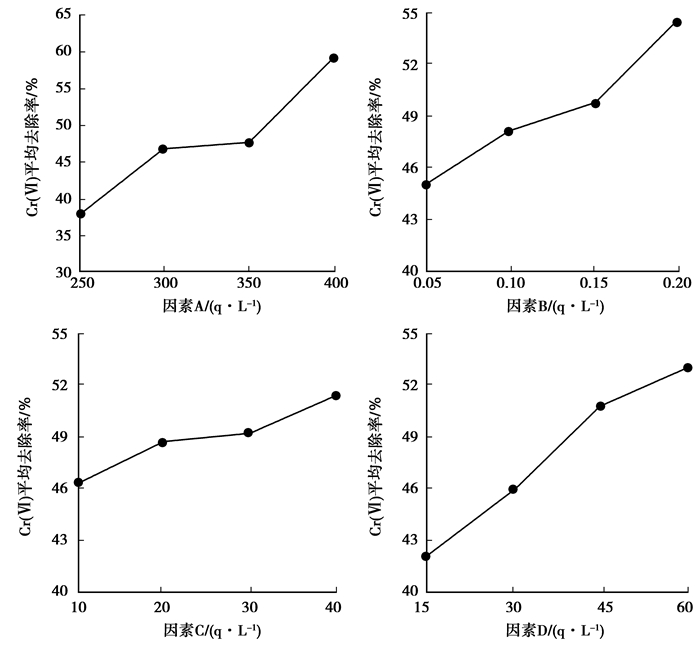
图 2(a)~(d)为各因素效应曲线图。横坐标为因素值,纵坐标为六价铬去除率。结果表明:各因素对Ni/Fe-AC BPs的还原性能的影响程度依次为A>D>B>C,与直观分析结果一致;整体上,FeSO4·7H2O质量浓度越高,Cr(Ⅵ)去除率越高,Ni/Fe-AC BPs的主要成分可能是Fe0,是去除Cr(Ⅵ)的有效成份;硼酸的质量浓度变化对六价铬去除率影响最小;引入Mn2+可增强阴极电化学极性,有效降低了浓差极化,提高沉积液分散能力,改善沉积条件,与已有研究结论一致[27]。
|
图 2 因素A~D的效应曲曲线图 Fig. 2 The effect curves of factor A, B, C and D |
综上分析,增大硫酸亚铁、硼酸及硫酸锰的质量浓度或提高铁镍比,所配沉积液均有利于所制Ni-Fe双金属颗粒性能的提升,能达到优化制备的目的。但配制沉积液预试验表明:当FeSO4·7H2O质量浓度为400 g/L,铁镍质量比为0.2时,硼酸40 g/L,MnSO4·H2O质量浓度为60 g/L,在30 ℃水浴条件下达到最大溶解限度。所以,试验最终以A4B4C4D4为最优沉积液配比,在此条件下所制Ni/Fe-AC BPs对六价铬的去除率可达63.16%。
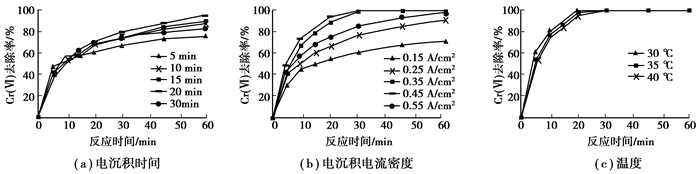
2.1.2 电沉积条件的优化在最优沉积液配比下,通过控制变量法进行单因素试验,研究不同电沉积时间、电流密度和温度下Ni/Fe-AC BPs对六价铬的去除率见图 3。
|
图 3 不同影响因素对六价铬去除率的影响 Fig. 3 Different influence factors on the removal rate of hexavalent chromium |
在电沉积电流密度为0.25 A/cm2,电沉积温度为30 ℃条件下,控制电沉积时间为5,10,15,20,30 min,制备Ni/Fe-AC BPs,并对40 mg/L六价铬溶液进行去除试验,结果如图 3(a)所示。由图 3(a)分析可得:不同电沉积时间对Cr(Ⅵ)去除速率的趋势大体一致,均先快后慢,最后趋于稳定;不同电沉积时间所制Ni-Fe双金属颗粒在相同条件下对Cr(Ⅵ)去除率不同,随着时间的增加,Cr(Ⅵ)去除率增高后降低,最佳电沉积时间为10 min。分析原因为随着反应的进行,有效Ni-Fe金属颗粒数逐渐减少,活性点位减少,最后趋于耗尽,因此,效应曲线呈现出先快后慢,最后趋于稳定的趋势;随着沉积时间的增长,制得的Ni/Fe金属颗粒越多,去除率先增高,当电沉积时间超过某一范围可能导致沉积厚度过大致使原本沉淀在活性炭电极片上的金属颗粒脱落,去除率降低;此外,电极片上的Fe长时间暴露在含氧的沉积液中,易被氧化为Fe3+,丧失还原性能,因此,最佳电沉积时间为10 min。
在最佳电沉积时间10 min前提下,控制电沉积温度30 ℃,分别于0.15,0.25,0.35,0.45,0.55 A/cm2的电流密度下制备Ni/Fe-AC BPs,并以六价铬去除率为指标进行性能试验,试验结果如图 3(b)所示。结果表明,当电流密度小于0.45 A/cm2时,随着电流密度的不断增大,六价铬去除率呈不断上升趋势,去除速度也逐渐加快;当电流密度大于0.45 A/cm2时,六价铬去除率反而降低,最佳电流密度为0.45 A/cm2,30 min时Cr(Ⅵ)去除率可达到100%。分析可能原因为Ni/Fe双金属电沉积属于异相共沉积,Fe优先析出,随着电流密度的增大,铁镍电沉积速度加快,阴极表面附近的Fe2+被大量消耗,形成了一个Fe2+的贫瘠区,导致纳米Fe颗粒沉积受到限制,而纳米Ni颗粒的沉积,使得阴极片上沉积的金属Fe颗粒过少而金属Ni颗粒过多,使Ni/Fe-AC BPs对六价铬的去除率低;当阴极电流密度过大时,会造成镀层烧焦,析氢严重,镀层质量差。
在最佳电沉积时间10 min,电沉积密度0.45 A/cm2条件下,控制电沉积温度依次为30,35,40 ℃,制备Ni/Fe-AC BPs,并六价铬去除效果进行分析,结果如图 3(c)所示。随着电沉积温度的升高,六价铬的去除速度提高,当反应平衡时Cr(Ⅵ)去除率一样,说明电沉积温度对六价铬的去除率影响不大。分析主要原因可能是:虽然沉积液温度升高,能有效降低阴极极化,有利于增大阴极电流密度,提升电沉积速率,增加Ni-Fe金属颗粒,但温度的升高会降低沉积的稳定性,促使Fe2+氧化加速,导致沉积液中Fe2+浓度降低,从而使得阴极片上沉积有效金属颗粒含量降低,因此,温度对制备的有效金属颗粒影响不大,主要影响反应速率。综合节能和增加反应速率两方面考虑,确定40 ℃为最优电沉积温度。
2.1.3 Ni/Fe-AC BPs性能试验结果分析由表 1可知,AC、Fe-AC和Ni/Fe-AC BPs对六价铬的去除效果差异显著,在反应15 min时,AC、Fe-AC和Ni/Fe-AC BPs所对应六价铬的去除率分别为3.40%,47.34%,85.76%;反应30 min时,AC、Fe-AC和Ni/Fe-AC BPs所对应六价铬的去除率分别为5.43%,59.18%,100%。总的来看,AC对六价铬的物理吸附去除作用非常微弱,反应进行30 min去除率也仅有5.43%,Ni/Fe-AC BPs对六价铬的去除效果最佳。
| 表 1 相同条件下AC、Fe-AC、Ni/Fe-AC BPs对六价铬去除效果 Table 1 Effect of AC, Fe-AC, Ni/Fe-AC BPs on removal of hexavalent chromium under the same conditions |
分析原因,可能是试验中所用活性炭是电沉积法制备Fe-AC和Ni/Fe-AC BPs所用活性炭电极片,其尺寸小,且掺有石墨及泡沫镍,活性炭含量不高,且压制成电极片使其表面性能降低、孔隙率下降,由此导致活性炭对六价铬去除效果十分微弱。而Ni/Fe-AC BPs效果最佳,可能是因为在Fe-AC的基础新增催化金属Ni颗粒,降低零价Fe颗粒与六价铬氧化还原反应所需活化能,加快反应速率,有效提高六价铬的去除率。此外,零价Fe颗粒与金属Ni颗粒可在反应溶液中形成微小的原电池,Fe将电子转移给Ni,有利于提高对六价铬的去除效果。
2.2 Ni/Fe-AC BPs的形貌结果特征试验结果表明,在最佳沉积液配比和在电流密度0.45 A/cm2,温度40 ℃,电沉积10 min的最优电沉积条件下制得的Ni/Fe-AC BPs对40 mg/L的Cr(Ⅵ)去除率可高达100%。为了进一步证明金属修饰和固体负载两种改性方法结合电沉积法成功制备了性能优越的镍铁双金属颗粒,本试验对最佳条件下制得的双金属颗粒进行了电镜扫描、能谱图及比表面积表征分析,分析结果如下。
2.2.1 FESEM结构分析图 4所示为最优工艺条件下制备的Ni/Fe-AC BPs在500,2 000,10 000倍下的扫描电镜图片。

|
图 4 Ni/Fe-AC BPs FESEM图 Fig. 4 FESEM figure of Ni/Fe-AC BPs |
FESEM表征结果如图 4(a)~(c)所示。活性炭电极片经过电沉积负载Ni/Fe双金属颗粒后,表面上出现许多颗粒细物质,颗粒物呈絮球状颗粒,直径约1 μm,较为均匀的排布在活性炭电极片表面,分散性较好,团聚现象较少,可能为电沉积法制备的Ni/Fe双金属颗粒。
2.2.2 EDS元素组成分析EDS元素分析结果如图 5所示,结果表明活性炭电极片载体表面的主要成分为Fe,O,Ni,C,且Fe,Ni元素含量分别为71.9%,5.0%,说明电沉积法成功地将铁、镍元素沉积到了活性炭电极片上。

|
图 5 Ni/Fe-AC BPs的EDS谱图 Fig. 5 EDS spectrum of Ni/Fe-AC BPs |
图 6为XRD图晶型分析图,由图得所制物质在2θ为44.03°,82.97°时存在两组衍射峰。由铁的标准PDF卡片相关系数[28]得44.03°,82.97°的两组衍射峰分别对应bcc-Fe0的110衍射峰和211衍射峰,证明了Ni/Fe-AC BPs上存在α-Fe0。零价镍的衍射峰对应78°左右的位置,XRD图示并不明显,结合EDS分析可能是因为镍含量过少(5%)而导致衍射峰显示不明显。

|
图 6 Ni/Fe-AC BPs的XRD谱图 Fig. 6 XRD spectrum of Ni/Fe-AC BPs |
比表面积分析仪测得电沉积前后样品的比表面积分别为711.345 m2/g、388.637 m2/g。研究发现,电沉积后活性炭电极片的比表面积降低到原来的47.60%,分析表明活性炭电极片表面基本被铁-镍双金属颗粒覆盖,比表面积变小,Ni/Fe-AC BPs的吸附性能不如活性炭,但理论上仍具有一定的吸附性能。
3 结论试验结果表明电沉积法制备Ni/Fe-AC BPs的最佳沉积液物料配比为硫酸亚铁400 g/L,硫酸镍80 g/L,硼酸40 g/L,硫酸锰60 g/L;最佳电沉积条件为电流密度为0.45 A/cm2,电沉积温度40 ℃,电沉积10 min,此条件下制备的Ni/Fe-AC BPs对40 mg/L的六价铬在20 min的去除率可达到100%。
同时,对最佳沉积液配比和电沉积条件下制备的双金属颗粒表征结果显示:Ni/Fe双金属颗粒呈絮球状均匀分布于活性炭上,团聚减少;EDS和XRD表征表明成功制备了Ni-Fe双金属颗粒;而BET比表面积分析和AC、Ni/Fe-AC BPs对Cr(Ⅵ)去除效果对比分析表明,活性炭负载Ni/Fe颗粒后比表面积下降47.60%,制备电极片的AC对Cr(Ⅵ)去除20 min,去除率仅5.43%,吸附效果微弱,而Ni/Fe-AC BPs对Cr(Ⅵ)得去除率可达100%,说明Ni/Fe-AC BPs具有良好的催化还原性。
| [1] |
Zhang W J, Gao H Y, He J J, et al. Removal of norfloxacin using coupled synthesized nanoscale zero-valent iron (nZVI) with H2O2 system:Optimization of operating conditions and degradation pathway[J]. Separation and Purification Technology, 2017, 172: 158-167. DOI:10.1016/j.seppur.2016.08.008 |
| [2] |
Boparai H K, O'Carroll D M. Removal of trichloroethylene and heavy metals by zerovalent iron nanoparticles[C]//Proceedings of the AGU Spring Meeting. American Geophysical Union, 2009.
|
| [3] |
Krishna L S, Soontarapa K, Yuzir A, et al. Kaolin-nano scale zero-valent iron composite (K-nZVI):synthesis, characterization and application for heavy metal removal[J]. Desalination and Water Treatment, 2017, 100: 168-177. DOI:10.5004/dwt.2017.21754 |
| [4] |
Yang X C, Shen X Q, Jing M X, et al. Removal of heavy metals and dyes by supported nano zero-valent iron on barium ferrite microfibers[J]. Journal of Nanoscience and Nanotechnology, 2014, 14(7): 5251-5257. DOI:10.1166/jnn.2014.8687 |
| [5] |
Zarime N A, Yaacob W Z W, Jamil H. Removal of heavy metals using bentonite supported nano-zero valent iron particles[C/OL]//AIP Conference Proceedings. AIP, 2018.[2019-04-02]. https://doi.org/10.1063/1.5027944.
|
| [6] |
Kang S H, Liu S W, Wang H M, et al. Enhanced degradation performances of plate-like micro/nanostructured zero valent iron to DDT[J]. Journal of Hazardous Materials, 2016, 307: 145-153. DOI:10.1016/j.jhazmat.2015.12.063 |
| [7] |
Mao Z, Wu Q Z, Wang M, et al. Tunable synthesis of SiO2-encapsulated zero-valent iron nanoparticles for degradation of organic dyes[J]. Nanoscale Research Letters, 2014, 9(1): 501. DOI:10.1186/1556-276X-9-501 |
| [8] |
Shi L N, Zhang X, Chen Z L. Removal of Chromium (Ⅵ) from wastewater using bentonite-supported nanoscale zero-valent iron[J]. Water Research, 2011, 45(2): 886-892. DOI:10.1016/j.watres.2010.09.025 |
| [9] |
Laumann S, MicićV, Hofmann T. Mobility enhancement of nanoscale zero-valent iron in carbonate porous media through co-injection of polyelectrolytes[J]. Water Research, 2014, 50: 70-79. DOI:10.1016/j.watres.2013.11.040 |
| [10] |
Tomašević D D, Kozma G, Kerkez D V, et al. Toxic metal immobilization in contaminated sediment using bentonite- and kaolinite-supported nano zero-valent iron[J]. Journal of Nanoparticle Research, 2014, 16(8): 2548. DOI:10.1007/s11051-014-2548-2 |
| [11] |
Trujillo-Reyes J, Peralta-Videa J R, Gardea-Torresdey J L. Supported and unsupported nanomaterials for water and soil remediation:are they a useful solution for worldwide pollution?[J]. Journal of Hazardous Materials, 2014, 280: 487-503. DOI:10.1016/j.jhazmat.2014.08.029 |
| [12] |
Kuang Y, Du J H, Zhou R B, et al. Calcium alginate encapsulated Ni/Fe nanoparticles beads for simultaneous removal of Cu (Ⅱ) and monochlorobenzene[J]. Journal of Colloid and Interface Science, 2015, 447: 85-91. DOI:10.1016/j.jcis.2015.01.080 |
| [13] |
张智敏, 王自为, 张晔, 等. 电化学沉积法制备纳米铁微粒及其性能的研究[J]. 山西大学学报(自然科学版), 2003, 26(3): 235-237. ZHANG Zhimin, WANG Ziwei, ZHANG Ye, et al. Study on preparation with electrodeposition and properties of nanometer-sized Fe[J]. Journal of Shanxi University(Natural Science Edition), 2003, 26(3): 235-237. (in Chinese) DOI:10.3969/j.issn.0253-2395.2003.03.012 |
| [14] |
Petala E, Dimos K, Douvalis A, et al. Nanoscale zero-valent iron supported on mesoporous silica:Characterization and reactivity for Cr(Ⅵ) removal from aqueous solution[J]. Journal of Hazardous Materials, 2013, 261: 295-306. DOI:10.1016/j.jhazmat.2013.07.046 |
| [15] |
Kim S A, Kamala-Kannan S, Lee K J, et al. Removal of Pb(Ⅱ) from aqueous solution by a zeolite-nanoscale zero-valent iron composite[J]. Chemical Engineering Journal, 2013, 217: 54-60. DOI:10.1016/j.cej.2012.11.097 |
| [16] |
Messele S A, Bengoa C, Stüber F, et al. Catalytic wet peroxide oxidation of phenol using nanoscale zero-valent iron supported on activated carbon[J]. Desalination and Water Treatment, 2016, 57(11): 5155-5164. DOI:10.1080/19443994.2014.1002011 |
| [17] |
Shi J L, Long C, Li A M. Selective reduction of nitrate into nitrogen using Fe-Pd bimetallic nanoparticle supported on chelating resin at near-neutral pH[J]. Chemical Engineering Journal, 2016, 286: 408-415. DOI:10.1016/j.cej.2015.10.054 |
| [18] |
Shen W J, Mu Y, Wang B N, et al. Enhanced aerobic degradation of 4-chlorophenol with iron-nickel nanoparticles[J]. Applied Surface Science, 2017, 393: 316-324. DOI:10.1016/j.apsusc.2016.10.020 |
| [19] |
Weng X L, Sun Q, Lin S, et al. Enhancement of catalytic degradation of amoxicillin in aqueous solution using clay supported bimetallic Fe/Ni nanoparticles[J]. Chemosphere, 2014, 103: 80-85. DOI:10.1016/j.chemosphere.2013.11.033 |
| [20] |
Lu Z Q, Xu Y L, Zhou S M. High saturation magnetization superparamagnetic Fe/Ni core/shell microparticles for chromium removal[J]. RSC Advances, 2017, 7(67): 42363-42369. DOI:10.1039/C7RA04104G |
| [21] |
Zhou S M, Li Y, Chen J T, et al. Enhanced Cr(vi) removal from aqueous solutions using Ni/Fe bimetallic nanoparticles:characterization, kinetics and mechanism[J]. RSC Adv, 2014, 4(92): 50699-50707. DOI:10.1039/C4RA08754B |
| [22] |
Gonçalves A A, Araújo A F, de Mesquita J P, et al. Characterisation of silica-supported Fe-Ni bimetallic nanoparticles and kinetic study of reductive degradation of the drug nimesulide[J]. Journal of Environmental Chemical Engineering, 2016, 4(4): 4354-4365. DOI:10.1016/j.jece.2016.09.038 |
| [23] |
Schrick B, Blough J L, Jones A D, et al. Hydrodechlorination of trichloroethylene to hydrocarbons using bimetallic nickel-iron nanoparticles[J]. Chemistry of Materials, 2002, 14(12): 5140-5147. DOI:10.1021/cm020737i |
| [24] |
Kadu B S, Wani K D, Kaul-Ghanekar R, et al. Degradation of doxorubicin to non-toxic metabolites using Fe-Ni bimetallic nanoparticles[J]. Chemical Engineering Journal, 2017, 325: 715-724. DOI:10.1016/j.cej.2017.05.097 |
| [25] |
Li X L, Xue Z. The effect of electrochemical conditions on morphology and properties of Bi2Se3 thick films by electrodeposition[J]. Materials Letters, 2014, 129: 1-4. DOI:10.1016/j.matlet.2014.05.009 |
| [26] |
Ghalandari K. Investigation of the key factors influencing on successful offer of Internet banking services in Iran:presenting a predictive model using decision tree[J]. Middle-East Journal of Scientific Research, 2012, 12(5): 707-716. |
| [27] |
田永常, 方小红, 潘秉锁, 等. 不同氯化锰含量对铁电沉积过程的影响[J]. 材料保护, 2014, 47(6): 9-12. TIAN Yongchang, FANG Xiaohong, PAN Bingsuo, et al. Effect of manganese chloride content on cathodic process of iron electrodeposition[J]. Journal of Materials Protection, 2014, 47(6): 9-12. (in Chinese) |
| [28] |
肖利, 张斯淇, 刘晓静, 等. 关于X射线在晶体中衍射的理论研究[J]. 核电子学与探测技术, 2012, 32(1): 83-86. XIAO Li, ZHANG Siqi, LIU Xiaojing, et al. Research on X-ray diffraction in crystal[J]. Nuclear Electronics & Detection Technology, 2012, 32(1): 83-86. (in Chinese) DOI:10.3969/j.issn.0258-0934.2012.01.018 |
 2019, Vol. 42
2019, Vol. 42


