攀西地区拥有丰富的钒钛磁铁矿资源,在实现钒资源的综合高效利用过程中,二次选矿后得到的钛精矿是生产钛产品的原料,但钛精矿品位低,钙镁含量高[1-2],给传统的冶炼工艺带来了复杂性和难度,难以实现钛精矿的高效提取利用。电炉法可实现钛渣的冶炼,但无法实现对非铁杂质的去除,不能直接用于氯化法生产钛白。硫酸法和盐酸法虽除钙镁杂质强,但能耗高,设备腐蚀严重,产生的废酸量大,环境污染严重。钛精矿中高含量的钙镁杂质严重遏制了攀西地区钛资源的综合利用[3-4]。因此,如何绿色高效分离钛精矿中的钙镁杂质是影响我国钛资源综合利用的关键所在。
近年来,许多学者针对钛精矿还原过程中的物相变化[5]和还原历程[6-7]进行了研究,并在预处理[8]、添加剂[9-10]和外场条件[11-12]对钛精矿的中低品位矿强化还原的影响方面也做了一系列的研究,以上方式均能一定程度地强化钛精矿的还原,降低反应温度或缩短反应时间,提高钛渣品位,优化冶炼工艺,但仍然不能有效地去除钙镁等杂质。Huang等[13-15]结合理论和实验研究,提出真空碳热还原钛精矿制备高品位钛渣的新工艺,该工艺在温度超过1 500 ℃,配碳量高于12%时,有效地去除钙镁等杂质,得到较高品位的钛渣(93%TiO2,CaO+MgO<0.45%)。然而,该新工艺还原过程中的物相变化及还原历程还需要进一步探明。因此,笔者针对真空碳热还原钛精矿制备高品位钛渣新工艺中钛精矿还原过程中的物相变化进行研究,探明其还原历程,为真空碳热还原钛精矿制备高品位钛渣新工艺提供理论基础。
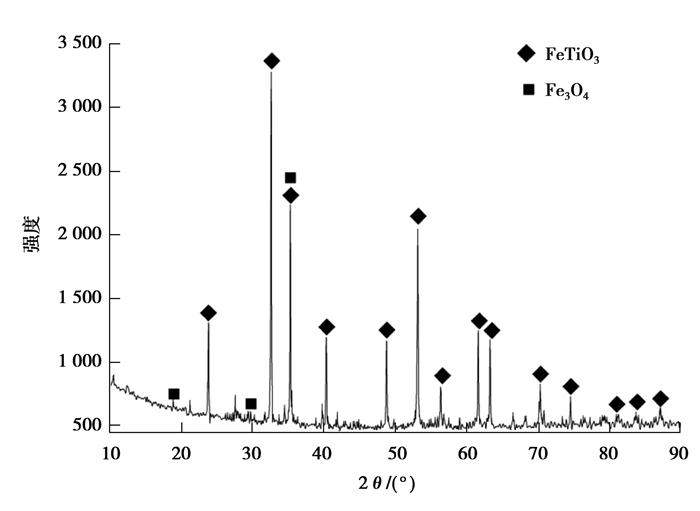
1 实验 1.1 原料及设备实验所用钛精矿和焦粉均取自于攀枝花某企业,其化学成分如表 1和2所示。钛精矿的XRD图谱如图 1所示,钛精矿的主要物相为钛铁矿和少量的磁铁矿。钛精矿和焦粉粒度均小于75 μm。
| 表 1 钛铁矿精矿化学成分(以质量分数计) % Table 1 Chemical composition of the ilmenite concentrate |
| 表 2 焦炭的化学成分(以质量分数计) % Table 2 Chemical composition of the dried coke |
|
图 1 钛精矿的X射线衍射图 Figure 1 XRD diagram of ilmenite concentrate |
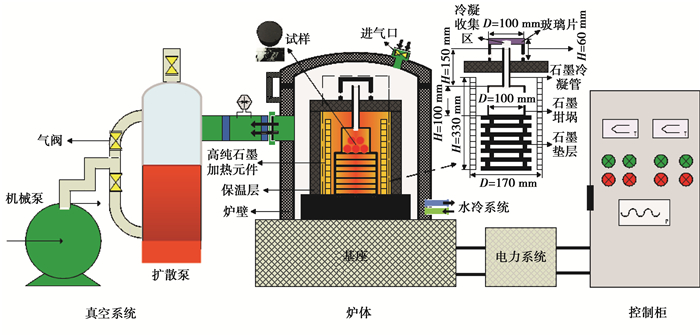
实验所用真空碳管炉是以高纯石墨作为发热元件,结构如图 2所示,主要由控制柜、真空系统、炉体和冷却系统组成。其中真空系统由机械泵和扩散泵组成,能保持炉内压强处于0.1 Pa状态。
|
图 2 真空碳管炉示意图 Figure 2 Schematic diagram of vacuum carbon tube furnace |
真空还原实验中的还原剂焦炭遵循碳氧摩尔比1 :2(即12%配碳量)进行计算取量,粘结剂为甲基纤维素。将钛精矿、焦炭、粘结剂和水充分混匀后放入圆柱体模具中压样,压力约为15 MPa,单个试样质量约为24.07 g,直径30 mm,高度13 mm。试样在105 ℃下干燥120 min后,在真空碳管炉内进行碳热还原,升温速率为6 ℃/min,设定温度分别为1 000、1 050、1 100、1 150、1 200、1 250、1 300、1 350、1 400 ℃。当温度到达预设温度时,立即停止加热,通过水循环冷却,冷却至室温后取出试样称质量,然后对试样进行化学元素、光学显微镜、扫描电镜背散射电子成像(BSE)、能量色散X射线光谱(EDS)和XRD分析。
真空碳热还原过程中,碳夺取钛精矿中金属氧化物的氧元素,形成气体逸出,导致试样质量发生变化。因此,还原过程中金属不发生挥发时,失质量率在一定程度上可以表征试样的还原程度,计算公式如下所示:
| $ \alpha =\frac{{{m}_{0}}-{{m}_{1}}-{{m}_{2}}}{{{m}_{0}}-{{m}_{2}}}\times 100\%, $ | (1) |
式中:α为失质量率;m0为还原前试样的质量;m1为还原后试样的质量;m2为添加粘结剂的质量。
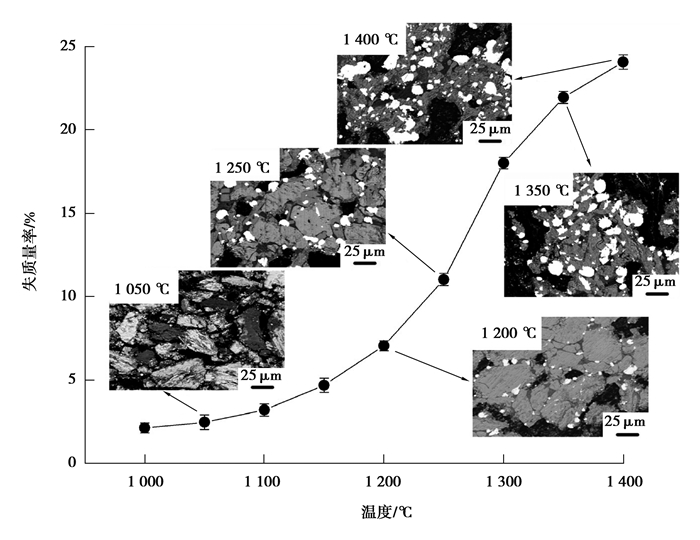
2 结果与讨论 2.1 还原温度对试样失质量率的影响试样的失质量率和微观形貌随温度的变化情况如图 3所示。由图可知,随着还原温度的升高,失质量率持续上升,上升趋势在1 200 ℃时增加,1 300 ℃时减缓,说明还原温度能促进还原反应的进行;试样的微观形貌随着还原温度的升高而变得平整规则,且亮白色的金属相聚集长大,进一步说明随着还原温度的升高,金属氧化物被还原,并形核长大。
|
图 3 还原温度对试样的失质量率和微观形貌的影响 Figure 3 Effect of reduction temperature on the mass loss rate and micromorphology of the sample |
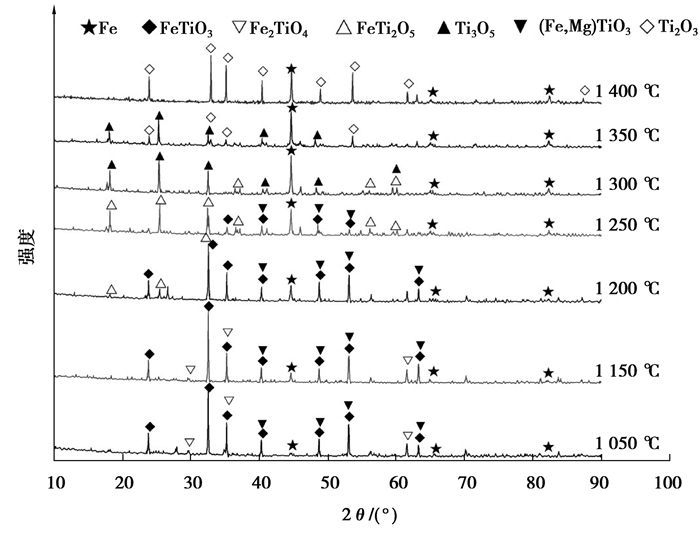
为研究真空碳热还原钛精矿中物相变化过程,分别对不同温度下的试样进行X射线衍射分析,结果如图 4所示。1 200 ℃之前出现Fe2TiO4相特征峰,这与之前的研究[7, 16]结果相似。由于实验所用钛精矿中含有少量的磁铁矿,在低温过程中反应为:
| $ \text{F}{{\text{e}}_{\text{3}}}{{\text{O}}_{\text{4}}}\text{+C=3FeO+CO;} $ | (2) |
| $ \text{FeO+C=Fe+CO;} $ | (3) |
| $ \text{FeTi}{{\text{O}}_{3}}+\text{FeO}=\text{F}{{\text{e}}_{2}}\text{Ti}{{\text{O}}_{4}}; $ | (4) |
| $ \text{F}{{\text{e}}_{\text{2}}}\text{Ti}{{\text{O}}_{\text{4}}}\text{+C=Fe+FeTi}{{\text{O}}_{\text{3}}}\text{+CO}。$ | (5) |
|
图 4 不同温度下还原样品的XRD图谱 Figure 4 XRD diagram of the reduced samples at different temperatures |
1 200 ℃时Fe2TiO4相特征峰消失,FeTi2O5相特征峰出现,FeTiO3和(Fe,Mg)TiO3特征峰强度减弱;1 250 ℃时FeTiO3和(Fe,Mg)TiO3特征峰强度继续减弱,FeTi2O5相特征峰强度急剧增加,此阶段主要反应为:
| $ \text{2FeTi}{{\text{O}}_{\text{3}}}\text{+C=Fe+FeT}{{\text{i}}_{\text{2}}}{{\text{O}}_{\text{5}}}\text{+CO;} $ | (6) |
| $ \text{3/5FeT}{{\text{i}}_{\text{2}}}{{\text{O}}_{\text{5}}}\text{+C=3/5Fe+2/5T}{{\text{i}}_{\text{3}}}{{\text{O}}_{\text{5}}}\text{+CO}。$ | (7) |
1 300 ℃时FeTiO3和(Fe,Mg)TiO3特征峰消失,Ti3O5相特征峰出现。1 350 ℃时FeTi2O5相特征峰消失,Ti3O5相特征峰强度减弱,Ti2O3相特征峰出现。1 400 ℃时Ti3O5相特征峰消失,Ti2O3相特征峰强度增加。此阶段反应为:
| $ 2\text{T}{{\text{i}}_{3}}{{\text{O}}_{5}}+\text{C}=3\text{T}{{\text{i}}_{2}}{{\text{O}}_{3}}+\text{C}{{\text{O}}}。$ | (8) |
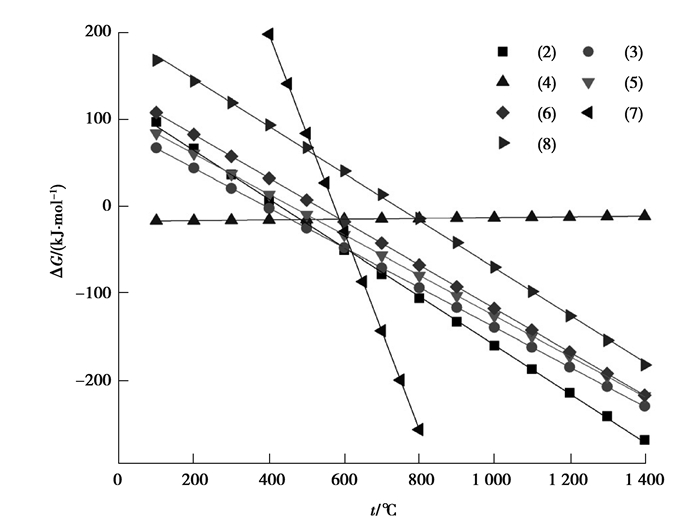
实验过程中,随着还原反应进行,产生的气体会逸出试样,导致炉内压强上升,但最高不超过10 Pa。真空系统会随时将炉内的气体抽出,当还原反应减弱时,炉内的压强下降并稳定在0.1 Pa左右。因此运用FactSage 7.2软件中的Reaction模块在10 Pa压强下对式(2)~(8)的反应进行热力学计算,得到反应吉布斯自由能与温度的关系如图 5所示。
|
图 5 还原反应在10 Pa下的吉布斯自由能ΔG与温度t的关系图 Figure 5 Relationships between Gibbs free energy ΔG and temperature t of the reduction reactions at 10 Pa |
随着还原温度升高,Fe相特征峰强度逐渐增加,在1 200~1 250 ℃阶段快速增加。最终还原试样的主要物相为Ti2O3和Fe,因此,在1 000~1 400 ℃还原过程中,除了初期少量的Fe2TiO4还原成FeTiO3外,钛精矿的还原历程主要为:FeTiO3→FeTi2O5→Ti3O5→Ti2O3。通过还原过程的分析,将1 000~1 400 ℃的还原过程分为3个阶段,第1阶段(1 000~1 200 ℃,式(2)~(5)发生的少量还原反应阶段)还原反应式多但反应的量少;第2阶段(1 200~1 300 ℃,式(6)~(7)发生的FeTiO3→FeTi2O5→Ti3O5阶段)还原反应式少,但是主要还原阶段,反应大量发生;第3阶段(1 300~1 400 ℃,式(8)发生的Ti3O5→Ti2O3阶段)为钛的高价氧化物向低价氧化物的转化阶段。
2.3 微观形貌分析对还原试样进行BSE和EDS分析,分析结果如图 6和表 3所示。结合图 4的分析可知,图 6中a代表的区域主要是FeTiO3,有少量的Fe2TiO4。在1 250 ℃时,进入剧烈还原反应阶段,此时出现b和c代表的两种不同区域,通过EDS分析可知,b区域主要为FeTiO3,但含有少量的FeTi2O5,而c区域则主要是FeTi2O5。d和e区域分别是Ti3O5和Ti2O3,这与图 4中分析的还原历程一致。f1,f2和f3为金属铁相区域,且从f1→f2→f3,金属铁相形核长大,1 350 ℃时,有硅进入铁相。

|
图 6 不同温度还原试样的微观形貌图 Figure 6 Microstructure of reduced samples at different temperatures |
| 表 3 不同区域EDS元素原子百分比的平均值 % Table 3 The average atomic percentage of EDS elements at different areas |
由表 3的原子比可知,在a、b、c、d和e代表的富钛区域,有镁和铝存在,因为在1 300 ℃之前的还原阶段,铁逐渐被还原且镁会取代部分铁,形成稳定钛铁矿(Fe,Mg)TiO3[17],从而降低铁的还原效果,但在1 300 ℃高温时钛铁矿(Fe, Mg)TiO3消失。当温度高于1 250 ℃时,会生成钛的低价氧化物(Ti3O5和Ti2O3),而钛的低价氧化物则会与镁铝等氧化物形成M3O5的固溶体[18],其中M=Fe、Ti、Mg、Mn、Al,从而降低铁的还原效果[19-20]。
3 结论运用FactSage、XRD和BSE-EDS分析手段研究了在1 000~1 400 ℃下真空碳热还原钛精矿的物相变化及还原历程,主要得到以下结论:
1) 随着还原温度升高,失质量率持续上升,还原温度能促进还原反应进行和金属铁的形核长大,且在1 350 ℃时,有硅进入铁相。
2) 在1 000~1 400 ℃还原过程中,除了初期少量的Fe2TiO4→FeTiO3外,钛精矿的还原历程主要为FeTiO3→FeTi2O5→Ti3O5→Ti2O3。铁氧化物被还原为金属铁并形核长大,钛氧化物则由高价向低价转变,最终主要物相为Ti2O3和金属铁。
3) 在1 300 ℃之前的还原阶段中,镁会取代FeTiO3中的部分铁形成(Fe,Mg)TiO3固溶体,减弱铁的还原效果,但在1 300 ℃时,(Fe,Mg)TiO3固溶体会消失。当温度高于1 250 ℃时,还原反应生成钛的低价氧化物(Ti3O5和Ti2O3)会与镁铝等氧化物形成M3O5的固溶体,其中M=Fe、Ti、Mg、Mn、Al,从而减弱铁的还原效果。
| [1] |
邓国珠. 钛冶金[M]. 北京: 冶金工业出版社, 2010: 55-55. DENG Guozhu. Titanium metallurgy[M]. Beijing: Metallurgical Industry Press, 2010: 55-55. (in Chinese) |
| [2] |
李大成, 纪安, 扈玫珑. 钒钛磁铁矿提钒新工艺研究[J]. 重庆大学学报, 2018, 41(10): 45-52. LI Dacheng, JI An, HU Meilong. A new process of vanadium extraction from vanadium-titanium magnetite[J]. Journal of Chongqing University, 2018, 41(10): 45-52. (in Chinese) DOI:10.11835/j.issn.1000-582X.2018.10.005 |
| [3] |
李大成, 周大利, 刘恒. 镁热法海绵钛生产[M]. 北京: 冶金工业出版社, 2009: 5-6. LI Dacheng, ZHOU Dali, LIU Heng. Sponge titanium production of magnesiothermy[M]. Beijing: Metallurgical Industry Press, 2009: 5-6. (in Chinese) |
| [4] |
莫畏, 邓国珠, 罗方承. 钛冶金[M]. 2版. 北京: 冶金工业出版社, 1998: 124-124. MO Wei, DENG Guozhu, LUO Fangcheng. Titanium metallurgy[M]. 2nd ed. Beijing: Metallurgical Industry Press, 1998: 124-124. (in Chinese) |
| [5] |
Dewan M A R, Zhang G Q, Ostrovski O. Phase development in carbothermal reduction of ilmenite concentrates and synthetic rutile[J]. ISIJ International, 2010, 50(5): 647-653. DOI:10.2355/isijinternational.50.647 |
| [6] |
Gou H P, Zhang G H, Hu X J, et al. Kinetic study on carbothermic reduction of ilmenite with activated carbon[J]. Transactions of Nonferrous Metals Society of China, 2017(8): 1856-1861. |
| [7] |
Fu X, Wang Y, Wei F. Phase transitions and reaction mechanism of ilmenite oxidation[J]. Metallurgical and Materials Transactions A, 2010, 41(5): 1338-1348. DOI:10.1007/s11661-010-0173-y |
| [8] |
Ranganathan S, Bhattacharyya K, Ray K, et al. Investigations on the reduction and growth of particles of iron from ilmenite ore[J]. Mineral Processing and Extractive Metallurgy, 2012, 121(1): 55-63. |
| [9] |
Huang R, Lv X, Bai C G, et al. Enhancement reduction of Panzhihua ilmenite concentrate with coke and conglomeration of metal with ferrosilicon[J]. Steel Research International, 2013, 84(9): 892-899. DOI:10.1002/srin.v84.9 |
| [10] |
薛正良, 肖承鹏, 杭桂华, 等. CaF2强化红土镍矿自还原过程中金属相聚集长大行为[J]. 重庆大学学报, 2017, 40(12): 43-51. XUE Zhengliang, XIAO Chengpeng, HANG Guihua, et al. Promoting effects of CaF2 on the aggregation and growth of metal phases in self-reduction of laterite nickel ore[J]. Journal of Chongqing University, 2017, 40(12): 43-51. (in Chinese) DOI:10.11835/j.issn.1000-582X.2017.12.006 |
| [11] |
Chen Y, Hwang T, Marsh M, et al. Mechanically activated carbothermic reduction of ilmenite[J]. Metallurgical and Materials Transactions A, 1997, 28(5): 1115-1121. DOI:10.1007/s11661-997-0277-1 |
| [12] |
Lv W, Bai C G, Lv X, et al. Carbothermic reduction of ilmenite concentrate in semi-molten state by adding sodium sulfate[J]. Powder Technology, 2018, 340: 354-361. DOI:10.1016/j.powtec.2018.09.043 |
| [13] |
Huang R, Liu P S, Yue Y H, et al. Vacuum carbothermic reduction of Panzhihua ilmenite concentrate:a thermodynamic study[J]. Mineral Processing and Extractive Metallurgy Review, 2017, 38(3): 193-198. DOI:10.1080/08827508.2017.1281129 |
| [14] |
Huang R, Liu P S, Qian X, et al. Comprehensive utilization of Panzhihua ilmenite concentrate by vacuum carbothermic reduction[J]. Vacuum, 2016, 134: 20-24. DOI:10.1016/j.vacuum.2016.09.006 |
| [15] |
Huang R, Liu P S, Zhang J Z, et al. Effects of temperature on vacuum carbothermic reduction of Panzhihua ilmenite concentrate[J]. Metallurgist, 2017, 61(5/6): 511-516. |
| [16] |
Hu T, Lv X, Bai C G, et al. Reduction behavior of Panzhihua titanomagnetite concentrates with coal[J]. Metallurgical and Materials Transactions B, 2013, 44(2): 252-260. DOI:10.1007/s11663-012-9783-7 |
| [17] |
Wang Y M, Yuan Z F. Reductive kinetics of the reaction between a natural ilmenite and carbon[J]. International Journal of Mineral Processing, 2006, 81(3): 133-140. DOI:10.1016/j.minpro.2006.07.010 |
| [18] |
侯景潇, 汪琦. 外包法直接还原钛铁矿过程的动力学研究[J]. 有色金属(冶炼部分), 2014(2): 18-20, 38. HOU Jingxiao, WANG Qi. Study on kinetics of direct reduction process of ilmenite[J]. Nonferrous Metals(Extractive Metallurgy), 2014(2): 18-20, 38. (in Chinese) DOI:10.3969/j.issn.1007-7545.2014.02.005 |
| [19] |
Pesl J, Eric R H. High temperature carbothermic reduction of Fe2O3-TiO2-MxOy oxide mixtures[J]. Minerals Engineering, 2002, 15(11): 971-984. DOI:10.1016/S0892-6875(02)00136-X |
| [20] |
Liu S S, Guo Y F, Qiu G Z, et al. Solid-state reduction kinetics and mechanism of pre-oxidized vanadium-titanium magnetite concentrate[J]. Transactions of Nonferrous Metals Society of China, 2014(10): 3372-3377. |
 2019, Vol. 42
2019, Vol. 42


